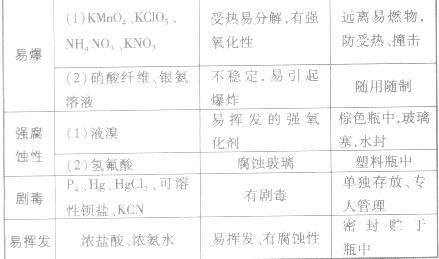
本试题 “下列实验操作中不正确的是( )A.新制的氯水、浓氨水、浓硝酸等装在棕色试剂瓶中B.NaOH溶液、KOH溶液、水玻璃等装在带橡皮塞的无色试剂瓶中C.制NO可以用Cu...” 主要考查您对化学药品的保存、放置
物质的分离
气体的收集、净化、干燥
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学药品的保存、放置
- 物质的分离
- 气体的收集、净化、干燥
物质保存中需注意:
一、 防挥发:
1 .油封:氨水,浓盐酸,浓硝酸等易挥发无机液体,在液面上滴 10 ~ 20 滴矿物油,可以 防止挥发(不可用植物油)。
2 .水封:二硫化碳中加 5mL 水,便可长期保存。汞上加水,可防汞蒸气进入空气。汞旁放 些硫粉,一但失落,散布硫粉使遗汞消灭于化学反应中。
3 .腊封:乙醚、乙醇、甲酸等比水轻的或易溶性挥发液体,以及萘、碘等易挥发固体,紧 密瓶塞,瓶口涂腊。 溴除进行原瓶腊封外,应将原瓶置于具有活性炭的塑料筒内, 筒口进行 腊封。
二、防潮:
1 .漂白粉、过氧化钠应该进行腊封,防止吸水分解或吸水爆炸。氢氧化钠易吸水潮解,应 该进行腊封; 硝酸铵、 硫酸钠易吸水结状, 倒不出来, 以至导致试剂瓶破裂, 也应严密腊封。
2 .碳化钙、无水硫酸铜、五氧化二磷、硅胶极易吸水变质,红磷易被氧化,然后吸水生成 偏磷酸,以上各物均应存放在干燥器中。
3 .浓硫酸虽应密闭,防止吸水,但因常用,故宜放磨口瓶中,磨口瓶塞应该原配,切勿对调。
4 .“ 特殊药品 ” 的地下室,下层布块灰,中层布熟石灰上层布双层柏油纸,方可存放药物。
三、防变质:
1 .防氧化:亚硫酸钠、硫酸亚铁、硫代硫酸钠均易被氧化,瓶口应涂腊。
2 .防碳酸化:硅酸钠、过氧化钠、苛性碱均易吸收二氧化碳,应该涂腊。
3 .防风化:晶体碳酸钠、晶体硫酸铜应进行腊封,存放在地下室中。
4 .防分解:碳酸氢铵、浓硝酸受热易分解,涂腊后,存放在地下室中。
5 .活性炭能吸附多种气体而变质,(木炭亦同),应放在干燥器中。
6 .黄磷遇空气易自燃,永远保存水中,每 15 天查水一次:磷试剂瓶中加水、置于有水水 糟中,上加钟罩封闭。
7 .钾、钠保存在火油中。
8.硫酸亚铁溶液中滴几滴稀硫酸,加入过量细铁粉,进行腊封。
9 .葡萄糖溶液容易霉变,稍加几滴甲醛即可保存。
10 .甲醛易聚合,应开瓶后立即加少量甲醇;乙醛则加乙醇。
四、防光:
1 .硝酸银,浓硝酸及大部份有机药品应该放在棕色瓶中。
2 .硝酸盐存放在地下室中既防热,又防光、防火还能防震。
3 .有机试剂橱窗一律用黑漆涂染。
4 .实验室用色布窗帘,内红外黑双层。
五、防毒害:
1 .磷、硝酸银、氯酸钾、氯化汞等剧毒物放地下室内,双人双锁,建立档案,呈批取用, 使用记载,定期检查。
2 .磷化钙、磷化铝吸水后放出剧毒性磷化氢,应放在干燥器中保存,贴上红色标签。
3 .由于没有通风橱,经常在地面布石灰,吸附某些毒害气相物质。
4 .浓酸,浓碱、溴、酚等腐蚀的药物,使用红色标签,以示警戒。
六、防震:
1 .硝酸铵震动易爆炸,放地下室中。
2 .自制的大晶体明矾、大晶体硫酸铜,用软纸垫包放大口试剂瓶中,进行缓冲,并按 “ 四位 数字 ” 进行编号入厨。
易变质和具有危险性药品的特性及保存方法:
一、 防挥发:
1 .油封:氨水,浓盐酸,浓硝酸等易挥发无机液体,在液面上滴 10 ~ 20 滴矿物油,可以 防止挥发(不可用植物油)。
2 .水封:二硫化碳中加 5mL 水,便可长期保存。汞上加水,可防汞蒸气进入空气。汞旁放 些硫粉,一但失落,散布硫粉使遗汞消灭于化学反应中。
3 .腊封:乙醚、乙醇、甲酸等比水轻的或易溶性挥发液体,以及萘、碘等易挥发固体,紧 密瓶塞,瓶口涂腊。 溴除进行原瓶腊封外,应将原瓶置于具有活性炭的塑料筒内, 筒口进行 腊封。
二、防潮:
1 .漂白粉、过氧化钠应该进行腊封,防止吸水分解或吸水爆炸。氢氧化钠易吸水潮解,应 该进行腊封; 硝酸铵、 硫酸钠易吸水结状, 倒不出来, 以至导致试剂瓶破裂, 也应严密腊封。
2 .碳化钙、无水硫酸铜、五氧化二磷、硅胶极易吸水变质,红磷易被氧化,然后吸水生成 偏磷酸,以上各物均应存放在干燥器中。
3 .浓硫酸虽应密闭,防止吸水,但因常用,故宜放磨口瓶中,磨口瓶塞应该原配,切勿对调。
4 .“ 特殊药品 ” 的地下室,下层布块灰,中层布熟石灰上层布双层柏油纸,方可存放药物。
三、防变质:
1 .防氧化:亚硫酸钠、硫酸亚铁、硫代硫酸钠均易被氧化,瓶口应涂腊。
2 .防碳酸化:硅酸钠、过氧化钠、苛性碱均易吸收二氧化碳,应该涂腊。
3 .防风化:晶体碳酸钠、晶体硫酸铜应进行腊封,存放在地下室中。
4 .防分解:碳酸氢铵、浓硝酸受热易分解,涂腊后,存放在地下室中。
5 .活性炭能吸附多种气体而变质,(木炭亦同),应放在干燥器中。
6 .黄磷遇空气易自燃,永远保存水中,每 15 天查水一次:磷试剂瓶中加水、置于有水水 糟中,上加钟罩封闭。
7 .钾、钠保存在火油中。
8.硫酸亚铁溶液中滴几滴稀硫酸,加入过量细铁粉,进行腊封。
9 .葡萄糖溶液容易霉变,稍加几滴甲醛即可保存。
10 .甲醛易聚合,应开瓶后立即加少量甲醇;乙醛则加乙醇。
四、防光:
1 .硝酸银,浓硝酸及大部份有机药品应该放在棕色瓶中。
2 .硝酸盐存放在地下室中既防热,又防光、防火还能防震。
3 .有机试剂橱窗一律用黑漆涂染。
4 .实验室用色布窗帘,内红外黑双层。
五、防毒害:
1 .磷、硝酸银、氯酸钾、氯化汞等剧毒物放地下室内,双人双锁,建立档案,呈批取用, 使用记载,定期检查。
2 .磷化钙、磷化铝吸水后放出剧毒性磷化氢,应放在干燥器中保存,贴上红色标签。
3 .由于没有通风橱,经常在地面布石灰,吸附某些毒害气相物质。
4 .浓酸,浓碱、溴、酚等腐蚀的药物,使用红色标签,以示警戒。
六、防震:
1 .硝酸铵震动易爆炸,放地下室中。
2 .自制的大晶体明矾、大晶体硫酸铜,用软纸垫包放大口试剂瓶中,进行缓冲,并按 “ 四位 数字 ” 进行编号入厨。
易变质和具有危险性药品的特性及保存方法:

分离与提纯的原则和要求:
(1)选择分离与提纯方法应遵循的原则
①不增:指不能引入新的杂质。
②不减:指应尽可能减少被分离与提纯的物质的损失。
③易分离:指如果使用试剂除去杂质时,要求反应后的产物跟被提纯的物质容易分离。
④易复原:指分离物或被提纯的物质都要容易复原。
(2)分离与提纯操作过程应遵循“三必须”
①除杂质试剂必须过量;
②过量试剂必须除尽(因过量试剂会带人新的杂质);
③除杂途径必须选最佳。
常见的分离与提纯的方法:
(1)物质分离与提纯常用的物理方法
| 方法 | 适用范围或原理 | 装置 | 举例 | 注意事项 |
| 过滤 | 分离固体和液体混合物 | 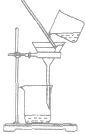 |
粗盐提纯时把粗盐溶于水,经过滤把不溶于水的杂质除去 | ①要“一贴二低三靠” 滤纸紧贴漏斗内壁;滤纸边缘低于漏斗口,漏斗里液面低于滤纸边缘;烧杯口紧靠玻璃棒,玻璃捧下端紧靠三层滤纸.漏斗下端紧靠烧杯内壁。 ②必要时洗涤沉淀物(在过滤器中加少量水),不可搅拌 |
| 结晶 重结晶 |
分离各组分在溶剂中的溶解度随温度变化不同的混合物 | 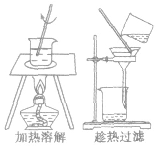 |
KNO3溶解度随温度变化大, NaCl溶解度随温度变化小,可用该法从二者的混合液中提纯KNO3 | ①一般先配较高温度下的浓溶液,然后降温结晶 ②结晶后过滤,分离出晶体 |
| 蒸发 | 溶解度随温度变化较小的物质 |  |
从食盐水溶液中提取食盐晶体 | ①溶质应不易分解、不易水解、不易被氧气氧化 ②蒸发过程应不断搅拌 ③近干时停止加热,余热蒸干 |
| 蒸馏 | 分离沸点不同的液体混合物 | 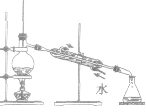 |
制无水乙醇(加生石灰)、硝酸的浓缩[加浓硫酸或 Mg(NO3)2] | ①温度计水银球在蒸馏烧瓶支管口处 ②加沸石(碎瓷片) ③注意冷凝管水流方向应下进上出 ④不可蒸干 |
| 分馏 | 分离多种液态混合物 | 同蒸馏 | 石油分馏 | 同蒸馏 |
| 萃取 | 分离两种互溶的液体 |  |
CCl4把溴水中的Br2萃取出来 |
①萃取后再进行分液操作 ②对萃取剂的要求:与原溶剂互不混溶,不反应;溶质在其中的溶解度比在原溶剂中大;溶质不与萃取剂反应 ③萃取后得到的仍是溶液,一般要通过分馏等方法进一步分离 |
| 分液 | 分离两种不相混溶的液体(密度不同) | 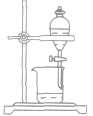 |
水、苯的分离 | 下层液体从下口放出,上层液体从上口倒出 |
| 液化 | 利用气体混合物中某组分易液化的特点来分离 | 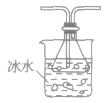 |
除去SO2中的SO3 | 可把锥形瓶换成硬质大试管 |
| 盐析 | 利用某些物质在加某些无机盐时,其溶解度降低而凝聚的性质来分离物质 | —— | 从皂化液中分离肥皂、甘油,蛋白质的盐析 | 盐析是物理变化。盐析之后一般要采取过滤的操作 |
| 洗气 | 杂质气体易溶于某液体 | 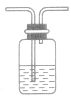 |
除去CO2中的HCl气体,可使混合气体通过盛有饱和NaHCO3 溶液的洗气瓶 | ①从洗气瓶的长导管一端进气 ②混合物中气体溶解度差别较大 |
| 升华 | 利用某些物质有升华的特性 |  |
粗碘中碘与钾、钠、钙、镁的碘化物混合,利用碘易升华的特点将碘与杂质分开 | 升华物质的集取方法不作要求 |
| 渗析 | 胶体提纯、精制 | 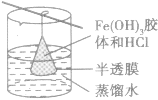 |
除去Fe(OH)3胶体中的HCl | 要不断更换烧杯中的水或改用流动水,以提高渗析效果 |
(2)物质分离与提纯常用的化学方法:
①加热法
混合物中混有某些热稳定性差的物质时,可直接加热,使热稳定性差的物质分解而分离出来。例如:食盐中混有氯化铵、纯碱中混有小苏打等均可直接加热除去杂质。
②沉淀法
在混合物中加入某试剂,使其中一种以沉淀形式分离出去的方法。使用该方法一定要注意不能引入新杂质,若使用多种试剂将溶液中不同粒子逐步沉淀时,应注意后加入试剂能将先加入的过量试剂除去,最后加入的试剂不引入新杂质。例如:加入适量BaCl2溶液可除去NaCl中混有的Na2SO4。
③转化法
利用化学反应将某种物质进行多次转化而分离。例如:分离Fe3+和Al3+时,可加入过量的NaOH溶液,生成Fe(OH)3和NaAlO2,过滤后,分别再加盐酸重新生成Fe3+和Al3+。注意转化过程中尽量减少被分离物质的损失.而且转化后的物质要易恢复为原物质。
④酸碱法
被提纯物质不与酸或碱反应,而杂质可与酸或碱发生反应,可用酸或碱作除杂试剂。例如:用盐酸除去 SiO2中的石灰石,用氢氧化钠除去铁粉中的铝粉。
⑤氧化还原法
a.对混合物中混有的还原性杂质,可加入适当的氧化剂将杂质氧化为被提纯物质。例如:将氯水滴入混有FeCl2的FeCl3溶液中,除去FeCl2杂质。
b.对混合物中混有的氧化性杂质,可加入适当还原剂将杂质还原为被提纯物质。例如:将过量铁粉加入混有FeCl3的FeCl2溶液中,振荡过滤,除去FeCl3 杂质。
⑥调节pH法
通过加入试剂来调节溶液的pH,使溶液中某组分沉淀而分离的方法。一般加入相应的难溶或微溶物来调节。例如:在CaCl2溶液中含有FeCl3杂质,由于 Fe3+水解,溶液呈酸性,可采用调节溶液pH的方法将 Fe3+沉淀除去,为此,可向溶液中加氧化钙或氢氧化钙或碳酸钙等。
⑦电解法
此法利用电解原理来分离、提纯物质。例如:电解精炼铜,将粗铜作阳极,精铜作阴极,电解液为含铜离子的溶液,通直流电,在阳极铜及比铜活泼的杂质金属失电子,在阴极只有铜离子得电子析出,从而提纯了铜。
收集方法及装置:
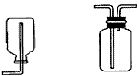
a.排水集气法:适用于收集不溶于水,不与水反应的气体。装置如下:如采用第二个装置,气体应短进长出。

b.向上排空气法:适用于收集密度比空气大不与空气反应的气体,装置如下:如采用第二个装置,气体应长进短出。

c.向下排空气法:适用于收集密度比空气小不与空气反应的气体。装置如下:如采用第二个装置,气体应短进长出。
气体净化:
装置: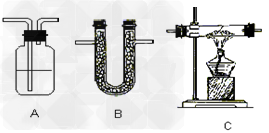

气体干燥:
(1)干燥原则:
干燥剂只能吸收气体中含有的水分而不能与气体发生反应。
①酸性干燥剂不能干燥碱性气体。
②碱性干燥剂不能干燥酸性气体。
③具有强氧化性的干燥剂不能干燥具有强还原性的气体。注意H2、CO、SO2虽具有还原性,但可用浓H2SO4干燥。
(2)常见物质干燥
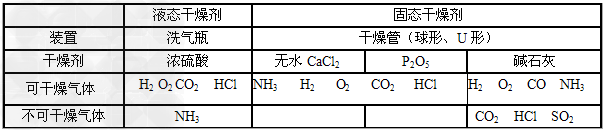
a.排水集气法:适用于收集不溶于水,不与水反应的气体。装置如下:如采用第二个装置,气体应短进长出。

b.向上排空气法:适用于收集密度比空气大不与空气反应的气体,装置如下:如采用第二个装置,气体应长进短出。

c.向下排空气法:适用于收集密度比空气小不与空气反应的气体。装置如下:如采用第二个装置,气体应短进长出。

气体净化:
装置:


气体干燥:
(1)干燥原则:
干燥剂只能吸收气体中含有的水分而不能与气体发生反应。
①酸性干燥剂不能干燥碱性气体。
②碱性干燥剂不能干燥酸性气体。
③具有强氧化性的干燥剂不能干燥具有强还原性的气体。注意H2、CO、SO2虽具有还原性,但可用浓H2SO4干燥。
(2)常见物质干燥

发现相似题
与“下列实验操作中不正确的是( )A.新制的氯水、浓氨水、浓硝...”考查相似的试题有:
- 实验室里不同化学试剂的保存方法不尽相同,①NaOH溶液 ②大理石 ③NaCl溶液 ④稀硝酸4种试剂通常各自存放在下列图示的某种试剂瓶...
- 氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为(MgCO3,舍少量FeCO3)...
- 下列括号中的分离方法运用得当的是A.植物油和自来水(蒸馏)B.水溶液中的食盐和碘(分液)C.SiO2和CaCl2(溶解、过滤、蒸...
- 在氯碱工业中,原料盐中的杂质离子危害很高,能破坏离子膜,以下对Ca2+、Mg2+、Fe3+、SO42-除去顺序不合理的是 ( )。A.B...
- 实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:①蒸馏;②水洗;③用干燥剂干燥;④用质量分数为10%的NaOH溶液润...
- 除去下列物质中所含的杂质,选用的试剂正确的是( )选项物质(杂质)试剂AAl2O3(SiO2)NaOHBCO2(SO2)Na2CO3溶液CFeCl2溶...
- 下列除去碳酸钠固体中少量碳酸氢钠的方法正确的是( )A.加入盐酸B.加入氢氧化钙C.加入氯化钡D.加热
- (12分)海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:请填写下列空白:(1) 步骤①灼烧海...
- 实验室用图的装置将CO2和CO进行分离和干燥,已知a、b均为活塞,试回答:(1)甲瓶中装的是______溶液,乙瓶中装的是______溶...
- (14分)某化学小组用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,其实验流程如下所示:(1)步骤①中氧化铜...