本试题 “某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S,设计了以下实验流程图(1)为了验证气体A,按下图所示进行实验:若能观察到__________________现...” 主要考查您对氯的其他化合物(高氯酸、氯化物、氯酸盐,盐酸等)
单质硫
其他物质的检验
设计实验方案及探究实验
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氯的其他化合物(高氯酸、氯化物、氯酸盐,盐酸等)
- 单质硫
- 其他物质的检验
- 设计实验方案及探究实验
常见的氯化物:
(1)高氯酸:高氯酸HClO4,无色透明的发烟液体,在无机酸中酸性最强。可助燃,具强腐蚀性、强刺激性,可致人体灼伤。与有机物、还原剂、易燃物如硫、磷等接触或混合时有引起燃烧爆炸的危险。在室温下分解,加热则爆炸。
(2)氯化物:如氯化钠、氯化钙等,Cl-+Ag+==AgCl↓
(3)次氯酸盐:次氯酸盐是次氯酸的盐,含有次氯酸根离子ClO-,其中氯的氧化态为+1。次氯酸盐常以溶液态存在,不稳定,会发生歧化反应生成氯酸盐和氯化物。见光分解为氯化物和氧气。次氯酸盐是一种常用的漂白剂和消毒剂。在人体组织中,在亚铁血红素的髓过氧化物酶的催化作用下,过氧化物与氯化物反应可产生ClO-或HClO。这种在血球内产生的ClO-/HClO或Cl2
(4)氯酸盐:如氯酸钾在二氧化锰催化下可制取氧气
(5)盐酸:盐酸是氯化氢的水溶液,是一种混合物。纯净的盐酸是无色的液体,有刺激性气味。工业品浓盐酸因含有杂质(Fe3+)带有黄色。浓盐酸具有挥发性,打开浓盐酸的瓶盖在瓶口立即产生白色酸雾。这是因为从浓盐酸中挥发出来的氯化氢气体跟空气中水蒸汽接触,形成盐酸小液滴分散在空气中形成酸雾。
(6)氯化氢:无色或微黄色易挥发性液体,有刺鼻的气味。易溶于水与氨气反应生成氯化铵HCl+NH3==NH4Cl
卤化氢和氢卤酸、卤化银及碘化物:
1.卤化氢物理性质:卤化氢均为无色有刺激性气味的气体,均极易溶于水,在空气中都易形成酸雾。化学性质:从HF—HCl—HBr—HI,稳定性逐渐减弱,HI受热易分解;还原性逐渐增强。
2.氢卤酸:Hx溶于水后形成的溶液即氢卤酸。在氢卤酸中,除氢氟酸是弱酸外,其余皆为强酸。从氢氟酸一氢碘酸,酸性逐渐增强,还原性也逐渐增强,其中氢碘酸在空气中易被氧气氧化。
3.卤化银:

4.碘化物碘是人体必需的微量元素之一,又称“智慧元素”。人体缺碘会导致碘缺乏病(IDD),从而损害人的智力和健康。补碘最经济、方便有效的方法是食用含碘食盐。含碘食盐中加的是碘酸钾。值得注意的是,人体摄入过多的碘也是有害的,不能认为高碘的食物吃得越多越好,要根据个人的身体情况而定。
卤素单质及其化合物的特殊性:
(1)Br2是常温下唯一呈液态的非金属单质,易挥发,蒸气有毒。保存液溴要采用水封法。
(2)碘单质易升华,AgI可用于人工降雨,碘盐可用于防治甲状腺肿大。
(3)HClO4是常见含氧酸中酸性最强的酸,HClO 是氯的含氧酸中氧化性最强的酸。
(4)在卤素中,氯、溴、碘均有多种价态,但氟只有-1价和0价,而无正价。
(5)卤素单质一般不与稀有气体反应,但F,却能与Xe、Kr等稀有气体反应生成相应的氟化物。如 KrF2、XeF2、:XeF4、XeF6等。
(6)Cl2、Br2、I2的实验室制法均可用MnO2与相应的浓的氢卤酸反应制得,但F2不能用上述方法在实验室制得。
(7)卤素单质与水反应,其中Cl2、Br2、I2在反应中既是氧化剂又是还原剂,而F2与水作用时,只作氧化剂。
(8)卤素单质都能与强碱溶液反应,一般可表示为 X2+2OH-==X-+XO-+H2O(F、I除外)。
(9)碘单质遇淀粉呈现特殊蓝色。可用来鉴别碘单质或淀粉。
(10)I2在水中的溶解度很小,若在水中加入少量的KI,碘的溶解度却明显增大,这是因为发生了反应I2 +I-==I3-
(11)卤素单质与Fe作用时,除Fe+I2==FeI2 外,其他均生成+3价铁盐。常温下,干燥的液氯不与 Fe作用,故工业上可用钢瓶盛液氯。
(12)随着相对分子质量的增大,HCl、HBr、HI的熔、沸点逐渐升高。HF的相对分子质量虽比HCl小,其熔、沸点却比HCl高,是因为HF分子间存在氢键。
(13)在氧卤酸中,只有氢氟酸能与玻璃反应:SiO2 +4HF==SiF4↑+2H2O,在实验室制取HF必须在铅皿中进行。
(14)实验室制取HF、HCl分别用CaF2、NaCl与浓硫酸反应,但实验室制取HBr、HI宜用NaBr和KI与浓磷酸反应。因为生成的HBr、HI易被浓硫酸氧化生成Br2或I2。
(15)在卤化银中,AgCl、AgBr、AgI均难溶于水,且见光易分解,但AgF却易溶于水且见光不分解。
硫:
硫是一种非金属元素,化学符号是S,原子序数是16。单质硫是一种非常常见的无臭无味的非金属,纯的硫是黄色的晶体,又称作硫磺。
分子结构:硫元素有多种同素异形体 (由同一种元素形成的性质不同的单质)。若将硫的分子式设为 Sx,则x=1,2,3,4,5,6,7,8,9,10,12,18。Sx的分子结构可用如图表示。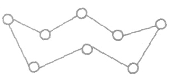
硫的物理性质和化学性质:
(1)物理性质:硫为黄色晶体,俗称硫黄,质脆,易研成粉末。硫的密度比水大,不溶于水,微溶于酒精,易溶于CS。
(2)化学性质:硫位于第3周期ⅥA族,最外层有6个电子,在反应中易得到2个电子而呈-2价;硫的最高正价为+6价;单质硫的化合价为0,处于中间价态,故单质硫既有氧化性又有还原性,在反应中既可作氧化剂又可作还原剂。
如;
①弱氧化性
在加热的条件下,硫黄能被H:和绝大多数的金属单质还原。南于硫的氧化性比较弱,与变价金属反应时往往生成低价态的金属硫化物。例如: 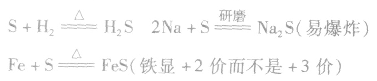

②弱还原性
在一定条件下,硫黄可被F2、O2、Cl2等非金属单质以及一些具有氧化性的化合物氧化,例如:

③硫黄在强碱溶液里加热可发生歧化反应。 (可用热碱液除去试管中残留的硫) 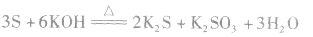
④特性:Hg、Ag在常温下不跟O2反应,但易跟S 反应。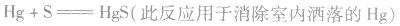
存在与用途:
存在:游离态的硫存在于火山喷口附近或地壳的岩层里,火山喷出物中含有大量含硫化合物,如H2S、 SO2、SO3等。化合态的硫主要以硫化物和硫酸盐的形式存在,如硫铁矿(FeS2)、石膏(CaSO4·2H2O)等。
用途:制H2SO4、黑火药、农药、医药和硫化橡胶。
1.有机物的检验
(1)在有机物检验时,需特别知道的物质性质:
①溶解性:有机物均能溶于有机溶剂,能溶于水的有机物为:低级醇、醛、酸。
②密度:比水小:烃、苯及同系物、酯、油脂;比水大:CCl4、溴苯、硝基苯。
③有毒:苯、硝基苯、甲醇、甲醛。
(2)常见有机物或官能团的检验

2.卤代烃中卤元素的检验:与氢氧化钠加热反应后取上层反应完全的清夜,再加入稀硝酸酸化的硝酸银溶液,观察沉淀颜色,白色的是氯离子,淡黄色的是溴离子,黄色的是碘离子
3.淀粉水解产物的检验:用稀硫酸作为催化剂,水解后先加NaOH来中和硫酸酸性,然后再分出一部分加足量碘酒,若变蓝,则仍含有淀粉,未完全水解;反之则已经完全水解;另一部分加土伦试剂或者菲林试剂,检验葡萄糖,若有银镜生成,或者有砖红色沉淀生成,则说明含有还原糖,水解已经发生,反之则没有发生水解。
化学实验方案的设计:
1.概念:化学实验方案的设计是在实施化学实验之前.根据化学实验的目的和要求,运用相关的化学知识和技能,对实验的仪器、装置和方法所进行的一种规划。
2.实验方案设计的基本要求
(1)科学性:实验原理、实验操作程序和方法必须科学合理。
(2)安全性:尽量避免使用有毒药品和进行有一定危险性的实验操作,保护人身安全,保护仪器。
(3)可行性:实验所选用的药品、仪器、设备和方法等在中学现有条件下能满足要求。
(4)简约性:方案简单易行,尽可能采用简单的实验装置,较少的实验步骤和药品。还应遵循完成实验所用时间较短,副反应少,效果好等基本要求。
(5)经济性:综合考虑原料的用量和价格。
3.化学实验设计的基本内容一个相对完整的化学实验方案一般包括下述内容:
(1)实验名称;
(2)实验目的;
(3)实验原理;
(4)实验用品(药品、仪器、装置、设备)及规格;
(5)实验装置图、实验步骤和操作方法;
(6)实验注意事项;
(7)实验现象的记录及结果处理;
(8)问题与讨论。
4.化学实验方案设计的基本思路 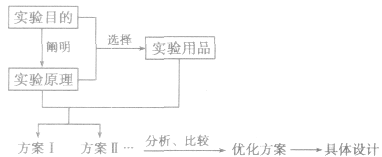
(1)明确目的、原理首先必须认真审题,明确实验的目的,弄清题目有哪些新的信息,结合已学过的知识,通过类比、迁移、分析,从而明确实验原理。
(2)选择仪器、药品根据实验的目的和原理,以及反应物和生成物的性质、反应条件(如反应物和生成物的状态、能否腐蚀仪器、反应是否需要加热及温度是否需要控制在一定的范围内等),合理选择化学仪器和药品。
(3)设汁装置、步骤根据实验目的和原理,以及所选用的仪器和药品,设计出合理的实验装置和实验操作步骤。学生应具备识别和绘制典型的实验仪器装置图的能力,实验步骤应既完整又简明。
(4)记录现象、数据根据观察,全面而准确地记录实验过程中的现象和数据。
(5)分析得出结论根据实验观察到的现象和记录的数据,通过分析、计算、图表、推理等,得出正确的结论。
化学实验方案设计的分类:
1.物质性质实验方案的设计研究物质性质的基本方法:观察法、实验法、分类法、比较法等。研究物质性质的基本程序:观察外观性质一预测物质性质一实验和观察一解释及结论。图示如下:
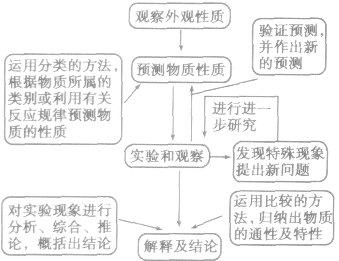
在进行性质实验方案的设计时,要充分了解物质的结构、性质、用途与制法之间的相互关系,要根据物质的结构特点,设计化学实验方案来探究或验证物质所具有的一些性质:
2.物质制备实验方案的设计
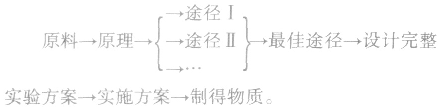
制备实验方案的设计,应遵循以下原则
(1)条件合适,操作简便;
(2)原理正确,步骤简单;
(3)原料丰富,价格低廉;
(4)产物纯净,污染物少。制备实验方案的设计,主要涉及原料、基本化学反应原理,实验程序和仪器、设备。核心是原料,由原料可确定反应原理,推导出实验步骤及所用仪器。
3.物质检验实验方案的设计

通过特定的反应现象,推断被检验物质是否存在。在对物质进行检验或鉴别时,一般的原则是:
①给出n 种物质进行鉴别,一般只需检验n一1种即可;
②物理和化学方法可并用,一般先用物理方法(如物质的颜色、气味、水溶性等),再用化学方法;
③设计的实验步骤越简单越好,实验现象越明显越好;
④有干扰离子存在时,应先排除干扰,以免得出错误的结论;
⑤进行检验的一般步骤为:观察外表一一加热固体(确定是否有结晶水)——配成溶液——观察外观一一加入试剂——观察现象——得出结论。
化学实验方案的评价:
对几个实验方案的正确与错误、严密与不严密、准确与不准确作出判断,要考虑是否合理、有无干扰现象、经济上是否合算和对环境有无污染等。
1.从可行性方面对实验方案作出评价科学性和可行性是设计实验方案的两条重要原则,在对实验方案进行评价时,要分析实验方案是否科学可行,实验方案是否遵循化学理论和实验方法的要求,在实际操作时能否做到可控易行。评价时,可从以下4个方面分析:
(1)实验原理是否正确、可行;
(2)实验操作是否安全、合理;
(3)实验步骤是否简单、方便;
(4)实验现象是否明显。
2.从“绿色化学”视角对实验方案作出评价 “绿色化学”要求设计安全的、对环境友好的合成线路,降低化学工业生产过程对人类健康和环境的危害,减少废弃物的产生和排放。据此,对化学实验过程或方案从以下4个方面进行综合评价:
(1)反应原料是否易得、安全、无毒;
(2)反应速率是否适巾;
(3)原料利用率以及合成物质的产率是否较高;
(4)合成过程中是否造成环境污染。
3.从安全性方面对实验方案作出评价从安全角度常考虑的主要因素如下:
(1)净化、吸收气体及熄灭酒精灯时要防止液体倒吸;
(2)使用某些易燃易爆品进行实验时要防爆炸(如 H2还原CuO应先通H2可燃性气体点燃前先验纯等);
(3)防氧化(如H2还原CuO后要“先灭灯再停氢”,白磷切割宜在水中进行等);
(4)防吸水(如实验取用、制取易吸水、潮解、水解的物质时宜采取必要措施,以保证达到实验目的);
(5)冷凝回流(有些反应中,为减少易挥发液体反应物的损耗和充分利用原料,需在反应装置上加装冷凝回流装置,如长玻璃管、竖装的干燥管及冷凝管等);
(6)易挥发液体产物(导出时可为蒸气)的及时冷却;
(7)仪器拆卸的科学性与安全性(可从防污染、防氧化、防倒吸、防爆炸、防泄漏等角度考虑);
(8)其他(如实验操作顺序、试剂加入顺序等)。
与“某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S,...”考查相似的试题有:
- 下列关于氯及其化合物叙述错误的是A.实验室选用二氧化锰和稀盐酸加热制取氯气,并用向上排空气法收集B.除去氯气中混有的氯...
- 常温度下,将Cl2缓慢通入水中至饱和,然后再滴加0.1mol/L的NaOH溶液,整个过程中溶液的pH变化曲线如图所示。下列选项正确的是A...
- 已知NH4CuSO3与足量的1mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判...
- 在下列物质中,在一定条件下能与某些酸、碱、金属、非金属都反应的是……( )(双选,请举例说明。)A.Al2O3B.H2SO3C.H2SD.N...
- 下图是各物质的反应关系图:已知A和E都是黄色粉末.F有刺激性气味且有漂白性常被不法商人用来漂白腐竹等.请据此回答下列问题:(1...
- 浓H2SO4可以用来干燥H2、O2等气体,是由于浓H2SO4具有 ( )A.吸水性B.氧化性C.酸性D.脱水性
- 新切开的苹果在空气中放置一段时间表面会变黄,最终变成褐色,这种现象在食品科学上通常称为“褐变”。 关于苹果褐变的原因有以...
- (12分)某化学研究性学习小组探讨Fe3+和SO32-之间发生怎样的反应,请你一起参与并协助他们完成实验。⑴提出猜想:甲同学认为发...
- 利用 Y 型管与其它仪器组合可以进行许多实验(固定装置略)。分析并回答下列问题:(1)实验目的:验证SO2有氧化性。将胶头滴...
- 菠菜营养丰富,素有“蔬菜之王”的美称。民间流传:菠菜豆腐同食,易得结石。某化学兴趣小组对“菠菜豆腐是否能同食”等阃题进行...