本试题 “有媒体经常报道一些具有独特性质的化学物质,如:改变世界的新材料一石墨烯、爆炸力极强的N5、比黄金还贵的O-18气体、太空中的甲醇气团等.有关这些物质的下...” 主要考查您对氧化还原反应的本质和特征
氧化还原反应的定义
极性分子、非极性分子
同位素
合成有机高分子化合物
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化还原反应的本质和特征
- 氧化还原反应的定义
- 极性分子、非极性分子
- 同位素
- 合成有机高分子化合物
电子的转移(得失或偏移)
氧化还原反应的特征:
化合价升降(某些元素化合价在反应前后发生变化,是氧化还原反应判别的依据)
氧化还原反应的发展史:
- 物质与氧气发生的反应属于氧化反应,含氧化合物中氧被夺去的反应属于还原反应。
- 有化合价升降的反应属于氧化还原反应。
- 有电子得失或偏移的反应属于氧化还原反应。
对物质的认识存在发展的过程,从最初的隔离开的氧化反应、还原反应,到从表面上看化合价变化的氧化还原反应,把氧化与还原统一在一个概念下,再透过现象看本质,化合价的变化是有电子得失或偏移引起的。
氧化还原反应中应注意的几个问题:
1、氧化剂氧化性的强弱,不是看得电子的多少,而是看得电子的难易;
还原剂还原性的强弱,不是看失电子的多少,而是看失电子的难易。
eg:氧化性:浓HNO3>稀HNO3还原性:Na>Al
2、有新单质参加或生成的反应不一定是氧化还原反应 eg:C(金刚石)==C(石墨);3O2==2O3(放电);P4(白磷)==4P(红磷)
3、任何元素在化学反应中,从游离态变为化合态,或由化合态变为游离态,均发生氧化还原反应(比如置换反应,化合反应,分解反应)
4、置换反应一定是氧化还原反应,复分解反应一定不是氧化还原反应;有单质参加的化合反应和有单质生成的分解反应全部属于氧化还原反应。
5、元素具有最高价的化合物不一定具有强氧化性! eg.H3PO4、H2SiO3(或H4SiO4)两酸均无强氧化性但硝酸有强氧化性。
氧化还原的表示可用单线桥也可用双线桥:
一、双线桥法:
此法不仅能表示出电子转移的方向和总数,还能表示出元素化合价升降和氧化、还原关系。双线桥的箭头始于反应物有关元素的原子或离子,箭头指向发生化合价变化后生成物中对应元素的原子或离子或原子团。
标变价 明确标出所有发生氧化还原反应的元素的化合价,不变价的元素不标化合价。
连双线 将标化合价的同一元素用直线加箭头从反应物指向生成物(注意:箭头的起止一律对准各元素)
标得失 1.标电子转移或偏离数 明确标出得失电子数,格式为“得/失发生氧化还原反应原子个数×单位原子得失电子数”
2.标化合价变化 一律标出化合价的变化,只有“化合价升高”“化合价降低”这两种写法,不可写为“升价”“降价”等
3.标出元素反应类型 一律标出元素所发生的反应,“被氧化”或“被还原”,其余写法均不正确
4.检查得失电子守恒 检查得失电子数是否相等,如不相等则重新分析。
例如: 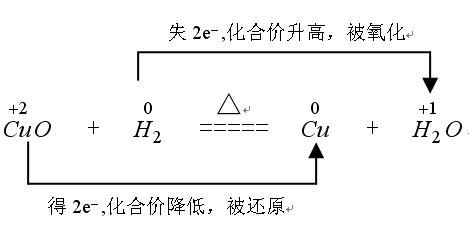
二、单线桥法:
在氧化还原反应中,有电子发生转移(得失或偏移),也就是在反应物中有元素电子发生得失或偏移,这时用一条带箭头的曲线从失去电子的元素指向得到电子的元素,并在“桥”上标出转移的电子数,这种表示方法叫单线桥法。
(1)标价态明确标明发生氧化还原反应的元素的化合价
(2)连单线连接方程式左边的氧化剂与还原剂,箭头一律指向氧化剂
(3)不注得失标出转移的电子的总数,这里不用像双线桥那样,仅需直接标出电子总数
例如: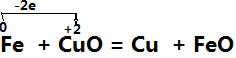
注意事项:
(1)不得标明"得"或"失",否则是错的
(2)箭头表示电子转移的方向,指向氧化剂注意:为了规范起见,单线桥法最好不用于自身氧化还原的反应,因为那样标记会使反应中的电子去向不明确,故在自身氧化还原的反应方程式中最好用双线桥法表示电子转移。
氧化还原反应:
有电子转移(得失或偏移)的反应;(无电子转移(得失或偏移)的反应为非氧化还原反应)
反应历程:
氧化还原反应前后,元素的氧化数发生变化。根据氧化数的升高或降低,可以将氧化还原反应拆分成两个半反应:氧化数升高的半反应,称为氧化反应;氧化数降低的反应,称为还原反应。氧化反应与还原反应是相互依存的,不能独立存在,它们共同组成氧化还原反应。
氧化还原反应中存在以下一般规律:
强弱律:氧化性:氧化剂>氧化产物;
还原性:还原剂>还原产物。
价态律:元素处于最高价态,只具有氧化性;元素处于最低价态,只具有还原性;处于中间价态,既具氧化性,又具有还原性。
转化律:同种元素不同价态间发生归中反应时,元素的氧化数只接近而不交叉,最多达到同种价态。
优先律:对于同一氧化剂,当存在多种还原剂时,通常先和还原性最强的还原剂反应。守恒律:氧化剂得到电子的数目等于还原剂失去电子的数目。
氧化还原性的强弱判定:
物质的氧化性是指物质得电子的能力,还原性是指物质失电子的能力。物质氧化性、还原性的强弱取决于物质得失电子的能力(与得失电子的数量无关)。从方程式与元素性质的角度,氧化性与还原性的有无与强弱可用以下几点判定:
(1)从元素所处的价态考虑,可初步分析物质所具备的性质(无法分析其强弱)。最高价态——只有氧化性,如H2SO4、KMnO4中的S、Mn元素;最低价态,只有还原性,如Cl-、S2-等;中间价态——既有氧化性又有还原性,如Fe、S、SO2等。
(2)根据氧化还原的方向判断:氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。
(3)根据反应条件判断:当不同的氧化剂与同一种还原剂反应时,如氧化产物中元素的价态相同,可根据反应条件的高、低进行判断,如是否需要加热,是否需要酸性条件,浓度大小等等。
电子的得失过程:

其过程用核外电子排布变化情况可表示为:
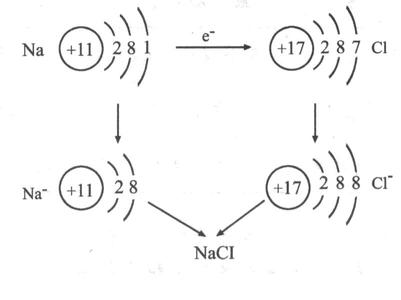
(1)极性分子:正电荷中心和负电荷中心不相重合的分子
(2)非极性分子:正电荷中心和负电荷中心相重合的分子
(3)分子极性的判断:分子的极性由共价键的极性及分子的空间构型两个方面共同决定
非极性分子和极性分子的比较:
| 非极性分子 | 极性分子 | |
| 形成原因 | 整个分子的电荷分布均匀,对称 | 整个分子的电荷分布不均匀、不对称 |
| 存在的共价键 | 非极性键或极性键 | 极性键 |
| 分子内原子排列 | 对称 | 不对称 |

分子极性的判断方法:
An型分子(以非极性键结合形成的单质分子)一般是非极性分子(O3例外),AB型分子一定是极性分子。对于ABn型分子是极性分子还是非极性分子,通常有以下判断方法。
1.根据分子的立体构型判断
判断ABn型分子是否有极性,关键是看分子的立体构型.如果分子的立体构型为直线形、平面三角形、正四面体形、三角双锥形、正八面体形等空间对称的结构,致使正电中心与负电中心重合,这样的分子就是非极性分子。若为V形、三角锥形、四面体形(非正四面体形)等非对称结构,则为极性分子。比如H2O分子中虽然2个H原子轴对称,但整个分子的空间构型是不对称的: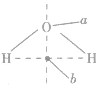 ,负电中心在a点,正电中心在b 点,二者不重合,因此是极性分子。
,负电中心在a点,正电中心在b 点,二者不重合,因此是极性分子。
2.根据实验现象判断
将液体放入适宜的滴定管中,打开活塞让其缓慢流下,将用毛皮摩擦过的橡胶棒靠近液流,流动方向变化(发生偏移)的是极性分子.流动方向不变的是非极性分子。
3.根据中心原子最外层电子是否全部成键判断
ABn型分子中的中心原子A的最外层电子若全部成键(没有孤电子对),此分子一般为非极性分子,如CO2、CCl4等;分子中的中心原子最外层电子若未全部成键(有孤电子对),此分子一般为极性分子,如H2O、 PCl3等。
4.判断ABn型分子极性的经验规律
若中心原子A的化合价的绝对值等于该元素所在的主族序数,则为非极性分子;若不等,则为极性分子。如BF3、CO2、CH4、SO3等分子中,B、C、S等元素的化合价的绝对值等于其主族序数,是非极性分子;H2O、 NH3、SO2、PCl3等分子中,O、N、S、P等元素的化合价的绝对值不等于其主族序数,是极性分子。
定义:
质子数相同而中子数不同的原子互称为同位素(即同一元素的不同核素互称为同位素)。元素符号表示不同,如 ;电子结构相同,原子核结构不同;物理性质不同,化学性质相同。
;电子结构相同,原子核结构不同;物理性质不同,化学性质相同。
同位素的应用:
(1)同位素在医学领域中的应用最为广泛,主要用于显像、诊断和治疗,还用于医疗用品消毒、药物作用机理研究和生理医学研究等。
(2)同位素辐射育种技术为农业提供了改进农产品质量、增加产量的新技术;利用同位素示踪技术,可检测并确定植物的最佳肥料吸入量和农药吸入量。
(3)14C纪年测定法与其他放射性同位素测定法已成为地质学、考古学、人类学、地球科学等领域广泛采用的一种准确的断代方法。
合成有机高分子化合物:
由千百个原子彼此以共价键结合形成相对分子质量特别大、具有重复结构单元的有机化合物。是由一类相对分子质量很高的分子聚集而成的化合物,也称为高分子、大分子等。一般把相对分子质量高于10000的分子称为高分子。包括天然和合成有机高分子化合物。常见合成有机高分子化合物:聚乙烯、聚氯乙烯等
有机高分子化合物的合成:
高分子化合物大部分是由小分子通过聚合反应制得的。
(1)加聚反应:不饱和单体通过加聚反应生成高分子化合物。
①聚乙烯类(塑料、纤维)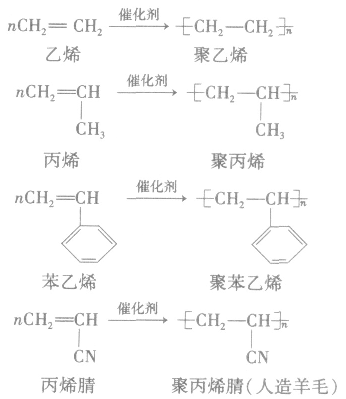
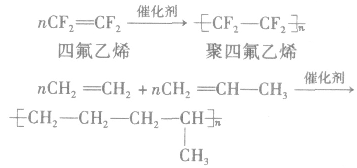
②聚二烯类(橡胶)
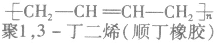
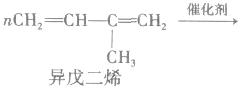
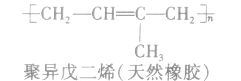
(2)缩聚反应:单体聚合成高分子的同时有小分子生成的聚合反应。
①聚酯类 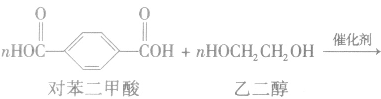
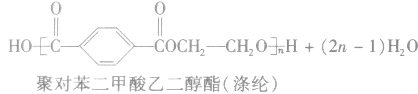
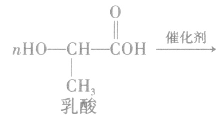
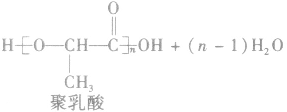
②聚氨基酯类
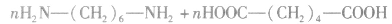
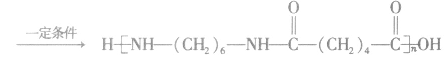
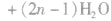

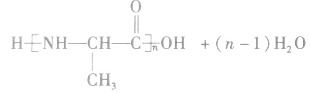
③酚醛树脂类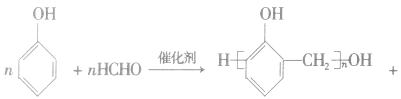
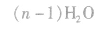
对高分子化合物的理解:
(1)通常把生成高分子化合物的低分子化合物(反应物)叫做单体(如乙烯是聚乙烯的单体),高分子化合物中化学组成相同、可重复的最小单位叫做链节(如一CH2一CH2一是聚乙烯的链节),高分子链中含有链节的数目叫做聚合度,通常用n表示。注意单体与链节是不同的,单体是反应前的低分子化合物;链节不是物质,不能独立存在,是反应后有机高分子化合物中的片段。 (2)低分子有机物的相对分子质量都有一个确定的数值,而高分子化合物的相对分子质量只是一个平均值。它是以低分子有机物作原料,经聚合反应得到各种相对分子质量不等的物质的混合物。
单体与高分子化合物的互推规律:
聚合时找准结合点,反推单体时找准分离处,“结合点必为分离处”。
1.由单体推断高聚物的方法
(1)单烯烃型单体加聚时,“断开双键,键分两端,添上括号,n写后面”。如

(2)二烯烃型单体加聚时,“单变双,双变单,破两头,移中间,添上括号.n写后面”。如
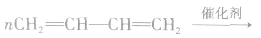
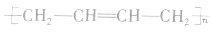
(3)分别含有一个双键的两种单体聚合时,“双键打开,中间相连,添上括号,n写后面”。如 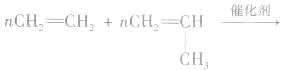
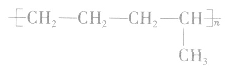
2.由高聚物推导单体的方法
(1)加聚产物单体的判断方法
①凡链节主链只有两个碳原子(无其他原子)的聚合物,其合成单体必为一种,将两个半键闭合即可。如
②凡链节主链有四个碳原子(无其他原子),且链节无双键的聚合物,其单体必为两种,在中央画线断开,然后两键闭合即可。如
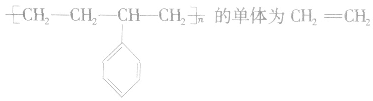
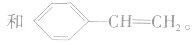
③凡链节主链上只有碳原子,斤存在碳碳双键结构的高聚物,其规律是“凡双键,四个碳;无双键,两个碳”画线断开。如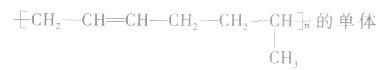
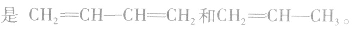
(2)缩聚产物单体的判断方法
①酯类高聚物中含有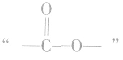 ,它的单体有两种,从
,它的单体有两种,从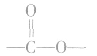 中间断开,
中间断开,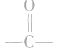 恢复为
恢复为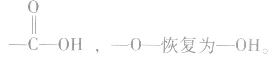
如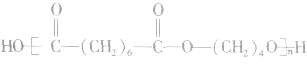 的单体为
的单体为
②酰胺类高聚物中含有"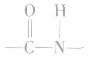 ",它的单体有两种,在亚氨基氮原子上加氢,羰基碳原子上加羟基,即得高聚物的单体。如
",它的单体有两种,在亚氨基氮原子上加氢,羰基碳原子上加羟基,即得高聚物的单体。如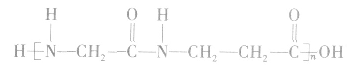 的单体为
的单体为
结构为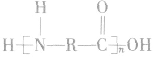 的高聚物,其合成单体必为一种,在亚氨基氮原子上加氢,在羰基碳原子上加羟基即得高聚物的单体。 如
的高聚物,其合成单体必为一种,在亚氨基氮原子上加氢,在羰基碳原子上加羟基即得高聚物的单体。 如 的单体为
的单体为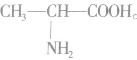
③酚醛树脂是由苯酚和甲醛缩聚而成的,链节中有酚羟基的结构。
如 和
和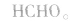
与“有媒体经常报道一些具有独特性质的化学物质,如:改变世界的...”考查相似的试题有:
- 下列反应都有沉淀生成,其中属于氧化还原反应的是( )A.Na2SO4+BaCl2═2NaCl+BaSO4↓B.4Fe(OH)2+O2+2H2O═4Fe(OH)3↓C.Fe...
- 下列反应中铁元素发生氧化反应的是A.FeS+2HCl=FeCl2+H2S↑B.Fe+H2SO4=FeSO4+ H2↑C.Fe2O3+3CO2Fe+3CO2D.2FeCl3+Cu=2FeCl2+C...
- 已知只有浓盐酸与MnO2在加热的条件下才能反应产生C12,稀盐酸与MnO2不反应.请问在课堂上做演示实验时,用下列两种方法制取C1...
- 在反应:3BrF3+5H2O=HBrO3+Br2+9HF十O2中(F为-1价)(1)此反应中被氧化的元素是______、被还原的元素是______.(2)当有5m...
- 三聚氰酸[C3N3(OH)3]可用于消除汽车尾气中的NO2.其反应原理为:C3N3(OH)3 △ . 3HNCO;8HNCO+6NO2 △ . 7N2+8CO2+4H2O下列...
- 下列物质在空气中久置变质,在变质过程中,既有氧化还原反应发生,又有非氧化还原反应发生的是( )A.食盐B.漂白粉C.氯水D...
- 下列变化中,一定需加还原剂才能实现的是( )A.FeCl3→FeCl2B.CO2→CO32-C.C→CO2D.KMnO4→MnO2
- 中新网沈阳4月18日,沈阳市公安局查获掺入非食品添加剂的毒豆芽二十余吨.经检测,毒豆芽中含有亚硝酸钠(NaNO2)等有害物质...
- (多选题)2005年中国考古重大新发现是13C、15N分析考古方法.13C、15N分析法作为以往研究方法的补充,通过对遗留在古人骨骼...
- 下列有机物用于合成聚乙烯塑料,是聚乙烯的单体的是A.CH4B.CH2=CH2C.CH3CH2OHD.CH2=CHCH3