本试题 “下列有关说法不正确的是[ ]A.水合铜离子的模型如图(1)所示,1个水合铜离子中有4个配位键B.CaF2晶体的晶胞如图(2)所示,每个CaF2晶胞平均占有4个Ca2+C. H原...” 主要考查您对电子云和原子轨道
配合物理论
晶胞
金属晶体
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电子云和原子轨道
- 配合物理论
- 晶胞
- 金属晶体
核外电子运动状态:
核外电子的运动特征核外电子的质量很小,运动空间小,但运动速度却很大,接近光速。
由于电子的绕核运转是高速的、无规律的,因此我们无法预测电子在某一时刻的位置,只能预测电子在某一区域内出现几率的大小。
现代量子力学指出,核外电子的运动不能像经典力学中确定宏观物体的运动状态那样,同时用位置和速度的物理量来准确描述它的运动状态,而只能确定它在原子核外各处出现的概率。
电子云:
由于核外电子的概率密度分布看起来像一片云雾,因而被形象地称作电子云。换句话说,电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述。
电子云密度大的地方,表明电子在核外空间单位体积内出现的机会多;电子云密度小的地方,表明电子在核外空间单位体积内出现的机会少。
原子轨道:
(1)定义:量子力学把电子在原子核外的一个空间运动状态称为一个原子轨道。
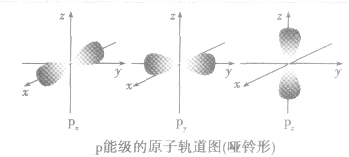
(2)原子轨道的形状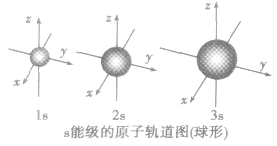
配位键、配合物:
1.配位键配位键是一种特殊的共价键。成键的两个原子间的共用电子对是由一个原子单独提供的。形成配位键的条件是其中一个原子有孤电子对,另一个原子有接受孤电子对的“空轨道”。配位键用A→B表示,A是提供孤电子对的原子,B是接受孤电子对的原子。
2.配合物通常把金属离子(或原子)与某些分子或离子(称为配体)以配位键结合形成的化合物称为配合物。
3.配位键的形成
(1) 中配位键的形成
中配位键的形成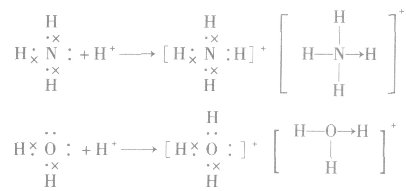
注意:结构式中“→”表示配位键及其共用电子对的提供方式。
(2)配离子 中配位键的形成
中配位键的形成
在 里,NH3分子中的氮原子给出孤电子对,
里,NH3分子中的氮原子给出孤电子对,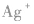 接受电子对,以配位键形成了
接受电子对,以配位键形成了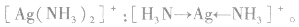
(3)配离子 的形成
的形成
在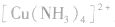 里,
里, 分子中的氮原子给出孤电子对,
分子中的氮原子给出孤电子对, 接受电子对,以配位键形成了
接受电子对,以配位键形成了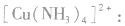
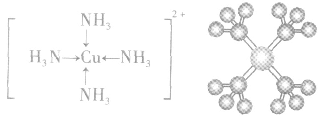
4.配合物的组成
配合物的组成包含中心原子、配体和配位原子、配位数,内界和外界等。以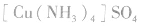 为例说明,如下图所示:
为例说明,如下图所示: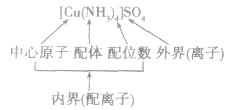
配合物的内界和外界之间多以离子键结合,因而属于离子化合物、强电解质,能完全电离成内界离子和外界离子,内界离子也能电离但程度非常小,可谓“强中有弱”。例如,配合物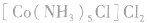 溶液中加入
溶液中加入 溶液,外界的
溶液,外界的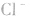 能被沉淀,而内界的
能被沉淀,而内界的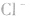 不能形成沉淀。
不能形成沉淀。
晶胞:
1.定义描述晶体结构的基本单元叫做晶胞。
2.结构一般来说,晶胞为平行六面体,晶胞只是晶体微观空间里的一个基本单元,在它的上、下、左、右、前、后无隙并置地排列着无数晶胞,而且所有晶胞的形状及其内部的原子种类、个数及几何排列是完全相同的。“无隙”是指相邻晶胞之间没有任何间隙,“并置”是指所有晶胞都是平行排列的,取向相同。
晶胞中微粒数目的确定:
计算晶胞中微粒数目的常用方法是均摊法。均摊法是指每个晶胞平均拥有的粒子数目。如某个粒子为n个晶胞所共有,则该粒子有 属于这个晶胞。
属于这个晶胞。
(1)长方体(或正方体)形晶胞中不同位置的粒子数的计算。
①处于顶点的粒子,同时为8个晶胞所共有,每个粒子有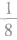 属于该晶胞。
属于该晶胞。
②处于棱上的粒子,同时为4个晶胞所共有,每个粒子有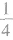 属于该晶胞。
属于该晶胞。
③处于面上的粒子,同时为2个晶胞所共有。每个粒子有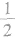 属于该晶胞。
属于该晶胞。
④处于晶胞内部的粒子,则完全属于该晶胞。
(2)非平行六面体形晶胞中粒子数目的计算同样可用均摊法,其关键仍然是确定一个粒子为几个晶胞所共有。例如,石墨晶胞每一层内碳原子排成许多个六边形,其顶点(1个碳原子)对六边形的贡献为 ,那么每一个六边形实际有6×
,那么每一个六边形实际有6× =2个碳原子。
=2个碳原子。
(3)在六棱柱晶胞(如图所示 MgB2的晶胞)中,顶点上的原子为6 个晶胞(同层3个,上层或下层3个) 共有,面上的原子为2个晶胞共有,因此镁原子个数为12×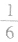 +2×
+2×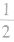 =3,硼原子个数为6。
=3,硼原子个数为6。 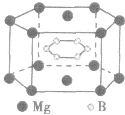
特别提醒:在晶胞中微粒个数的计算过程中,不要形成思维定式,不同形状的晶胞应先分析任意位置上的一个粒子被几个晶胞共用,如六棱柱晶胞中,顶点、侧棱、底面上的棱、面心上的原子依次被6、3、4、2 个晶胞共用。
有关晶胞密度的计算步骤:
①根据“分摊法”算出每个晶胞实际含有各类原子的个数,计算出晶胞的质量m:
②根据边长计算晶胞的体积V:
③根据 进行计算,得出结果。
进行计算,得出结果。
通过金属离子与自由电子间的较强作用(金属键)形成的单质晶体,熔沸点(除Hg外)高,导热性、延展性良好,易导电,硬度一般较大。
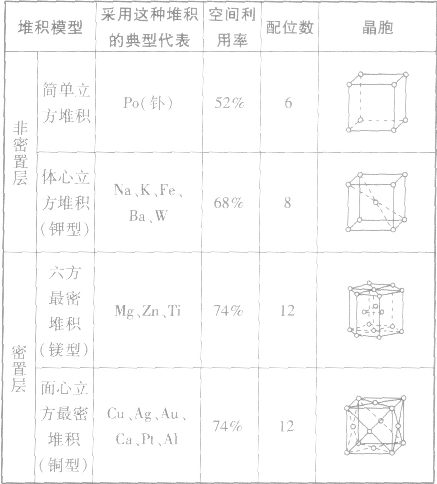
如:金属单质金属晶体原子堆积模型:
(1)简单立方堆积 (2)体心立方堆积 (3)六方最密堆积和面心立方最密堆积
晶体的基本类型与性质:
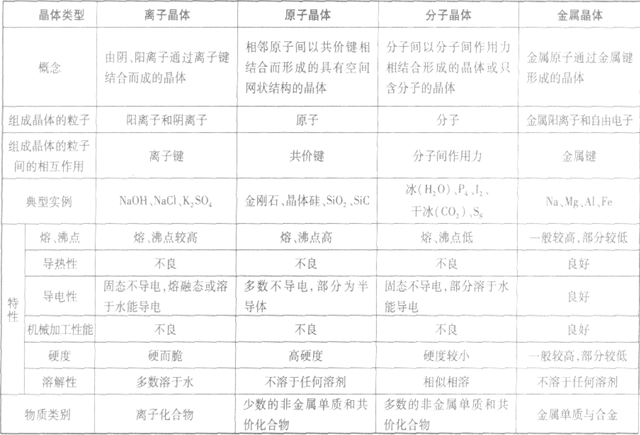
金属晶体的原子堆积模型:
与“下列有关说法不正确的是[ ]A.水合铜离子的模型如图(1)所示,...”考查相似的试题有:
- 设阿伏加德罗常数的值为NA,下列说法正确的是A.18g冰晶体中含有的氢键数为4NAB.30g SiO2晶体中含Si–O键数为NAC.78g Na2O2...
- 某离子晶体的晶胞结构如下图所示:则该离子晶体的化学式为A.abcB.abc3C.ab2c3D.ab3c
- 下列说法正确的是( )A.熔点:金刚石>晶体硅>干冰>氯化钠晶体B.由于HCl的分子间作用力大于HI,故HCl比HI稳定C.等质量的金...
- 钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题...
- 干冰晶体是一种立方面心结构,即每8个CO2构成立方体,且在6个面的中心又各被一个CO2分子占据,在每个CO2周围最近且等距离的CO...
- 下列叙述正确的是A.正四面体构型的分子中键与键之间的夹角均是109°28′B.粒子间以分子间作用力结合而成的晶体其熔点一般不会...
- 碘的熔、沸点较低,其原因是 ( )A.碘的非金属性较弱B.I2中I-I键不稳定C.碘晶体属于分子晶体D.碘的氧化性较弱
- 下列物质中熔点最高的是A.干冰B.氯化钠C.金刚石D.汞
- 分析下列各物质的物理性质,可判断其固态不属于分子晶体的是( )A.碳化铝,黄色晶体,熔点2200℃,熔融态不导电B.溴化铝,无...
- X、Y、Z、U为原子序数依次增大的前四周期元素,X、Y、Z三种元素位于同一周期,其中基态Y原子的2p轨道处于半充满状态,Y和Z的...