本试题 “用蒸汽密度法测定物质的相对分子质量是一种常用的方法。现测得0.2g某挥发性液体化合物样品在挥发时排出的空气在标准状况下是40mL,则该化合物的相对分子质量...” 主要考查您对质量守恒定律
化学单位(摩尔)
物质的量
阿伏加德罗定律
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 质量守恒定律
- 化学单位(摩尔)
- 物质的量
- 阿伏加德罗定律
质量守恒定律:
参加化学反应的各物质质量总和等于反应后生成的各物质质量总和。
化学反应前后,各种原子种类、数目、质量都不改变。
任何变化包括化学反应和核反应都不能消除物质,只是改变了物质的原有形态或结构,所以该定律又称物质不灭定律。
质量守恒定律的本质:
原子是物质质量的最小承担者。故在化学反应中,只要各种原子总数保持不变,则总质量保持不变。所以,质量守恒定律也就等价于元素守恒。
质量守恒定律的适用范围:
①质量守恒定律适用的范围是化学变化而不是物理变化;
②质量守恒定律揭示的是质量守恒而不是其他方面的守恒。物体体积不一定守恒;
③质量守恒定律中“参加反应的”不是各物质质量的简单相加,而是指真正参与了反应的那一部分质量,反应物中可能有一部分没有参与反应;
④质量守恒定律的推论:化学反应中,反应前各物质的总质量等于反应后各物质的总质量
质量守恒定律的应用:
(1)根据质量守恒定律,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。利用这一定律可以解释反应前后物质的质量变化及用质量差确定某反应物或生成物的质量。
(2)根据质量守恒定律,化学反应前后元素的种类和质量不变,由此可以推断反应物或生成物的组成元素。
(3)据质量守恒定律:化学反应前后元素的种类和数目相等,推断反应物或生成物的化学式。
(4)已知某反应物或生成物质量,根据化学方程式中各物质的质量比,可求出生成物或反应物的质量。
摩尔:
物质的量的单位为摩尔,简称摩,符号mol 。1mol粒子集体所含有的粒子数与0.012Kg12C中所含有的碳原子数相同,约为6.02×1023。
摩尔描述的对象:
摩尔只能用来描述微观粒子,其度量的对象是原子、分子、离子、质子、中子、电子或它们的特定组合。对于宏观可见的物质是不能用摩尔来描述的。比如,1mol大米是错误的。
摩尔的使用方法:
在使用摩尔作单位时,必须指明微粒的名称、符号或化学式,而不能用元素名称,如1molH2、0.5molH+,但不能说1mol氢。
物质中含有一定数目粒子集体的物理量。是国际单位制中7个基本物理量之一(7个基本的物理量分别为:长度、质量、时间、电流强度、发光强度、温度、物质的量)符号:n
计算公式:物质的量(n)=粒子数(N)/阿伏加德罗常数(NA) 以物质的量为中心的各种化学常用量间的关系:n=N/NA=m/M=V/Vm=cV=ρV/M
使用物质的量注意事项:
(1)物质的量表示物质所含指定粒子的多少,物质的量是一个整体,不得简化或增添任何字。
(2)物质的量及其单位摩尔的适用范围是微观粒子,因此在使用中应指明粒子的名称。
物质的量的相关解法:
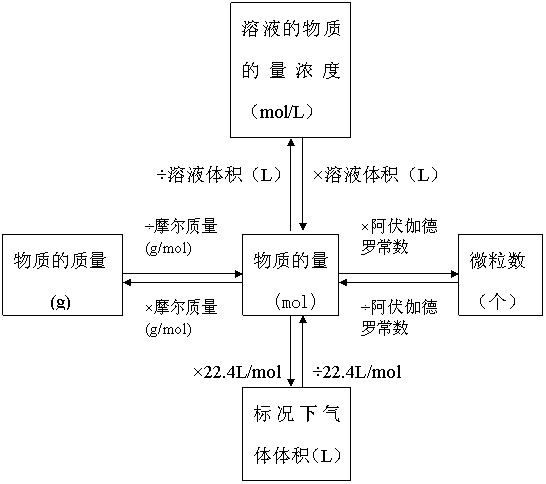
问题探究:
(1)1mol氢这种说法正确吗?如何表示1mol氢原子、1mol氢分子、1mol氢离子?
答:使用摩尔作单位时,应用化学式(符号)指明离子的种类,1mol氢的说法不正确,因其咩有指明是氢分子还是氢离子、氢原子。1mol氢原子、1mol氢分子、1mol氢离子分别表示为1molH、1molH2、1molH+。
(2)阿佛加德罗常数和6.02×1023mol-1在实际使用上有何区别?
阿佛加德罗常数是一个非常精确的数字,而6.02×1023mol-1只是阿佛加德罗常数的一个近似值。在关于概念性描述时要求非常准确,要使用阿佛加德罗常数,而在涉及计算时,则用6.02×1023mol-1进行粗略计算。二者关系类似于数学上的圆周率∏与3.14的关系。
阿伏伽德罗定律:
同温同压下,相同体积的任何气体含有相同的分子数。
阿伏伽德罗定律的使用范围:
阿伏伽德罗定律只对气体起作用,使用于任何气体,包括混合气体。
方法与技巧:
- “三同”定“一同”(温度、压强、气体体积、气体分子数);“两同”定“比例”。
- 阿伏伽德罗定律及其推论的数学表达式可由理想气体状态方程(PV=nRT)或其变形形式(PM=ρRT)推出,不用死记硬背。
理想气体状态方程:
理想气体状态方程的表达式:PV= nRT
P表示压强,V 表示体积,T表示温度,R是常数,n是气体的物质的量。
可根据此方程来推断阿伏伽德罗定律的相关推论:
| 条件 | 结论 | 语言表达 |
| T、P相同 | n1/n2=V1/V2 | 同温同压下,气体的分子数与其体积成正比 |
| T、V相同 | n1/n2=P1/P2 | 同温同体积,压强与其分子数成正比 |
| n、P相同 | V1/V2=T1/T2 | 分子数、压强相同的气体,体积与温度成正比 |
| n、T相同 | P1/P2= V2/V1 | 分子数、温度相同的气体,压强与体积成反比 |
| T、P相同 | ρ1/ρ2=M1/M2 | 同温同压下,气体的密度与相对分子质量(摩尔质量)成正比 |
| T、P、V相同 | m1/m2=M1/M2 | 同温同压下,相同体积的气体,质量与其相对分子质量成正比 |
| T、P、m相同 | M1/M2=V2/V1 | 同温同压下,等质量的气体,相对分子质量与其体积成反比 |
与“用蒸汽密度法测定物质的相对分子质量是一种常用的方法。现测...”考查相似的试题有:
- 下列说法正确的是A.液溴易挥发,在存放液溴的试剂瓶中应加水封B.能使湿润的淀粉KI试纸变成蓝色的物质一定是Cl2C.某溶液加...
- 下列说法正确的是[ ]A.化学反应既遵守“质量守恒”定律,也遵守“能量守恒”定律B.HF、HCl、HBr、HI的的稳定性依次增强C.丁烷...
- 2014年全运会在辽宁举办,其开幕式就是一场焰火盛宴。(1)焰火利用了部分金属元素特征的 反应,该反应属于 (填“物理”或“化学”)...
- 现有100克碳酸锂和碳酸钡的混和物,它们和一定浓度的盐酸反应时所消耗盐酸跟100克碳酸钙和该浓度盐酸反应时消耗盐酸量相同。...
- 如图是某学校实验室从化学试剂商品店买回的硫酸试剂标签上的部分内容,据此,下列说法正确的是( )A.该硫酸的物质的量浓度为9.2...
- “84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶某品牌“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:“84消...
- 中草药秦皮中含有的七叶树内酯结构是:,(C、H原子未画出,每个折点表示一个C原子)具有抗菌作用,若1 mol 七叶树内酯分别与...
- 下列反应是氧化还原反应的是A.CaCO3+2HCl===CaCl2+H2O+CO2↑B.CaO+H2O===Ca(OH)2C.2KMnO4K2MnO4+MnO2+O2↑D.CaCO3CaO...
- 下列反应属于化合反应的是 A.2Mg+O22MgOB.2Al+Fe2O3A12O3+2FeC.CaCO3CaO+CO2↑D.KCl + Ag NO3="=" KNO3+AgCl↓
- NA代表阿伏加德罗常数。下列有关叙述正确的是( )A.标准状况下,2.24LH2O含有的分子数等于0.1NAB.常温下,溶液中阴离子总...