本试题 “固体乙醇晶体中不存在的作用力是[ ]A.离子键B.极性键C.非极性键D.范德华力” 主要考查您对极性键、非极性键
离子键
范德华力
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 极性键、非极性键
- 离子键
- 范德华力
极性键和非极性键:
(1)非极性键:同种元素的原子间形成的共价键(共用电子对不偏移,成键原子双方不显电性)。
如:在非金属单质(H2 Cl2 O2)、共价化合物(H2O2 多碳化合物)、离子化合物(Na2O2 CaC2)中存在。
(2)极性键:不同元素的原子间形成的共价键(共用电子对偏向吸引电子能了强的一方,该元素显负价,偏离吸引电子能力弱的一方,该元素显正价)。如:在共价化合物(HCl H2O CO2 NH3)、某些离子化合物(NaOH Na2SO4 NH4Cl)中存在。
(1)非极性键:同种元素的原子间形成的共价键(共用电子对不偏移,成键原子双方不显电性)。
如:在非金属单质(H2 Cl2 O2)、共价化合物(H2O2 多碳化合物)、离子化合物(Na2O2 CaC2)中存在。
(2)极性键:不同元素的原子间形成的共价键(共用电子对偏向吸引电子能了强的一方,该元素显负价,偏离吸引电子能力弱的一方,该元素显正价)。如:在共价化合物(HCl H2O CO2 NH3)、某些离子化合物(NaOH Na2SO4 NH4Cl)中存在。
分子空间构型、键的极性与分子的极性:

化学键与物质类别:
1.只含有极性共价键的物质:一般是不同非金属元素构成的共价化合物。例如: 等。
等。
2.只含非极性共价键的物质:同种非金属元素构成的单质。例如: 、金刚石等。
、金刚石等。
3.既有极性键又有非极性键的物质。例如: 等。
等。
4.只含有离子键的物质:活泼非金属元素与活泼金属元素形成的化合物。例如: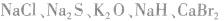 等。
等。
5.既有离子键又有非极性键的物质。例如: 等。
等。
6.既有离子键又有极性键的物质。例如: 等。
等。
7.由离子键、共价键、配位键构成的物质。例如: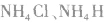 等。
等。
8.只含有共价键而无范德华力的物质。例如:金刚石、晶体硅、 等原子晶体。
等原子晶体。
9.由强极性键构成但又不是强电解质的物质。例如:HF。
10.没有化学键的物质。例如:稀有气体(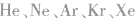 等)。
等)。
定义:
使阴阳离子结合成化合物的静电作用叫离子键。
成键元素:
活泼金属(或NH4+)与活泼的非金属或酸根离子、OH-
静电作用:
指静电吸引和静电排斥的作用
范德华力:
(1)概念:分子之间普遍存在的一种把分子聚集在一起的相互作用力。范德华力的作用能通常比化学键的键能小得多,一般只有2~20kJ/mol,主要影响物质的物理性质(熔、沸点和溶解度等)。
(2)规律:组成和结构相似的由分子构成的物质,相对分子质量越大,范德华力越大,物质的熔、沸点越高。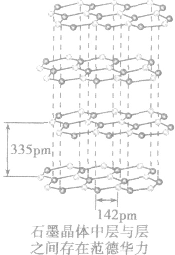
水分子间氢键的表示方法及意义:
(1)表示方法:如下图所示

(2)意义:水分子问存在氢键,使水的熔点和沸点升高,高于同主族其他元素的气态氢化物,所以常温常压下水呈液态。另外,在同态水(冰晶体)中,水分子间以氢键结合成排列规整的晶体,水分子间的氢键使冰的结构里存在较大的空隙,造成体积膨胀、密度减小至低于液态水的密度。水的这种性质对水生动物的生存有重要意义。
范德华力和氢键:
| 范德华力 | 氢键 | |
| 概念 | 把分子聚集在一起的作用力 | 分子中与氢原子形成共价键的非金属元素原子如果吸引电子的能力很强,原子半径很小,则使氢原子几乎成为“裸露”的质子,带部分正电荷,这样的分子之间氢核与带部分负电荷的非金属元素原子相互吸引,这种静电作用就是氢键 |
| 存在范围 | 分子之间 | 某些含强极性键的氢化物分子间(如 HF、H2O、NH3)等 |
| 强弱比较 | 比化学键弱得多 | 比化学键弱,但比范德华力强 |
| 影响因素 | 组成和结构相似的由分子组成的物质,相对分子质量越大,范德华力越大 | 形成氢键的除H外的非金属元素原子吸引电子的能力越强,半径越小,则氢键越强 |
| 对物质性质的影响 | 影响物质的熔沸点、溶解度等物理性质。一般来说,组成和结构相似的由分子组成的物质,随相对分子质量的增大,物质的熔沸点升高,如熔沸点: 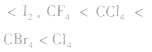 |
分子间氢键的存在,使物质的熔沸点升高,在水中的溶解度增大,如熔沸点:H2O 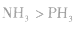 |
发现相似题
与“固体乙醇晶体中不存在的作用力是[ ]A.离子键B.极性键C.非...”考查相似的试题有:
- 下列叙述正确的是( )A.离子化合物中不可能含有共价键B.共价化合物中不可能含有离子键C.非极性分子中一定含有非极性键D....
- 下列叙述正确的是( )A.分子晶体中的每个分子内一定含有共价键B.原子晶体中的相邻原子间只存在非极性共价键C.离子晶体中...
- 下列物质中,既含有极性共价键,又含有非极性共价键的是[ ]A.CCl4B.CO2C.NH4ClD.C2H4
- 已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素...
- 根据下列10种物质的化学式与序号,填写下列空白。①O2、②H2、③NH4NO3、④K2O2、⑤Ba(OH)2、 ⑥CH4、⑦CO2、⑧NaF、⑨NH3、⑩I2。(1)由...
- 下列性质可以证明化合物内一定存在离子键的是[ ]A.可溶于水B.具有较高的熔点C.水溶液能导电D.熔融状态能导电
- 构成下列四种物质的微粒间,既存在离子键又存在共价键的是( )A.K2SB.Na2O2C.MgCl2D.SO3
- 下列各组物质气化或熔化时,所克服的粒子间的作用力属于同种类型的是[ ]A.二氧化硅和生石灰的熔化B.氯化钠和铁的熔化C.碘...
- 氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:(1)由B2O3制备BF3、...
- 共价键、离子键和范德华力都是微观粒子之间的不同作用力,下列物质: ①Na2O2;②SiO2;③石墨;④金刚石;⑤CaCl2;⑥白磷,其中含...