本试题 “下列说法正确的是( )A.氯化镁溶液导电时,镁离子向电源正极移动B.将一小块金属钠加入氯化铁溶液中有气体和红褐色沉淀生成C.除去铜粉中少量的氧化铜可以...” 主要考查您对关于溶液的计算
固体溶解度
物质的除杂
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 关于溶液的计算
- 固体溶解度
- 物质的除杂
溶质质量分数:
1. 概念:溶液中溶质的质量分数是溶质质量与溶液质量之比。
2. 表达式:
溶质质量分数= =
=
3. 含义:溶质质量分数的含义是指每100份质量的溶液中含有溶质的质份为多少。如100g10%的NaCl溶液中含有10gNaCl.。不要误认为是100g水中含有10gNaCl。
应用溶质质量分数公式的注意事项:
①溶质的质量是指形成溶液的那部分溶质,没有进入溶液的溶质不在考虑范围之内。如在20℃时,100g水中最多能溶解36gNaCl,则20gNaCl放入50g 水中溶解后,溶质的质量只能是18g。
②溶液的质量是该溶液中溶解的全部溶质的质量与溶剂的质量之和(可以是一种或几种溶质)。
③计算时质量单位应统一。
④由于溶液的组成是指溶液中各成分在质量方面的关系,因此,对溶液组成的变化来说,某物质的质量分数只有在不超过其最大溶解范围时才有意义。
例如在20℃时,NaCl溶液中溶质的质量分数最大为26.5%,此时为该温度下氯化钠的饱和溶液,再向溶液中加入溶质也不会再溶解,浓度也不会再增大。因此离开实际去讨论溶质质量分数更大的NaCl溶液是没有意义的。
⑤运用溶质质量分数表示溶液时,必须分清溶质的质量、溶剂的质量和溶液的质量。
a.结晶水合物溶于水时,其溶质指不含结晶水的化合物。如CuSO4·5H2O溶于水时,溶质是CuSO4。
溶质质量分数= ×100%
×100%
b.当某些化合物溶于水时与水发生了反应,此时溶液中的溶质是反应后生成的物质。如Na2O溶于水时发生如下反应:Na2O+H2O==2NaOH。反应后的溶质是NaOH,此
溶液的溶质质量分数= 。
。
c.若两种物质能发生反应,有沉淀或气体生成,此时溶液中的溶质质量分数=
影响溶质质量分数的因素:
(1)影响溶质质量分数的因素是溶质、溶剂的质录,与温度、是否饱和无关。在改变温度的过程中若引起溶液中溶质、溶剂质量改变,溶质的质量分数也会改变,但归根结底,变温时必须考虑溶质、溶剂的质量是否改变。因而,影响溶质的质量分数的因素还是溶质、溶剂的质量。例如:
①将饱和的NaNO3溶液降低温度,由于析出品体,溶液中溶质的质缺减少,溶剂的质量不变,所以溶液中溶质的质量分数变小。
②将饱和的NaNO3溶液升高温度,只是溶液变成了不饱和溶液,溶液中溶质、溶剂的质量不变,因而溶液中溶质的质量分数不变。
(2)不要认为饱和溶液变成不饱和溶液,溶质的质量分数就变小;也不要认为不饱和溶液变成饱和溶液,溶质的质量分数就变大;要具体问题具体分析。
有关溶质质量分数计算的类型
(1)利用公式的基本计算
①已知溶质、溶剂的质量,求溶质的质量分数。
直接利用公式:溶质的质量分数= ×100%
×100%
②已知溶液、溶质的质量分数,求溶质、溶剂的质量。
利用公式:溶质的质量=溶液的质量×溶质的质量分数
溶剂的质量=溶液的质量一溶质的质量
③已知溶质的质量、溶质的质量分数,求溶液的质量。
利用公式:溶液的质量=溶质的质量÷溶质的质量分数
④质量、体积、密度与溶质质量分数的换算
当溶液的量用体积表示时,计算时应首先将溶液的体积换算成质量后再进行相关计算。因为计算溶质的质量分数的公式中各种量都是以质量来表示的,不能以体积的数据来代替。
利用公式:溶液的质量=溶液的体积×溶液的密度
(2)溶液的稀释与浓缩
注意:
a.几种溶液混合,溶液的体积不能简单相加,即V总≠VA+VB
b.混合后溶液的质量、溶质的质量可以相加,即m总=mA+mB
c. 要求混合后溶液的总体积,必须依据公式V=m/ρ,所以要知道混合溶液的密度才能求出总体积。
(3)饱和溶液中溶质质量分数的计算
a. 固体溶解度的计算公式
根据固体溶解度的计算公式[溶解度(S)= ×100g]可推导出:
×100g]可推导出: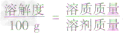 ,
,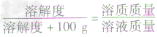
b. 溶解度与溶质质量分数的关系
特殊的溶质质量分数的计算:
(1)结晶水合物溶于水时,其溶质指不含结晶水的化合物。
如CuSO4·5H2O溶于水时,溶质是CuSO4。
溶质质量分数= ×100%
×100%
(2)溶质只能是已溶解的那一部分,没有溶解的不能做溶质计算
如20℃时,20gNaCl投入到50g中水中(20℃时,NaCl的溶解度为36g)。20℃时50g水最多只能溶解18gNaCl,如溶质的质量为18g,而不是20g,所以该NaCl溶液的质量分数=18g/(50g+18g)×100%=26.5%。
(3)当某些化合物溶于水时与水发生了反应,此时溶液中的溶质是反应后生成的物质。如Na2O溶于水时发生如下反应:Na2O+H2O==2NaOH。反应后的溶质是NaOH,此
溶液的溶质质量分数= 。
。
(4)某混合物溶于水,要计算某一溶质的质量分数,溶液的质量包括混合物与水的质量
如5gNaCl和1gKNO3的混合物溶于100g水,计算NaCl的溶质质量分数:
ω(NaCl)=5g/(5g+1g+100g)×100%=4.7%。
(5)利用元素的质量分数进行计算
溶液中溶质的质量分数与溶质中某元素的质量分数之间有着联系。溶液的溶质质量分数×溶质中某元素的质量分数=溶液中某元素的质量分数。
溶质质量分数的不变规律:
(1)从一瓶溶液中不论取出多少溶液,取出溶液及剩余溶液的溶质质量分数与原来溶液中溶质质量分数相同。
(2)溶质、溶质质量分数均相同的两种溶液混合,所得溶液的质量分数保持不变。
(3)一定温度时,向某饱和溶液中加入该溶质,所得溶液的溶质质量分数保持不变。
(4)一定温度时,对某饱和溶液恒温蒸发溶剂,所得溶液的溶质质量分数保持不变。
(5)对于溶解度随温度升高而增大的物质来说,将其饱和溶液(底部没有固体时)升高温度,所得溶液的溶质质量分数保持不变。而对于溶解度随温度升高而减小的物质(熟石灰)来说,降低温度,所得溶液的溶质质量分数保持不变。
1. 概念:溶液中溶质的质量分数是溶质质量与溶液质量之比。
2. 表达式:
溶质质量分数=
 =
=
3. 含义:溶质质量分数的含义是指每100份质量的溶液中含有溶质的质份为多少。如100g10%的NaCl溶液中含有10gNaCl.。不要误认为是100g水中含有10gNaCl。
应用溶质质量分数公式的注意事项:
①溶质的质量是指形成溶液的那部分溶质,没有进入溶液的溶质不在考虑范围之内。如在20℃时,100g水中最多能溶解36gNaCl,则20gNaCl放入50g 水中溶解后,溶质的质量只能是18g。
②溶液的质量是该溶液中溶解的全部溶质的质量与溶剂的质量之和(可以是一种或几种溶质)。
③计算时质量单位应统一。
④由于溶液的组成是指溶液中各成分在质量方面的关系,因此,对溶液组成的变化来说,某物质的质量分数只有在不超过其最大溶解范围时才有意义。
例如在20℃时,NaCl溶液中溶质的质量分数最大为26.5%,此时为该温度下氯化钠的饱和溶液,再向溶液中加入溶质也不会再溶解,浓度也不会再增大。因此离开实际去讨论溶质质量分数更大的NaCl溶液是没有意义的。
⑤运用溶质质量分数表示溶液时,必须分清溶质的质量、溶剂的质量和溶液的质量。
a.结晶水合物溶于水时,其溶质指不含结晶水的化合物。如CuSO4·5H2O溶于水时,溶质是CuSO4。
溶质质量分数=
 ×100%
×100%b.当某些化合物溶于水时与水发生了反应,此时溶液中的溶质是反应后生成的物质。如Na2O溶于水时发生如下反应:Na2O+H2O==2NaOH。反应后的溶质是NaOH,此
溶液的溶质质量分数=
 。
。c.若两种物质能发生反应,有沉淀或气体生成,此时溶液中的溶质质量分数=

影响溶质质量分数的因素:
(1)影响溶质质量分数的因素是溶质、溶剂的质录,与温度、是否饱和无关。在改变温度的过程中若引起溶液中溶质、溶剂质量改变,溶质的质量分数也会改变,但归根结底,变温时必须考虑溶质、溶剂的质量是否改变。因而,影响溶质的质量分数的因素还是溶质、溶剂的质量。例如:
①将饱和的NaNO3溶液降低温度,由于析出品体,溶液中溶质的质缺减少,溶剂的质量不变,所以溶液中溶质的质量分数变小。
②将饱和的NaNO3溶液升高温度,只是溶液变成了不饱和溶液,溶液中溶质、溶剂的质量不变,因而溶液中溶质的质量分数不变。
(2)不要认为饱和溶液变成不饱和溶液,溶质的质量分数就变小;也不要认为不饱和溶液变成饱和溶液,溶质的质量分数就变大;要具体问题具体分析。
有关溶质质量分数计算的类型
(1)利用公式的基本计算
①已知溶质、溶剂的质量,求溶质的质量分数。
直接利用公式:溶质的质量分数=
 ×100%
×100% ②已知溶液、溶质的质量分数,求溶质、溶剂的质量。
利用公式:溶质的质量=溶液的质量×溶质的质量分数
溶剂的质量=溶液的质量一溶质的质量
③已知溶质的质量、溶质的质量分数,求溶液的质量。
利用公式:溶液的质量=溶质的质量÷溶质的质量分数
④质量、体积、密度与溶质质量分数的换算
当溶液的量用体积表示时,计算时应首先将溶液的体积换算成质量后再进行相关计算。因为计算溶质的质量分数的公式中各种量都是以质量来表示的,不能以体积的数据来代替。
利用公式:溶液的质量=溶液的体积×溶液的密度
(2)溶液的稀释与浓缩
| 方法 | 计算依据 | 计算公式 | |
| 溶液的稀释 | ①加水稀释 ②加稀溶液稀释 |
①加水稀释前后,溶液中溶质的质量不变 ②用稀溶液稀释浓溶液时。稀溶液中溶质的质量与浓溶液中溶质的质量之和等于混合后溶液中溶质的质量 |
加水稀释:稀释前后溶液中溶质的质量不变 m浓×ω浓%=(m浓+m水)×ω稀% |
| 溶液的浓缩 | ①添加溶质 ②蒸发溶剂 ③加入浓溶液 | ①原溶液中的溶质与后加入的溶质质量之和等于混合后溶液中的溶质质量 ②蒸发溶剂前后溶液中溶质的质量不变(没有溶质析出) ③原溶液中的溶质与后加入浓溶液中的溶质质量之和等于混合后溶液中的溶质质量 |
蒸发浓缩:浓缩前后溶液中溶质的质量不变(m稀-m水)×ω浓%=m稀×ω稀% |
a.几种溶液混合,溶液的体积不能简单相加,即V总≠VA+VB
b.混合后溶液的质量、溶质的质量可以相加,即m总=mA+mB
c. 要求混合后溶液的总体积,必须依据公式V=m/ρ,所以要知道混合溶液的密度才能求出总体积。
(3)饱和溶液中溶质质量分数的计算
a. 固体溶解度的计算公式
根据固体溶解度的计算公式[溶解度(S)=
 ×100g]可推导出:
×100g]可推导出: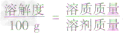 ,
,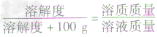
b. 溶解度与溶质质量分数的关系
| 溶解度 | 溶质质量分数 | |
| 意义 | 物质溶解性的量度,受外界温度的影响 | 表示溶液中溶质质量的多少,不受外界条件影响 |
| 容积要求 | 100g | 无要求 |
| 温度要求 | 与温度有关 | 一般与温度无关 |
| 溶液是否饱和 | 一定达到饱和 | 不一定饱和 |
| 计算公式 |  ×100g ×100g |
 |
| 单位 | 克 | 无单位 |
| 联系 | 饱和溶液中溶质的质量分数= | |
特殊的溶质质量分数的计算:
(1)结晶水合物溶于水时,其溶质指不含结晶水的化合物。
如CuSO4·5H2O溶于水时,溶质是CuSO4。
溶质质量分数=
 ×100%
×100%(2)溶质只能是已溶解的那一部分,没有溶解的不能做溶质计算
如20℃时,20gNaCl投入到50g中水中(20℃时,NaCl的溶解度为36g)。20℃时50g水最多只能溶解18gNaCl,如溶质的质量为18g,而不是20g,所以该NaCl溶液的质量分数=18g/(50g+18g)×100%=26.5%。
(3)当某些化合物溶于水时与水发生了反应,此时溶液中的溶质是反应后生成的物质。如Na2O溶于水时发生如下反应:Na2O+H2O==2NaOH。反应后的溶质是NaOH,此
溶液的溶质质量分数=
 。
。(4)某混合物溶于水,要计算某一溶质的质量分数,溶液的质量包括混合物与水的质量
如5gNaCl和1gKNO3的混合物溶于100g水,计算NaCl的溶质质量分数:
ω(NaCl)=5g/(5g+1g+100g)×100%=4.7%。
(5)利用元素的质量分数进行计算
溶液中溶质的质量分数与溶质中某元素的质量分数之间有着联系。溶液的溶质质量分数×溶质中某元素的质量分数=溶液中某元素的质量分数。
溶质质量分数的不变规律:
(1)从一瓶溶液中不论取出多少溶液,取出溶液及剩余溶液的溶质质量分数与原来溶液中溶质质量分数相同。
(2)溶质、溶质质量分数均相同的两种溶液混合,所得溶液的质量分数保持不变。
(3)一定温度时,向某饱和溶液中加入该溶质,所得溶液的溶质质量分数保持不变。
(4)一定温度时,对某饱和溶液恒温蒸发溶剂,所得溶液的溶质质量分数保持不变。
(5)对于溶解度随温度升高而增大的物质来说,将其饱和溶液(底部没有固体时)升高温度,所得溶液的溶质质量分数保持不变。而对于溶解度随温度升高而减小的物质(熟石灰)来说,降低温度,所得溶液的溶质质量分数保持不变。
概念:
在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里,该温度下的溶解度。
正确理解溶解度概念的要素:
①条件:在一定温度下,影响固体物质溶解度的内因是溶质和溶剂的性质,而外因就是温度。如果温度改变,则固体物质的溶解度也会改变,因此只有指明温度时,溶解度才有意义。
②标准:“在100g溶剂里”,需强调和注意的是:此处100g是溶剂的质量,而不是溶液的质量。
③状态:“达到饱和状态”,溶解度是衡址同一条件下某种物质溶解能力大小的标准,只有达到该条件下溶解的最大值,才可知其溶解度,因此必须要求“达到饱和状态”。
④单位:溶解度是所溶解的质量,常用单位为克(g)。
概念的理解:
①如果不指明溶剂,通常所说的溶解度是指固体物质在水中的溶解度。
②溶解度概念中的四个关键点:“一定温度,100g 溶剂、饱和状态、溶解的质量”是同时存在的,只有四个关键点都体现出来了,溶解度的概念和应用才是有意义的,否则没有意义,说法也是不正确的。
溶解度曲线:
在平面直角坐标系里用横坐标表示温度,纵坐标表示溶解度,画出某物质的溶解度随温度变化的曲线,叫这种物质的溶解度曲线。
①表示意义
a.表示某物质在不同温度下的溶解度和溶解度随温度变化的情况;
b.溶解度曲线上的每一个点表示该溶质在某一温度下的溶解度;
c.两条曲线的交点表示这两种物质在某一相同温度下具有相同的溶解度;
d.曲线下方的点表示溶液是不饱和溶液;
e.在溶解度曲线上方靠近曲线的点表示过饱和溶液(一般物质在较高温度下制成饱和溶液,快速地降到室温,溶液中溶解的溶质的质量超过室温的溶解度,但尚未析出晶体时的溶液叫过饱和溶液)。
②溶解度曲线的变化规律
a.有些固体物质的溶解度受温度影响较大,表现在曲线“坡度”比较“陡”,如KNO3;
b.少数固体物质的溶解度受温度的影响很小,表现在曲线“坡度”比较“平”,如NaCl 。
c.极少数固体物质的溶解度随温度的升高而减小,表现在曲线“坡度”下降,如Ca(OH)2
③应用
a.根据溶解度曲线可以查出某物质在一定温度下的溶解度;
b.可以比较不同物质在同一温度下的溶解度大小;
c.可以知道某物质的溶解度随温度的变化情况;
d.可以选择对混合物进行分离或提纯的方法;
e.确定如何制得某温度时某物质的饱和溶液的方法等。
运用溶解度曲线判断混合物分离、提纯的方法:
根据溶解度曲线受温度变化的影响,通过改变温度或蒸发溶剂,使溶质结晶折出,从而达到混合物分离、提纯的目的。如KNO3和NaCl的混合物的分离。 (KNO3,NaCl溶解度曲线如图)
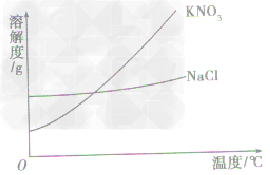
(1)温度变化对物质溶解度影响较大,要提纯这类物质。可采用降温结晶法。
具体的步骤为:①配制高温时的饱和溶液,②降温,③过滤,④干燥。如KNO3中混有少量的NaCl,提纯KNO3可用此法。
(2)温度变化对物质溶解度影响较小,要提纯这类物质,可用蒸发溶剂法。
具体步骤为:①溶解,②蒸发溶剂,③趁热过滤,④干燥。如NaCl中混有少量KNO3,要提纯NaCl,可配制溶液,然后蒸发溶剂,NaCl结晶析出,而KNO3在较高温度下,还没有达到饱和,不会结晶,趁热过滤,可得到较纯净的NaCl。
在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里,该温度下的溶解度。
正确理解溶解度概念的要素:
①条件:在一定温度下,影响固体物质溶解度的内因是溶质和溶剂的性质,而外因就是温度。如果温度改变,则固体物质的溶解度也会改变,因此只有指明温度时,溶解度才有意义。
②标准:“在100g溶剂里”,需强调和注意的是:此处100g是溶剂的质量,而不是溶液的质量。
③状态:“达到饱和状态”,溶解度是衡址同一条件下某种物质溶解能力大小的标准,只有达到该条件下溶解的最大值,才可知其溶解度,因此必须要求“达到饱和状态”。
④单位:溶解度是所溶解的质量,常用单位为克(g)。
概念的理解:
①如果不指明溶剂,通常所说的溶解度是指固体物质在水中的溶解度。
②溶解度概念中的四个关键点:“一定温度,100g 溶剂、饱和状态、溶解的质量”是同时存在的,只有四个关键点都体现出来了,溶解度的概念和应用才是有意义的,否则没有意义,说法也是不正确的。
溶解度曲线:
在平面直角坐标系里用横坐标表示温度,纵坐标表示溶解度,画出某物质的溶解度随温度变化的曲线,叫这种物质的溶解度曲线。
①表示意义
a.表示某物质在不同温度下的溶解度和溶解度随温度变化的情况;
b.溶解度曲线上的每一个点表示该溶质在某一温度下的溶解度;
c.两条曲线的交点表示这两种物质在某一相同温度下具有相同的溶解度;
d.曲线下方的点表示溶液是不饱和溶液;
e.在溶解度曲线上方靠近曲线的点表示过饱和溶液(一般物质在较高温度下制成饱和溶液,快速地降到室温,溶液中溶解的溶质的质量超过室温的溶解度,但尚未析出晶体时的溶液叫过饱和溶液)。
②溶解度曲线的变化规律
a.有些固体物质的溶解度受温度影响较大,表现在曲线“坡度”比较“陡”,如KNO3;
b.少数固体物质的溶解度受温度的影响很小,表现在曲线“坡度”比较“平”,如NaCl 。
c.极少数固体物质的溶解度随温度的升高而减小,表现在曲线“坡度”下降,如Ca(OH)2
③应用
a.根据溶解度曲线可以查出某物质在一定温度下的溶解度;
b.可以比较不同物质在同一温度下的溶解度大小;
c.可以知道某物质的溶解度随温度的变化情况;
d.可以选择对混合物进行分离或提纯的方法;
e.确定如何制得某温度时某物质的饱和溶液的方法等。
运用溶解度曲线判断混合物分离、提纯的方法:
根据溶解度曲线受温度变化的影响,通过改变温度或蒸发溶剂,使溶质结晶折出,从而达到混合物分离、提纯的目的。如KNO3和NaCl的混合物的分离。 (KNO3,NaCl溶解度曲线如图)

(1)温度变化对物质溶解度影响较大,要提纯这类物质。可采用降温结晶法。
具体的步骤为:①配制高温时的饱和溶液,②降温,③过滤,④干燥。如KNO3中混有少量的NaCl,提纯KNO3可用此法。
(2)温度变化对物质溶解度影响较小,要提纯这类物质,可用蒸发溶剂法。
具体步骤为:①溶解,②蒸发溶剂,③趁热过滤,④干燥。如NaCl中混有少量KNO3,要提纯NaCl,可配制溶液,然后蒸发溶剂,NaCl结晶析出,而KNO3在较高温度下,还没有达到饱和,不会结晶,趁热过滤,可得到较纯净的NaCl。
混合物的分离和提纯(除杂)
1. 分离与提纯的基本原理
(1)分离:就是用物理或化学的方法将混合物巾的各组分分开,并将物质恢复到原状态。
(2)提纯和除杂:用物理或化学的方法把混合物中的杂质除去而得到纯物质。在提纯过程中,如果杂质发生了化学变化,不必恢复成原物质。二者的方法在很多情况下是相似的,但分离比提纯的步骤要多,因为各组分均要保留,绎过化学反应使混合物中各组分经转化而分离后还要复原为原来的组分物质提纯和除杂过程中经常用到分离操作,二者有时又密不可分。
2.分离和提纯应遵循的原则
(1)不能“玉石俱焚”:即试剂一般要求与杂质反应,不与要保留的物质反应。但在特殊情况下,所加试剂可和保留物质应应,但最终要转化成需要保留的物质如除去FeCl3,溶液中的NaCl,可加过量的NaOH溶液→过滤→洗涤→加适量稀盐酸。
(2)“不增““不减”:即不增加新的杂质,不减少要保留的物质如除去FeCl3中的少量Fe2(SO4)3应选用BaCl2而不应选用Ba(NO3)2,否则发生反应3Ba(NO3)2+Fe2(SO4)3==3BaSO4↓+2Fe(NO3)3溶液中又增加了Fe(NO3)3.
(3)易分离:反应后,物质的状态不同,便于分离。
(4)不污染环境:即耍求所选用的除杂方法不能产生可污染环境的物质。
(5)不能“旧貌变新颜”:即除杂结束前,要恢复保留物质的原有状态。
常见除杂的方法:
CO2(O2):将气体通过灼热的铜网
CO2(H2或CO):将气体通过灼热的氧化铜
O2或CO2或H2(含H2O):将气体通过浓硫酸或氧化钙或氯化钙等干燥剂
O2或H2或CO(含CO2或SO2):将气体通入氢氧化钠溶液中
Cu(含Fe或Mg或Zn):加入足量的稀盐酸或稀硫酸,过滤
Fe(含Cu):用磁铁将铁粉吸引出来
Cu(含CuO),Fe(含Fe2O3):高温下与H2或CO反应
CuO(含Cu或C):在空气中灼烧
CaO(含CaCO3):高温煅烧(CaCO3分解成CaO和CO2)
CaCO3(含CaO):加足量水溶解,过滤,取滤渣
Ca(OH)2(含CaO)加足量水
FeSO4溶液(含H2SO4或CuSO4),FeCl2溶液(含盐酸或CuCl2):加过量铁粉,过滤,取滤液
NaCl溶液(含Na2CO3):加适量稀盐酸
Na2SO4溶液(含CuSO4):加适量 NaOH 溶液
酸、碱、盐溶液的除杂技巧:
1.被提纯物与杂质所含阳离子相同时,选取与杂质中的阴离子不共存的阳离子,再与被提纯物中的阴离子组合出除杂试剂。如除去Na2SO4溶液中的NaOH:可选用稀H2SO4溶液为除杂试剂(2NaOH+ H2SO4==Na2SO4+2H2O)、除去KCl溶液中的 K2SO4:可选用BaCl2溶液为除杂试制(K2SO4+BaCl2 ==2KCl+BaSO4↓,过滤除去)
2.被提纯物与杂质所含阴离子相同时,选取与杂质中阳离子不共存的阴离子,再与被提纯物中的阳离子组合出除杂试剂,如除去NaCl溶液中的BaCl2:可选用 Na2SO4溶液为除杂试剂(BaCl2+Na2SO4=BaSO4↓ +2NaCl,过滤除去).再如除去KNO3溶液中的AgNO3:可选用KCl溶液为除杂试剂(AgNO3+KCl=AgCl↓ +KNO3,过滤除去)。
3.被提纯物质与杂质所含阴离子、阳离子都不相同时,应选取与杂质中阴、阳离子都不共存的阳、阴离子组合出除杂试剂。如:除去NaCl溶液中的CuSO4:可选用Ba(OH)2溶液为除杂试剂[CuSO4+Ba(OH)2= BaSO4↓+Cu(OH)2↓,过滤除去]。
分离和提纯的方法:
物质的分离和提纯有两种主要的方法,即物理方法和化学方法。实际上在实验过程中往往需通过综合法来进行。
(1)物理方法主要包括过滤,蒸馏,结晶
(2)化学方法
(3)综合法
在进行混合物的分离或提纯时,采用一种方法往往不能达到目的,而要采用几种方法才能完成,这就是综合法。综合法主要有三种:
①物理方法的综合:主要是溶解、过滤、蒸发、结晶等方法的结合:
②化学方法的综合:当某物质所含杂质不止一种时,通常需加入多种试剂除去(或分离)不同的物质。
③物理与化学方法的综合:当某物质所含杂质不止一种,且有能用物理方法除去(或分离)的杂质时,首先应考虑用物理方法除去一种或几种杂质,然后再用化学方法除去其余杂质。
(4)除杂方法的几个优化原则
①若同时有多种方法能除去杂质,要选择那些简单易行、除杂彻底的方法。
②应尽量选择既可除去杂质,又可增加保留物质的方法,即“一举两得”。
③先考虑物理方法,再用化学方法。
常见的混合物类型及分类与提纯的方法见下表:
1. 分离与提纯的基本原理
(1)分离:就是用物理或化学的方法将混合物巾的各组分分开,并将物质恢复到原状态。
(2)提纯和除杂:用物理或化学的方法把混合物中的杂质除去而得到纯物质。在提纯过程中,如果杂质发生了化学变化,不必恢复成原物质。二者的方法在很多情况下是相似的,但分离比提纯的步骤要多,因为各组分均要保留,绎过化学反应使混合物中各组分经转化而分离后还要复原为原来的组分物质提纯和除杂过程中经常用到分离操作,二者有时又密不可分。
2.分离和提纯应遵循的原则
(1)不能“玉石俱焚”:即试剂一般要求与杂质反应,不与要保留的物质反应。但在特殊情况下,所加试剂可和保留物质应应,但最终要转化成需要保留的物质如除去FeCl3,溶液中的NaCl,可加过量的NaOH溶液→过滤→洗涤→加适量稀盐酸。
(2)“不增““不减”:即不增加新的杂质,不减少要保留的物质如除去FeCl3中的少量Fe2(SO4)3应选用BaCl2而不应选用Ba(NO3)2,否则发生反应3Ba(NO3)2+Fe2(SO4)3==3BaSO4↓+2Fe(NO3)3溶液中又增加了Fe(NO3)3.
(3)易分离:反应后,物质的状态不同,便于分离。
(4)不污染环境:即耍求所选用的除杂方法不能产生可污染环境的物质。
(5)不能“旧貌变新颜”:即除杂结束前,要恢复保留物质的原有状态。
常见除杂的方法:
CO2(O2):将气体通过灼热的铜网
CO2(H2或CO):将气体通过灼热的氧化铜
O2或CO2或H2(含H2O):将气体通过浓硫酸或氧化钙或氯化钙等干燥剂
O2或H2或CO(含CO2或SO2):将气体通入氢氧化钠溶液中
Cu(含Fe或Mg或Zn):加入足量的稀盐酸或稀硫酸,过滤
Fe(含Cu):用磁铁将铁粉吸引出来
Cu(含CuO),Fe(含Fe2O3):高温下与H2或CO反应
CuO(含Cu或C):在空气中灼烧
CaO(含CaCO3):高温煅烧(CaCO3分解成CaO和CO2)
CaCO3(含CaO):加足量水溶解,过滤,取滤渣
Ca(OH)2(含CaO)加足量水
FeSO4溶液(含H2SO4或CuSO4),FeCl2溶液(含盐酸或CuCl2):加过量铁粉,过滤,取滤液
NaCl溶液(含Na2CO3):加适量稀盐酸
Na2SO4溶液(含CuSO4):加适量 NaOH 溶液
酸、碱、盐溶液的除杂技巧:
1.被提纯物与杂质所含阳离子相同时,选取与杂质中的阴离子不共存的阳离子,再与被提纯物中的阴离子组合出除杂试剂。如除去Na2SO4溶液中的NaOH:可选用稀H2SO4溶液为除杂试剂(2NaOH+ H2SO4==Na2SO4+2H2O)、除去KCl溶液中的 K2SO4:可选用BaCl2溶液为除杂试制(K2SO4+BaCl2 ==2KCl+BaSO4↓,过滤除去)
2.被提纯物与杂质所含阴离子相同时,选取与杂质中阳离子不共存的阴离子,再与被提纯物中的阳离子组合出除杂试剂,如除去NaCl溶液中的BaCl2:可选用 Na2SO4溶液为除杂试剂(BaCl2+Na2SO4=BaSO4↓ +2NaCl,过滤除去).再如除去KNO3溶液中的AgNO3:可选用KCl溶液为除杂试剂(AgNO3+KCl=AgCl↓ +KNO3,过滤除去)。
3.被提纯物质与杂质所含阴离子、阳离子都不相同时,应选取与杂质中阴、阳离子都不共存的阳、阴离子组合出除杂试剂。如:除去NaCl溶液中的CuSO4:可选用Ba(OH)2溶液为除杂试剂[CuSO4+Ba(OH)2= BaSO4↓+Cu(OH)2↓,过滤除去]。
分离和提纯的方法:
物质的分离和提纯有两种主要的方法,即物理方法和化学方法。实际上在实验过程中往往需通过综合法来进行。
(1)物理方法主要包括过滤,蒸馏,结晶
| 方法 | 适用范围 | 举例 | 注意事项 |
| 过滤 | 分离不溶性固体和液体 | 粗盐提纯 | ①过滤时要“一贴、二低,三靠”; ②必要时要洗涤沉淀物 |
| 结晶 | 利用混合物中各组分在某种溶剂中溶解度随温度变化不同的性质来分离提纯物质 | 分离氯化钠和硝酸钾混合物 | ①一般先配较高温度下的浓溶液,然后降温结晶: ②结晶后过滤,分离出晶体 |
| 蒸馏 | 沸点不同的液体混合物 | 石油的分馏 | ①温度计水银球在蒸馏烧瓶的支管口处; ②加沸石(或碎瓷片); ③冷凝管水流方向 |
(2)化学方法
| 除杂方法 | 除杂原理 | 应用实例 |
| 化气法 | 与杂质反应生成气体而除去 | 除Na2SO4中的NaCO3,可加适量稀盐酸 NaCO3+H2SO4==Na2SO4+CO2↑+H2O |
| 沉淀法 | 将杂质转化为沉淀过滤除去 | 除去NaCl中的Na2SO4.可加适量的BaCl2 Na2SO4+BaCl2==BaSO4↓+2NaCl |
| 置换法 | 将杂质通过置换反应而除去 | c除去FeSO4中的CuSO4可加过量的铁粉 CuSO4+Fe==Cu+FeSO4 |
| 溶解法 | 将杂质溶丁某种试剂而除去 | 除C粉中的CuO粉末,可加适量稀盐酸,再过滤 CuO+H2SO4==CuSO4+H2O |
| 加热法 | 杂质受热易分解,通过加热将杂质除去 | 除CaO中的CaCO3可加热 CaCO3  CaO+CO2↑ CaO+CO2↑ |
| 转化法 | 将杂质通过化学反应转化为主要成分 | 除去CO2中的CO,可将气体通过灼热的CuO CO+CuO  Cu+CO2 Cu+CO2 |
(3)综合法
在进行混合物的分离或提纯时,采用一种方法往往不能达到目的,而要采用几种方法才能完成,这就是综合法。综合法主要有三种:
①物理方法的综合:主要是溶解、过滤、蒸发、结晶等方法的结合:
②化学方法的综合:当某物质所含杂质不止一种时,通常需加入多种试剂除去(或分离)不同的物质。
③物理与化学方法的综合:当某物质所含杂质不止一种,且有能用物理方法除去(或分离)的杂质时,首先应考虑用物理方法除去一种或几种杂质,然后再用化学方法除去其余杂质。
(4)除杂方法的几个优化原则
①若同时有多种方法能除去杂质,要选择那些简单易行、除杂彻底的方法。
②应尽量选择既可除去杂质,又可增加保留物质的方法,即“一举两得”。
③先考虑物理方法,再用化学方法。
常见的混合物类型及分类与提纯的方法见下表:
| 混合物类型采用的方法 | 物理方法 | 化学方法 | |
| 固—固混合 | 可溶—可溶 | 结晶 | 把杂质变成沉淀、气体等除去 |
| 可溶—不溶 | 过滤 | —— | |
| 不溶—不溶 | — | 把杂质变成可溶物除去 | |
| 固—液混合 | 过滤 | —— | |
| 液—液混合 | —— | 把杂质变成沉淀,气体或被提纯物 | |
| 气—气混合 | —— | 把杂质变成固体、溶液或被提纯物 | |
发现相似题
与“下列说法正确的是( )A.氯化镁溶液导电时,镁离子向电源正...”考查相似的试题有:
- 某小组同学将530g碳酸钠溶液加入到280g石灰乳(水和氢氧化钙的混合物)中,使之恰好完全反应,所得溶液中溶质的质量分数为1%...
- 现将100克20%的稀硫酸稀释为10%的稀硫酸,所得稀硫酸溶液的质量为( )A.100克B.150克C.200克D.300克
- 在一定温度下,向不饱和的NaNO3溶液中逐渐加入NaNO3晶体,在此变化过程中,溶液里溶质质量分数(ω)与时间(t)的关系正确的...
- A、B、C、D四个烧杯中分别盛有相等质量的水,在温度相同的条件下,向四个烧杯中分别加入20 g、15 g、10 g、5 g某物质,充分溶...
- 一定质量的20%的烧碱溶液和一定质量的硫酸镁溶液恰好完全反应,所得溶液的质量为109.2g,其中溶质的质量分数为13%,计算硫酸...
- 现有100mL20%的硫酸溶液,其密度为1.14g/cm3.下列说法正确的是( )A.该溶液含溶质20gB.溶质质量:溶液质量=1:4C.溶质质...
- 如图为A、B、C在水中的溶解度曲线图:(1)A、C交点的意义是 ;(2)t3℃时,A、B、C三者的溶解度由大到小的顺序是 __________...
- 除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是[ ]物质(括号内为杂质)试剂及操作方法A. Fe2( SO4)3溶液(NaCl...
- 某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少...
- 除去二氧化碳中混有少量一氧化碳的正确方法是[ ]A. 用燃着的木条点燃B. 通过灼热的木炭C. 通过澄清石灰水D. 通过灼热的氧化铜