本试题 “I、恒温下,将amolN2与bmolH2的混合气体通入一个固体容积的密闭容器中,发生如下反应:N2(g)+3H2(g)⇌2NH3(g)(1)若反应进行到某时刻t时,nt(N2)=13m...” 主要考查您对化学平衡的有关计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学平衡的有关计算
化学平衡计算的一般思路和方法:
有天化学平衡的计算一般涉及各组分的物质的量、浓度、转化率、百分含量,气体混合物的密度、平均摩尔质量、压强等。通常的思路是写出反应方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的火系,列出比例式或等式或依据平衡常数求解,这种思路和方法通常称为“三段式法”、如恒温恒压下的反应mA(g)+nB(g) pC(g)+ qD(g)
pC(g)+ qD(g)
(1)令A、B的起始物质的量分别为amol,bmol 达到平衡后,A的消耗量为m·xmol,容器容积为VL。
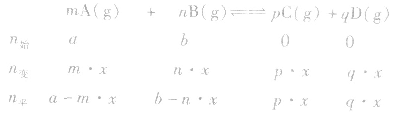
则有:

(2)对于反应物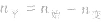 ,对于生成物
,对于生成物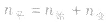
(3)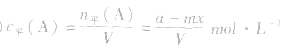
(4)A的转化率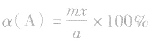
(5)平衡时A的体积(物质的量)分数
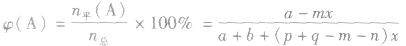
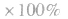
(6)
(7)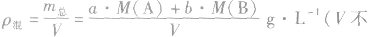
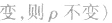
(8)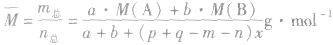
有天化学平衡的计算一般涉及各组分的物质的量、浓度、转化率、百分含量,气体混合物的密度、平均摩尔质量、压强等。通常的思路是写出反应方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的火系,列出比例式或等式或依据平衡常数求解,这种思路和方法通常称为“三段式法”、如恒温恒压下的反应mA(g)+nB(g)
 pC(g)+ qD(g)
pC(g)+ qD(g) (1)令A、B的起始物质的量分别为amol,bmol 达到平衡后,A的消耗量为m·xmol,容器容积为VL。
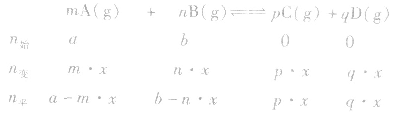
则有:

(2)对于反应物
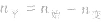 ,对于生成物
,对于生成物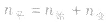
(3)
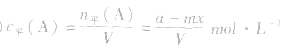
(4)A的转化率
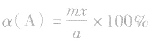
(5)平衡时A的体积(物质的量)分数
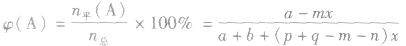
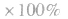
(6)

(7)
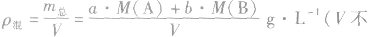
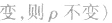
(8)
发现相似题
与“I、恒温下,将amolN2与bmolH2的混合气体通入一个固体容积的密...”考查相似的试题有:
- 哈三中某课外活动小组改进铜与浓硫酸反应的实验,制备并验证二氧化硫的性质,请回答下列问题:(1)铜丝在实验中的作用:____...
- 下列反应原理或过程,不能用勒夏特列原理解释的是A.用N2和H2合成氨需采用高压。B.由H2O2制氧气时使用MnO2催化剂。C.醋酸溶...
- 对于反应aA(g)+bB(g)cC(g)+dD(g),达到平衡后其他条件不变改变压强,则右图适合于哪种情况( )A.a+bc+d,加压C.a+bc+d,减压
- 将等物质的量的A、B、C、D四种物质混和,发生如下反应:当反应进行一定时间后,测得A减少了n mol,B减少了n/2mol,C增加了3n/...
- 一定温度下,将3molA气体和1molB气体通过一密闭容器中,发生如下反应:3A(g)+B(g)xC(g)。请填写下列空白:(1)若容器体积固...
- 某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。(1)反应物为 和 ,生成物为 (2)由图中所给...
- 氮是大气中含量最多的气体,研究氮及其化合物对人类有重要的意义.(1)合成氨的原理为:N2(g)+3H2⇌2NH3△H=-92.4kJ/mol①将...
- 下列有关平衡常数说法正确的是A.温度越高,K值越大B.K值越大,反应的转化率越小C.K值越大,反应的转化率越大D.K值的大小...
- 有一化学平衡mA(g)+nB(g)pC(g)+qD(g),如图所示是A的转化率同压强、温度的关系,分析图可以得出的正确...
- 下列说法不正确的是 A.在固定体积的密闭容器中发生可逆反应A(s)+B(g)C(g)+D(g),当混合气体的密度不再改变时,说明已...