本试题 “关于铜电极的叙述正确的是[ ]A.铜锌原电池中铜是正极B.用电解法精练粗铜时,粗铜作阴极C.在镀件上电镀铜时,可用金属铜作阳极D.电解稀硫酸制 H2、O2时铜...” 主要考查您对原电池原理
电镀
电解精炼铜
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原电池原理
- 电镀
- 电解精炼铜
原电池:
1.定义:将化学能转化为电能的装置。
2.工作原理:
以铜-锌原电池为例
(1)装置图:
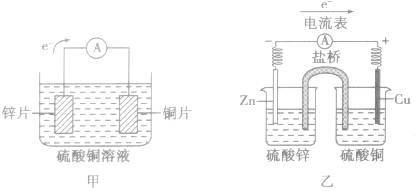
(2)原理图:
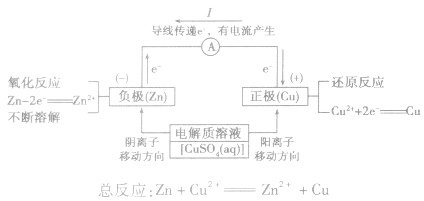
3.实质:化学能转化为电能。
4.构成前提:能自发地发生氧化还原反应。
5.电极反应:
负极:失去电子;氧化反应;流出电子
正极:得到电子;氧化反应;流入电子
6.原电池正负极判断的方法:
①由组成原电池的两级材料判断,一般是活泼金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②根据电流方向或电子流动方向判断,电流是由正极流向负极,电子流动方向是由负极流向正极。
③根据原电池里电解质溶液内离子的定向移动方向,在原电池的电解质溶液中,阳离子移向正极,阴离子移向负极。
④根据原电池两级发生的变化来判断,原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
⑤X极增重或减重:X极质量增加,说明溶液中的阳离子在X极(正极)放电,反之,X极质量减少,说明X极金属溶解,X极为负极。
⑥X极有气泡冒出:发生可析出氢气的反应,说明X极为正极。
⑦X极负极pH变化:析氢或吸氧的电极发生反应后,均能使该电极附近电解质溶液的pH增大,X极附近的pH增大,说明X极为正极。
1.定义:将化学能转化为电能的装置。
2.工作原理:
以铜-锌原电池为例

(1)装置图:

(2)原理图:

3.实质:化学能转化为电能。
4.构成前提:能自发地发生氧化还原反应。
5.电极反应:
负极:失去电子;氧化反应;流出电子
正极:得到电子;氧化反应;流入电子
6.原电池正负极判断的方法:
①由组成原电池的两级材料判断,一般是活泼金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②根据电流方向或电子流动方向判断,电流是由正极流向负极,电子流动方向是由负极流向正极。
③根据原电池里电解质溶液内离子的定向移动方向,在原电池的电解质溶液中,阳离子移向正极,阴离子移向负极。
④根据原电池两级发生的变化来判断,原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
⑤X极增重或减重:X极质量增加,说明溶液中的阳离子在X极(正极)放电,反之,X极质量减少,说明X极金属溶解,X极为负极。
⑥X极有气泡冒出:发生可析出氢气的反应,说明X极为正极。
⑦X极负极pH变化:析氢或吸氧的电极发生反应后,均能使该电极附近电解质溶液的pH增大,X极附近的pH增大,说明X极为正极。
原电池中的电荷流动:
在外电路(电解质溶液以外),电子(负电荷)由负极经导线(包括电流表和其他用电器)流向正极,使负极呈正电性趋势、正极呈负电性趋势。在内电路(电解质溶液中),阳离子(带正电荷)向正极移动,阴离子 (带负电荷)向负极移动。这样形成了电荷持续定向流动,电性趋向平衡的闭合电路。
电镀:
(1)概念:应用电解原理在某些金属表面镀上一薄层其他金属或合金的方法。
(2)目的:使金属增强抗腐蚀能力,增加美观和表面硬度。镀件(待镀金属制品)作阴极
(3)要求
如在铁制品表面上镀铜: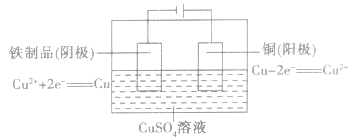
注意:理论上,电镀过程中电镀液的浓度保持不变。
精炼铜:
(1)要求
(2)反应原理如下图所示: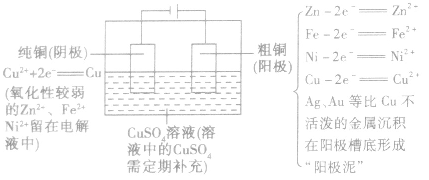
发现相似题
与“关于铜电极的叙述正确的是[ ]A.铜锌原电池中铜是正极B.用电...”考查相似的试题有:
- 生物燃料电池(BFC)是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化率高,是一种真正意义上...
- 右图为铜锌原电池示意图,下列说法正确的是A.电子由铜片通过导线流向锌片B.烧杯中溶液逐渐呈蓝色C.锌片逐渐溶解D.该装置...
- 在用锌片、铜片和稀硫酸组成的原电池装置中,经过—段时间工作后,下列说法正确的是A.锌片是负极,铜片是正极B.电子是从铜片...
- 如图所示装 置中,可观察到电流计指针偏转,M棒变粗,N棒变细。下表所列M、N、P物质中,可以组合成该装置的是( )选项MNPA锌铜硫酸...
- 将洁净的金属片A、B、C、D分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示)。在每次实验时,记录电压指针的移动方向和电...
- 高功率Ni/MH(M表示储氢合金)电池已经用于混合动力汽车。总反应方程式如下:Ni(OH)2+MNiOOH+MH,下列叙述正确的是 ( )A.放...
- 有下列4种燃料电池的工作原理示意图,其中正极反应的产物为水的是
- 原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是( )A.由Al、Cu、稀H2SO4组成原电池...
- 观察下列几个装置示意图,有关叙述正确的是( )A.装置①中阳极上析出红色固体B.装置②的待镀铁制品应与电源正极相连C.装置③...
- 下列叙述错误的是A.钢铁表面发生吸氧腐蚀时,钢铁表面水膜的pH增大B.电解精炼铜时,同一时间内阳极溶解的铜的质量比阴极析...