本试题 “已知元素的电负性和元素的化合价一样,也是元素的一种基本性质.下面给出14种元素的电负性:已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素...” 主要考查您对电负性
共价化合物
离子化合物
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电负性
- 共价化合物
- 离子化合物
电负性:
(1)键合电子、电负性的定义
元素相互化合时,原子中用于形成化学键的电子称为键合电子。电负性用来描述不同元素的原子对键合电子吸引力的大小。
(2)电负性的意义:电负性越大的原子,对键合电子的吸引力越大。
(3)电负性大小的标准:以氟的电负性为4.0作为相对标准。
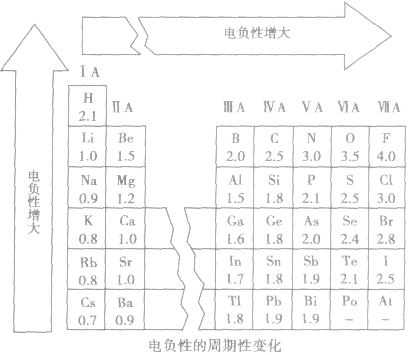
(4)电负性的变化规律
①随原子序数的递增,元素的电负性呈周期性变化。
②同周期,从左到右,元素的电负性逐渐变大。
③同主族,从上到下,元素的电负性逐渐变小。
电负性的应用:
①判断元素的金属性和非金属性的强弱
金属的电负性一般小于1.8,非金属的电负性一般大于1.8,而位于非金属三角区边界的“类金属”(如锗、锑等)的电负性则在1.8左右,它们既有金属性,又有非金属性。
②判断元素化合价的正负
利用电负性可以判断化合物中元素化合价的正负:电负性大的元素易呈现负价,电负性小的元素易呈现正价。
③判断化学键的类型
一般认为,如果成键原子所属元素的电负性差值大于 1.7,它们之间通常形成离子键;如果成键原子所属元素的电负性差值小于1.7,它们之间通常形成共价键。
④解释“对角线规则”
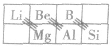
在元素周期表中,某些主族元素与其右下方的主族元素(如右图所示)的有些性质是相似的,被称为“对角线规则”。例如:硼和硅的含氧酸盐都能形成玻璃且互熔,含氧酸都是弱酸等。
定义:
直接相邻原子间均以共价键相结合的化合物。共价化合物中只含共价键。
离子化合物和共价化合物的比较:

直接相邻原子间均以共价键相结合的化合物。共价化合物中只含共价键。
离子化合物和共价化合物的比较:

定义:
含有离子键的化合物称为离子化合物,离子化合物中肯定存在离子键,也可以存在共价键。
含有离子键的化合物称为离子化合物,离子化合物中肯定存在离子键,也可以存在共价键。
发现相似题
与“已知元素的电负性和元素的化合价一样,也是元素的一种基本性...”考查相似的试题有:
- 元素电负性随原子序数的递增而增强的是[ ]A.Na, K, RbB.N, P, AsC.O, S, ClD.Si, P, Cl
- 四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y 原子的L层p轨道中有2个电...
- 有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数,C原子最外层中有2个不...
- 不同元素的原子在分子内吸引电子的能力大小可用电负性来表示,电负性越大,其原子吸引电子的能力越强,在所形成的分子中成为...
- 下面的叙述正确的是[ ]A.两种非金属元素原子之间形成的化学键不一定都是极性键B.共价化合物中可能含有离子键C.只要是离子...
- 下列说法中正确的是[ ]A.共价化合物中一定不含有离子键B.离子化合物中一定不含有共价键C.失电子难的粒子获得电子的能力不...
- 下列叙述正确的是( ) A.凡是能电离出离子的化合物都是离子化合物 B.含有共价键的化合物都是共价化合物 C.Na2O溶于水时只...
- 已知元素电负性的差值大于1.7时,原子间形成离子键,小于1.7时,原子间形成共价键,请指出下列原子之间形成的化学键是离子键...
- 下列说法正确的是( ) A.共价化合物中可能含有离子键 B.离子化合物中一定没有共价键 C.分子晶体中一定有共价键 D.原子晶...
- 下列说法正确的是[ ]A.含有离子键的化合物必是离子化合物B.含有共价键的物质就是共价化合物C.共价化合物可能含有离子键D....