本试题 “KMnO4溶液常用作氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中的某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配...” 主要考查您对质量守恒定律
阿伏加德罗定律
晶体、非晶体
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 质量守恒定律
- 阿伏加德罗定律
- 晶体、非晶体
质量守恒定律:
参加化学反应的各物质质量总和等于反应后生成的各物质质量总和。
化学反应前后,各种原子种类、数目、质量都不改变。
任何变化包括化学反应和核反应都不能消除物质,只是改变了物质的原有形态或结构,所以该定律又称物质不灭定律。
质量守恒定律的本质:
原子是物质质量的最小承担者。故在化学反应中,只要各种原子总数保持不变,则总质量保持不变。所以,质量守恒定律也就等价于元素守恒。
质量守恒定律的适用范围:
①质量守恒定律适用的范围是化学变化而不是物理变化;
②质量守恒定律揭示的是质量守恒而不是其他方面的守恒。物体体积不一定守恒;
③质量守恒定律中“参加反应的”不是各物质质量的简单相加,而是指真正参与了反应的那一部分质量,反应物中可能有一部分没有参与反应;
④质量守恒定律的推论:化学反应中,反应前各物质的总质量等于反应后各物质的总质量
质量守恒定律的应用:
(1)根据质量守恒定律,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。利用这一定律可以解释反应前后物质的质量变化及用质量差确定某反应物或生成物的质量。
(2)根据质量守恒定律,化学反应前后元素的种类和质量不变,由此可以推断反应物或生成物的组成元素。
(3)据质量守恒定律:化学反应前后元素的种类和数目相等,推断反应物或生成物的化学式。
(4)已知某反应物或生成物质量,根据化学方程式中各物质的质量比,可求出生成物或反应物的质量。
阿伏伽德罗定律:
同温同压下,相同体积的任何气体含有相同的分子数。
阿伏伽德罗定律的使用范围:
阿伏伽德罗定律只对气体起作用,使用于任何气体,包括混合气体。
方法与技巧:
- “三同”定“一同”(温度、压强、气体体积、气体分子数);“两同”定“比例”。
- 阿伏伽德罗定律及其推论的数学表达式可由理想气体状态方程(PV=nRT)或其变形形式(PM=ρRT)推出,不用死记硬背。
理想气体状态方程:
理想气体状态方程的表达式:PV= nRT
P表示压强,V 表示体积,T表示温度,R是常数,n是气体的物质的量。
可根据此方程来推断阿伏伽德罗定律的相关推论:
| 条件 | 结论 | 语言表达 |
| T、P相同 | n1/n2=V1/V2 | 同温同压下,气体的分子数与其体积成正比 |
| T、V相同 | n1/n2=P1/P2 | 同温同体积,压强与其分子数成正比 |
| n、P相同 | V1/V2=T1/T2 | 分子数、压强相同的气体,体积与温度成正比 |
| n、T相同 | P1/P2= V2/V1 | 分子数、温度相同的气体,压强与体积成反比 |
| T、P相同 | ρ1/ρ2=M1/M2 | 同温同压下,气体的密度与相对分子质量(摩尔质量)成正比 |
| T、P、V相同 | m1/m2=M1/M2 | 同温同压下,相同体积的气体,质量与其相对分子质量成正比 |
| T、P、m相同 | M1/M2=V2/V1 | 同温同压下,等质量的气体,相对分子质量与其体积成反比 |
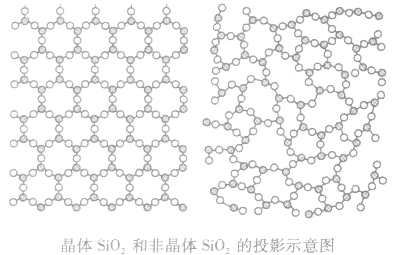
晶体与非晶体:
| 晶体 | 非晶体 | |
| 微观结构 | 原子在三维空间里呈周期性有序排列 | 原子排列相对无序 |
| 实例 | 白磷、硫黄、固态碘、高锰酸钾、干冰、金刚石、金属铜等绝大多数常见的固体 | 玻璃、石蜡、沥青等固体 |
| 自范性 | 有(能自发呈现封闭的、规则的多面体外形) | 无 |
| 各向异性 | 有(晶体在不同的方向上表现出不同的物理性质) | 无 |
| 对称性 | 有 | 无 |
| 熔点 | 固定 | 不固定 |
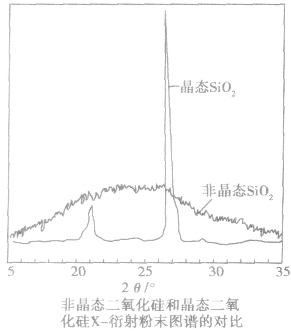
| 鉴别方法 | 对固体进行X一射线衍射实验。当单一波长的 X一射线通过晶体时,会在记录仪上看到分立的斑点或谱线 | |
与“KMnO4溶液常用作氧化还原反应滴定的标准液,由于KMnO4的强氧...”考查相似的试题有:
- 下列化学用语的表示正确的是( )A.乙酸的分子式:C2H402B.乙醇的结构简式:C2H60C.F原子结构示意图:D.四氯化碳的电子式:
- 水在下列各反应中扮演的角色不同,其中水只做还原剂的是A.2Na2O2+ 2H2O=4NaOH + O2↑B.2F2+ 2H2O=4HF + O2C.2Na+2H2O==2N...
- 下列有关物质的表达式正确的是A.1,3—丁二烯的分子式:C4H8B.溴乙烷的电子式:C.乙醇的结构简式:CH3CH2OHD.乙炔的分子模...
- 下列应用不涉及氧化还原反应的是A.工业上利用N2和H2合成氨,实现人工固氮B.实验室用NH4Cl和Ca(OH)2制备NH3C.用FeCl3溶液作...
- 雷雨天闪电时空气中有臭氧O3生成,下列说法正确的是[ ]A.O2和O3互为同位素B.O2和O3相互转化属于物理变化C.在相同的温度和...
- 今年我国“天宫一号”空间实验室将与“神舟”载人飞船实现对接。飞船升空所需的巨大能量可由下列化学反应提供:。有关该反应的说...
- 下列说法中错误的是( )A.凡是氧化还原反应,都不可能是复分解反应B.化合反应不可能是氧化还原反应C.置换反应一定是氧化...
- 同温同压下,已知O2的密度为ρ g/L,则NH3的密度为( )A.17ρ32g/LB.32ρ17g/LC.3217ρg/LD.1732ρg/L
- A.离子晶体中,一定存在离子键B.原子晶体中,只存在共价键C.金属晶体的熔沸点均很高D.稀有气体的原子能形成分子晶体
- H2O2可以作为脱氯剂,反应方程式为:H2O2+Cl2==2HCl+O2,下列说法错误的是( )A.该反应为置换反应B.生成1mol O2需转移电子...