本试题 “研究发现,空气中少量的NO2能参与硫酸型酸雨的形成,反应过程如下:①SO2+NO2→SO3+NO ②SO3+H2O→H2SO4③2NO+O2→2NO2NO2在上述过程中的作用,与H2SO4在下列变化中...” 主要考查您对三氧化硫
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 三氧化硫
三氧化硫:
分子式:SO3,是含极性键的非极性分子,固态时为分子晶体。
三氧化硫的物理性质和化学性质:
1.物理性质:无色易挥发的晶体,熔点为16.8℃,沸点为44.8℃,易升华。
2.化学性质:SO3表现出酸性氧化物的通性。
(1)与水反应: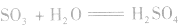 ,SO3遇水剧烈反应生成硫酸,同时放出大量的热,三氧化硫是硫酸的酸酐,又叫硫酐。
,SO3遇水剧烈反应生成硫酸,同时放出大量的热,三氧化硫是硫酸的酸酐,又叫硫酐。
(2)与碱反应:

(3)与碱性氧化物反应:
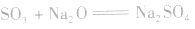
3.SO3的制法:
发现相似题
与“研究发现,空气中少量的NO2能参与硫酸型酸雨的形成,反应过程...”考查相似的试题有:
- 用下列装置可测定SO2转化为SO3的转化率。 (1)根据实验的需要,(Ⅰ)(Ⅱ)(Ⅲ)处应连接合适的装置。请从下面装置中选择合适...
- 下列说法中,正确的是( )A.亚硫酸钠溶液中加入氯化钡溶液后产生白色沉淀,再加稀盐酸沉淀不消失B.正常雨水的pH等于7,pH...
- 下列关于硫酸性质的描述中,正确的是A.浓H2SO4有氧化性,稀H2SO4无氧化性B.由于浓H2SO4具有吸水性,故可用来与蔗糖反应做“...
- 硫酸在生产中有广泛的应用,某厂以硫铁矿为主要原料生产硫酸。已知:①550℃时, ②一定温度下,硫铁矿在空气中煅烧可能发生下列...
- 下列有关SO2的性质的探究实验报告记录的实验现象正确的是( )
- X(盐)和Y(酸)反应,可放出有气味的气体Z;Z跟NaOH反应又得到X(盐);Z氧化的最终产物为W,W溶于水又得到Y(酸).则X(盐)和Y(酸)是A....
- (6分)指出硫酸在下列用途或反应中表现的性质A.高沸点B.强酸性C.吸水性D.脱水性E.强氧化性F.催化作用(填序号)(1)实...
- 下列离子方程式中,正确的是( )A.金属钠与冷水反应:Na+2H2O====Na++2OH-+H2↑B.碳酸钙投入醋酸溶液中CaCO3+2CH3COOH====C...
- 直接排放含SO2,的烟气会形成胶雨,危害环境。利用钠碱循环法可脱除烟气中的SO2(1)在钠碱循环法中,Na2SO3溶液作为吸收液,...
- 近年来,酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。(1)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,流程...