本试题 “下列推论正确的是[ ]A.S(g)+O2(g)=SO2(g) △H1,S(s)+O2(g)=SO2(g) △H2;则:△H1>△H2B.C(石墨,s)=C(金刚石,s) △H=+1.9kJ/mol,则:由石墨制取金刚石的反...” 主要考查您对吸热反应、放热反应
焓变、反应热
化学反应进行的方向
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 吸热反应、放热反应
- 焓变、反应热
- 化学反应进行的方向
吸热反应:
吸收热量的反应,即生成物的总能量大于反应物的总能量,反应需要吸收能量
放热反应:
放出热量的反应,即生成物的总能量小于反应物的总能量,反应释放出能量
放热反应和吸热反应的比较:
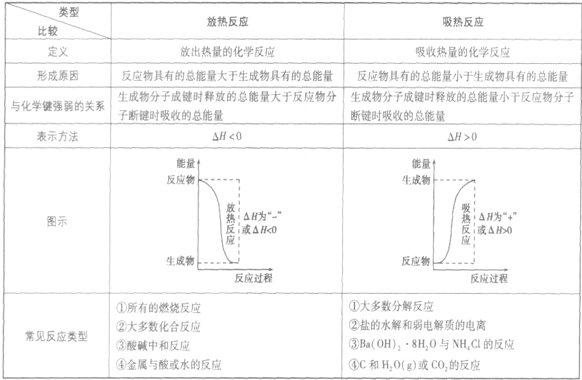
吸收热量的反应,即生成物的总能量大于反应物的总能量,反应需要吸收能量
放热反应:
放出热量的反应,即生成物的总能量小于反应物的总能量,反应释放出能量
放热反应和吸热反应的比较:

反应热,焓变:
化学能可以转化为热能、电能和光能等,化学反应中的能量变化,通常主要表现为热量的变化。
1.定义:在化学反应过程中,当生成物和反应物具有相同温度时所放出或吸收的热量,通常叫做化学反应的反应热。在恒温、恒压条件下,化学反应过程中吸收或放出的热量称为反应的焓变。
2.符号:△Ⅳ
3.单位:kJ·mol-1
4.产生原因:化学反应过程中旧键断裂吸收的总能量与新键形成释放的总能量不相等,故化学反应均伴随着能量变化——吸热或放热。
5.表示方法:放热反应的△H<0,吸热反应的△H>0.
化学能可以转化为热能、电能和光能等,化学反应中的能量变化,通常主要表现为热量的变化。
1.定义:在化学反应过程中,当生成物和反应物具有相同温度时所放出或吸收的热量,通常叫做化学反应的反应热。在恒温、恒压条件下,化学反应过程中吸收或放出的热量称为反应的焓变。
2.符号:△Ⅳ
3.单位:kJ·mol-1
4.产生原因:化学反应过程中旧键断裂吸收的总能量与新键形成释放的总能量不相等,故化学反应均伴随着能量变化——吸热或放热。
5.表示方法:放热反应的△H<0,吸热反应的△H>0.
化学反应的方向与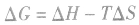 :
:
1.化学反应进行方向的判据
(1)由稳定性弱的物质向稳定性强的物质转变
如 ,稳定性
,稳定性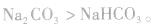
(2)离子反应总是向着使反应体系中某些离子浓度减小的方向进行
①溶解度大的物质向溶解度小的物质转变,如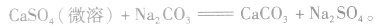
②由相对强酸(碱)向相对弱酸(碱)转变,如 ,
,  所以酸性强弱:
所以酸性强弱: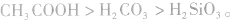
(3)由难挥发性物质向易挥发性物质转变
如 所以沸点:
所以沸点: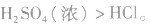
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质转变
如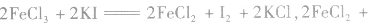
 ,则氧化性:
,则氧化性: 。
。
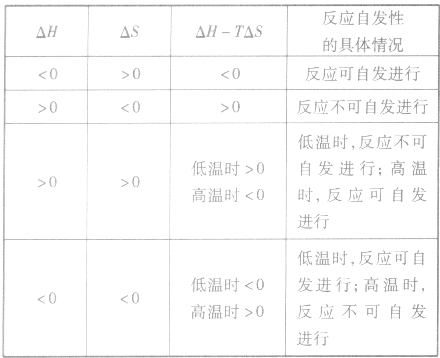
2.焓变和熵变共同判断反应的方向:
在温度、压强一定的条件下,自发反应总是向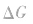
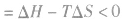 的方向进行,直至达到平衡状态;
的方向进行,直至达到平衡状态;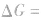
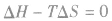 表明反应已达到平衡状态;
表明反应已达到平衡状态;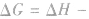
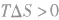 表明反应不能自发进行。
表明反应不能自发进行。
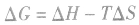 :
:1.化学反应进行方向的判据
(1)由稳定性弱的物质向稳定性强的物质转变
如
 ,稳定性
,稳定性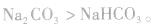
(2)离子反应总是向着使反应体系中某些离子浓度减小的方向进行
①溶解度大的物质向溶解度小的物质转变,如
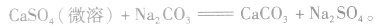
②由相对强酸(碱)向相对弱酸(碱)转变,如
 ,
,  所以酸性强弱:
所以酸性强弱: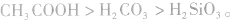
(3)由难挥发性物质向易挥发性物质转变
如
 所以沸点:
所以沸点: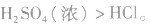
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质转变
如
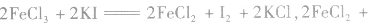
 ,则氧化性:
,则氧化性: 。
。 2.焓变和熵变共同判断反应的方向:
在温度、压强一定的条件下,自发反应总是向
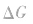
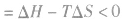 的方向进行,直至达到平衡状态;
的方向进行,直至达到平衡状态;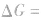
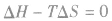 表明反应已达到平衡状态;
表明反应已达到平衡状态;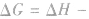
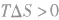 表明反应不能自发进行。
表明反应不能自发进行。
发现相似题
与“下列推论正确的是[ ]A.S(g)+O2(g)=SO2(g) △H1,S(s)+O2(g)=S...”考查相似的试题有:
- 下列反应中,属于吸热反应的是[ ]A.生石灰与水作用制熟石灰B.氯化铵与氢氧化钡晶体反应C.燃烧木炭取暖D.炸药爆炸
- SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:(1)反应2NO+2CO2CO2+N2能够自发进行,则该反应的ΔH ...
- 已知反应:①Al+Fe2O3Al2O3+Fe △H=a kJ/mol②101kPa时,2C(s)+O2(g)=2CO(g)△H=-221 kJ/mol③稀溶液中,H+(aq)+OH-(aq)...
- 有下列因素:①反应物的多少②反应进行的快慢③反应物和生成物的状态④反应进行的途径其中对某化学反应的反应热的大小有影响的因...
- 分析能量变化示意图,下列选项正确的是A.S(s,单斜)+O2(g)=SO2(g)△H ="+297.16" kJ•mol-1B.S(s,单斜)+O2(g)=SO2...
- 工业上利用CO和水蒸气在一定条件下发生反应制取氢气:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=-41kJ/mol某小组研究在相同温度下...
- 在25 ℃、101 kPa时,CH4(g)、H2(g)、C(s)的燃烧热分别是-890.3 kJ·mol-1、-285.8 kJ·mol-1和-393.5 kJ·mol-1,则CH4(g)...
- 下列说法正确的是( )A.任何化学反应不一定都有反应热B.能源是提供能量的资源,它包括化石燃料(煤、石油、天然气),不包...
- 过程的自发性的作用是[ ]A.判断过程的方向B.确定过程是否一定会发生C.判断过程发生的速率D.判断过程的热效应
- 高炉炼铁中常用焦炭还原Fe2O3。请运用所学知识判断用焦炭还原Al2O3炼制金属铝的可能性。已知298K时反应:3C(s)+2Al2O3(s)==...