本试题 “某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等。(1)氯气可以用于漂白、消毒的原...” 主要考查您对氯气用于自来水消毒杀菌
漂白粉、漂粉精
氯气
次氯酸
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氯气用于自来水消毒杀菌
- 漂白粉、漂粉精
- 氯气
- 次氯酸
氯气的基本用途:
①消毒。(自来水常用氯气消毒,1L水里约通入0.002g氯气,消毒原理是其与水反应生成了次氯酸,它的强氧化性能杀死水里的病菌。而之所以不直接用次氯酸为自来水杀菌消毒,是因为次氯酸易分解难保存、成本高、毒性较大,则用氯气消毒可使水中次氯酸的溶解、分解、合成达到平衡,浓度适宜,水中残余毒性较少。)
②制盐酸。
③工业用于制漂白粉或漂粉精。
④制多种农药。(如六氯代苯,俗称666。)
⑤制氯仿等有机溶剂。
⑥制塑料(如聚氯乙烯塑料)等Cl?可用来制备多种消毒剂,含Cl的消毒剂有ClO?,NaClO,Ca(ClO)?。
⑦常用于将FeCl?氧化成FeCl?
⑧工业用于海水提溴(Cl?+2NaBr==Br?+2NaCl)
漂白粉,漂白精:
主要成分是次氯酸钙,工业上通过氯气与石灰乳作用制成的。2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O,在潮湿的空气里,次氯酸钙与空气中的二氧化碳和水蒸气反应,生成次氯酸。所以漂粉精、漂白粉也具有漂白、消毒作用。
主要成分是次氯酸钙,工业上通过氯气与石灰乳作用制成的。2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O,在潮湿的空气里,次氯酸钙与空气中的二氧化碳和水蒸气反应,生成次氯酸。所以漂粉精、漂白粉也具有漂白、消毒作用。
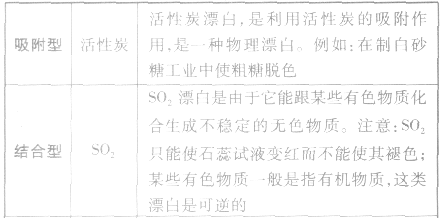
具有漂白作用的物质总结:

氯气:
①化学式:Cl2
②氯元素在周期表中的位置:第三周期ⅦA族
③氯原子的电子式: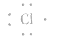
④氯的原子结构示意图: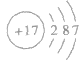
⑤氯原子的外围电子排布式:
⑥化学键类型:非极性共价键
⑦氯分子的电子式:
⑧氯分子的结构式:
氯气的物理性质和化学性质:
(1)物理性质:黄绿色,有刺激性气味,有毒,密度比空气大,能溶于水(1:2)。
(2)化学性质:氯气(Cl2)是双原子分子,原子的最外层有七个电子,是典型的非金属元素,单质是强氧化剂。
①氯气与金属反应: 2Na+Cl2
 2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2
2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2 2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2
2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2 CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。
CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。 ②与非金属的反应 H2+Cl2
 2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2
2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2 2HCl(发生爆炸) 2P+3Cl2
2HCl(发生爆炸) 2P+3Cl2 2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。
2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。 ③与碱反应 Cl2+2NaOH==NaCl+NaClO+H2O 2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
④与某些还原性物质反应:Cl2+2FeCl2===2FeCl3 Cl2+SO2+2H2O==2HCl+H2SO4
⑤有机反应(参与有机反应的取代和加成反应)
CH4+Cl2→CH3Cl+HCl
CH3Cl+Cl2→CH2Cl2+HCl
CH2Cl2+Cl2→CHCl3+HCl
CHCl3+Cl2→CCl4+HCl
Cl2+CH2=CH2→CH2Cl-CH2Cl(加成反应)
⑥与水反应 Cl2+H2O
 HCl+HClO
HCl+HClO 次氯酸:
化学式HClO,结构式H-O-Cl,仅存在于溶液中,浓溶液呈黄色,稀溶液无色,有非常刺鼻的气味,极不稳定,是很弱的酸,比碳酸弱,和氢硫酸相当。有很强的氧化性和漂白作用,它的盐类可用做漂白剂和消毒剂。
次氯酸盐的性质:
1.水解:
2.强氧化性:如与Fe2+反应
酸性条件下,不能与ClO-大量共存的有Fe2+、S2-、HS-、SO32-、I-等
3.与酸反应,如与稀盐酸反应
漂白粉漂白的原理: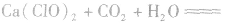
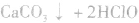 ,HClO具有强氧化性,漂白剂不用氯水,而是用Cl2制成漂白粉的原因是便于贮存运输。
,HClO具有强氧化性,漂白剂不用氯水,而是用Cl2制成漂白粉的原因是便于贮存运输。
发现相似题
与“某校高一化学研究性学习小组对日常生活中的氯气用途进行了调...”考查相似的试题有:
- 某同学用10mol• L-1的浓盐酸配制250mL 1mol• L-1的稀盐酸,并进行有关实验。请回答下列问题:(1)需要量取浓盐酸 mL。(2)...
- 四支试管分别充满O2、NO2、Cl2、NH3四种气体,把它们分别倒立于盛有下列各种液体的水槽中,发生的现象如图所示,其中充满Cl2的试...
- 溴、碘主要存在于海水中,有“海洋元素”的美称.海水中的碘富集在海藻中,我国海带产量居世界第一,除供食用外,大量用于制碘...
- 浓盐酸和Ca(ClO)2能发生如下反应:Ca(ClO)2+4HCl(浓)= CaCl2+2Cl2↑+2H2O,用贮存很久的漂白粉与浓盐酸反应制得的氯气中可能含...
- 工业上获得有关物质的方法或途径正确的是[ ]A.将氯气通入澄清石灰水,获得漂白粉B.工业上,用SiO2+2CSi+2CO↑制得粗硅C.钠...
- 用氯气消毒的自来水配制下列溶液时,会使配制的溶液变质的是( )①NaOH ②AgNO3 ③Na2CO3 ④KI ⑤FeCl2A.只有②④B.只有④⑤C.只...
- 下列物质中,不能通过氯气与单质直接化合制取的是( )A.NaClB.CuCl2C.FeCl2D.HCl
- agH2和bgCl2混合点燃反应后,将反应后所得的气体通入足量NaOH溶液中,求(1)通入NaOH溶液后,可能剩余的气体的质量。(2)溶...
- 某化学小组用下列装置抽取收集纯净的氯气,并研究其性质。请回稳下列问题。(1)装置A中发生反应的离子方程式为_____________...
- 下列实验现象和结论一致,正确的是A.氯水加入有色布条,有色布条褪色,说明溶液中有Cl2存在B.氯水溶液呈黄绿色,有刺激性气...