本试题 “下列各组物质的分类或相互关系,正确的是( )A.同位素:金刚石、石墨、C60B.含极性键的分子:CO2、CCl4、NH3C.非电解质:Cl2、NH3、C2H5OHD.同系物:、、” 主要考查您对同位素
极性键、非极性键
电解质、非电解质
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 同位素
- 极性键、非极性键
- 电解质、非电解质
定义:
质子数相同而中子数不同的原子互称为同位素(即同一元素的不同核素互称为同位素)。元素符号表示不同,如 ;电子结构相同,原子核结构不同;物理性质不同,化学性质相同。
;电子结构相同,原子核结构不同;物理性质不同,化学性质相同。
同位素的应用:
(1)同位素在医学领域中的应用最为广泛,主要用于显像、诊断和治疗,还用于医疗用品消毒、药物作用机理研究和生理医学研究等。
(2)同位素辐射育种技术为农业提供了改进农产品质量、增加产量的新技术;利用同位素示踪技术,可检测并确定植物的最佳肥料吸入量和农药吸入量。
(3)14C纪年测定法与其他放射性同位素测定法已成为地质学、考古学、人类学、地球科学等领域广泛采用的一种准确的断代方法。
极性键和非极性键:
(1)非极性键:同种元素的原子间形成的共价键(共用电子对不偏移,成键原子双方不显电性)。
如:在非金属单质(H2 Cl2 O2)、共价化合物(H2O2 多碳化合物)、离子化合物(Na2O2 CaC2)中存在。
(2)极性键:不同元素的原子间形成的共价键(共用电子对偏向吸引电子能了强的一方,该元素显负价,偏离吸引电子能力弱的一方,该元素显正价)。如:在共价化合物(HCl H2O CO2 NH3)、某些离子化合物(NaOH Na2SO4 NH4Cl)中存在。
(1)非极性键:同种元素的原子间形成的共价键(共用电子对不偏移,成键原子双方不显电性)。
如:在非金属单质(H2 Cl2 O2)、共价化合物(H2O2 多碳化合物)、离子化合物(Na2O2 CaC2)中存在。
(2)极性键:不同元素的原子间形成的共价键(共用电子对偏向吸引电子能了强的一方,该元素显负价,偏离吸引电子能力弱的一方,该元素显正价)。如:在共价化合物(HCl H2O CO2 NH3)、某些离子化合物(NaOH Na2SO4 NH4Cl)中存在。
分子空间构型、键的极性与分子的极性:

化学键与物质类别:
1.只含有极性共价键的物质:一般是不同非金属元素构成的共价化合物。例如: 等。
等。
2.只含非极性共价键的物质:同种非金属元素构成的单质。例如: 、金刚石等。
、金刚石等。
3.既有极性键又有非极性键的物质。例如: 等。
等。
4.只含有离子键的物质:活泼非金属元素与活泼金属元素形成的化合物。例如: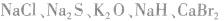 等。
等。
5.既有离子键又有非极性键的物质。例如: 等。
等。
6.既有离子键又有极性键的物质。例如: 等。
等。
7.由离子键、共价键、配位键构成的物质。例如: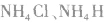 等。
等。
8.只含有共价键而无范德华力的物质。例如:金刚石、晶体硅、 等原子晶体。
等原子晶体。
9.由强极性键构成但又不是强电解质的物质。例如:HF。
10.没有化学键的物质。例如:稀有气体(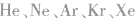 等)。
等)。
电解质和非电解质:
1.电解质和非电解质在水溶液里或熔融状态下能导电的化合物,叫做电解质。在水溶液里和熔融状态下都不导电的化合物,叫做非电解质。
2.电解质和非电解质的比较

说明(1)电解质、非电解质均是化合物。
(2)电解质导电必须有外界条件:水溶液或熔融状态。
(3)电解质是一定条件下本身电离而导电的化合物。CO2、SO2、SO3、NH3溶于水后也导电,但是与水反应生成的新物质电离而导电的,不是本身电离而导电的,故属于非电解质。
(4)电解质的强弱由物质的内部结构决定,与其溶解度无关。某些难溶于水的化合物,如BaSO4、AgCl,虽然溶解度很小,但溶解的部分是完全电离的,所以是强电解质。
(5)电解质不一定导电,非电解质一定不导电;导电的物质不一定是电解质,不导电的物质不一定是非电解质。
1.电解质和非电解质在水溶液里或熔融状态下能导电的化合物,叫做电解质。在水溶液里和熔融状态下都不导电的化合物,叫做非电解质。
2.电解质和非电解质的比较

说明(1)电解质、非电解质均是化合物。
(2)电解质导电必须有外界条件:水溶液或熔融状态。
(3)电解质是一定条件下本身电离而导电的化合物。CO2、SO2、SO3、NH3溶于水后也导电,但是与水反应生成的新物质电离而导电的,不是本身电离而导电的,故属于非电解质。
(4)电解质的强弱由物质的内部结构决定,与其溶解度无关。某些难溶于水的化合物,如BaSO4、AgCl,虽然溶解度很小,但溶解的部分是完全电离的,所以是强电解质。
(5)电解质不一定导电,非电解质一定不导电;导电的物质不一定是电解质,不导电的物质不一定是非电解质。
发现相似题
与“下列各组物质的分类或相互关系,正确的是( )A.同位素:金...”考查相似的试题有:
- 下列互称为同位素的是( ) A.202Pt和198Pt B.CO和CO2 C.O2和O3 D.H2O和D2O
- 下列晶体中,化学键种类相同、晶体类型也相同的是[ ]A.SO2与SiO2B.CO2与H2OC.C与HClD.CCl4与SiC
- 下列叙述中,错误的是[ ]A.离子化合物中可能含有非极性键B.分子晶体中的分子内不含有离子键C.原子晶体中可能含有非极性键D...
- 下列物质中,只含有非极性共价键的是[ ]A.H2O2B.I2C.CaC12D.NaOH
- 盛有一向定量的Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)近似的用下图中的曲...
- 下列物质不属于电解质的是( )A.固体氢氧化钠B.冰水混合物C.无水酒精D.氯化钠晶体
- 下列属于电解质并能导电的物质是( )A.熔融的NaClB.KNO3溶液C.干冰D.金属铝
- 下列物质中:(用序号填空)①氯化镁 ②氢氧化钠溶液 ③熔融硝酸钾 ④醋酸 ⑤钠 ⑥氨气 ⑦乙醇 ⑧氯化银 ⑨氢氧化铝 ⑩二氧化碳(1)属...
- 下列物质中属于电解质的是( )A.蔗糖B.金属铝C.碳酸钠D.氨水
- 下列物质属于电解质的是 ( )①NaOH ②BaSO4 ③Cu ④蔗糖 ⑤CO2A.①②B.①②⑤C.③④D.①⑤