本试题 “维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量可通过在弱酸性溶液中用已知溶液的I2溶液进行滴定。该反应的化学方...” 主要考查您对弱电解质的电离
氧化还原反应的计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 弱电解质的电离
- 氧化还原反应的计算
定义:
在一定温度、浓度的条件下,弱电解质在溶液中电离成离子的速率与离子结合成分子的速率相等时,电离过程就到了电离平衡状态,叫弱电解质的电离平衡。

电离平衡的特征:
(1)等:
(2)动: 的动态平衡
的动态平衡
(3)定:条件一定,分子与离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。
在一定温度、浓度的条件下,弱电解质在溶液中电离成离子的速率与离子结合成分子的速率相等时,电离过程就到了电离平衡状态,叫弱电解质的电离平衡。

电离平衡的特征:
(1)等:

(2)动:
 的动态平衡
的动态平衡(3)定:条件一定,分子与离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。
氧化还原反应的计算:
(1)比较典型的计算有:求氧化剂、还原剂物质的量之比或质量比,计算参加反应的氧化剂货还原剂的量,确定反应前后某一元素的价态变化等。
(2)计算的依据是:氧化剂得电子数等于还原剂失电子数,列出守恒关系式求解。
(1)比较典型的计算有:求氧化剂、还原剂物质的量之比或质量比,计算参加反应的氧化剂货还原剂的量,确定反应前后某一元素的价态变化等。
(2)计算的依据是:氧化剂得电子数等于还原剂失电子数,列出守恒关系式求解。
氧化还原反应的基本规律:
1.守恒规律
氧化还原反应中有物质失电子必有物质得电子,且失电子总数等于得电子总数。或者说氧化还原反应中,有元素化合价升高必有元素化合价降低,且化合价升高总数必等于降低总数。有关得失电子守恒(化合价守恒)的规律有如下应用:
(1)求某一反应中被氧化与被还原的元素原子个数之比,或求氧化剂与还原剂的物质的量之比及氧化产物与还原产物的物质的量之比。
(2)配平氧化还原反应方程式。
(3)进行有关氧化还原反应的计算:
2.强弱规律
较强氧化性的氧化剂跟较强还原性的还原剂反应,生成弱还原性的还原产物和弱氧化性的氧化产物。应用:在适宜条件下,用氧化性较强的物质制备氧化性较弱的物质,或用还原性较强的物质制备还原性较弱的物质,也可用于比较物质间氧化性或还原性的强弱。
3.价态规律
元素处于最高价,只有氧化性;元素处于最低价,只有还原性;元素处于中间价态,既有氧化性又有还原性,但主要表现一种性质。物质若含有多种元素,其性质是这些元素性质的综合体现。
4.转化规律
氧化还原反应中,以元素相邻价态之间的转化最容易;不同价态的同种元素之间发生反应,元素的化合价只靠近,不交叉;相邻价态的同种元素之间不发生氧化还原反应。如

5.难易规律
越易失去电子的物质,失去后就越难得到电子;越易得到电子的物质,得到后就越难失去电子。一种氧化剂同时和几种还原剂相遇时,还原性最强的优先发生反应;同理,一种还原剂同时与多种氧化剂相遇时,氧化性最强的优先发生反应,如向FeBr2溶液中通入Cl2时,发生离子反应的先后顺序为:
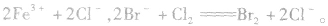 。
。
发现相似题
与“维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,...”考查相似的试题有:
- 对常温下pH=3的CH3COOH溶液,下列叙述不正确的是A.B.加入少量CH3COONa固体后,c(CH3COO—)降低C.该溶液中由水电离出的c(...
- A.2c(Na+)+c(H+)====c(S2-)+c(HS-)+c(OH-)B.c(Na+)+c(H+)====2c(S2-)+c(HS-)+c(OH-)C.c(H+)+c(HS-)+2...
- (9分)完成以下小题:(1)已知NaHSO3溶液显酸性,则溶液中各离子浓度从大到小的顺序是 。(2)25℃时,向pH=4的NaHSO4溶液中...
- 甲、乙两瓶稀氨水的浓度分别是1mol/L和0.1mol/L,则甲、乙两瓶氨水中c(OH—)之比为A.大于10B.小于10C.等于10D.无法确定
- 下列操作中,能使电离平衡H2O⇌H++OH-向右移动且溶液呈碱性的是( )A.向水中通入氨气B.向水中加入Al2(SO4)3溶液C.向水中...
- 250C时,0.1mol·L-1稀醋酸加水稀释,如图中的纵坐标y可以是( )A.溶液的pHB.醋酸的电离平衡常数C.溶液的导电能力D.醋酸...
- 等体积,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液、②HSCN溶液、③NaHCO3溶液,已知将①、②分别与③混合,实验测得产生的CO2气...
- 若不慎发生砒霜泄露,应急的措施是采用石灰中和,使被污染的河水含砷量降低到国家允许的标准范围内,以消除可能会造成的危害...
- 向50 mL 18 mol/L的H2SO4溶液中加入足量的铜片,加热使之反应。充分反应后,被还原的H2SO4的物质的量[ ]A.小于0.45 molB.等...
- 下列说法正确的是[ ]A. 金属Cu与人体分泌的盐酸及体内的空气可反应生成一种弱酸超氧酸HO2,反应方程式如下:Cu+HCl+O2==CuCl+...