本试题 “下列说法错误的是[ ]A.顺-2-丁烯和反-2-丁烯分别与H2加成,生成相同的加成产物B.(CH3)3CCl和(CH3)2CHCH2Cl分别与NaOH的乙醇溶液共热,生成相同的消去产物C...” 主要考查您对烯烃的通性
卤代烃
同分异构体
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 烯烃的通性
- 卤代烃
- 同分异构体
烯烃的通性:
(1)物理性质:随着分子中碳原子数的递增,熔沸点逐渐升高,相对密度逐渐增大,常温下存在状态,由气态逐渐过渡到液态、固态。
(2)化学性质:烯烃可发生氧化、加成、加聚等反应。
①烯烃的氧化反应:烯烃燃烧生成二氧化碳和水。CnH2n+3n/2O2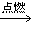 nCO2+nH2O
nCO2+nH2O
②烯烃的加成:烯烃可与氢气、卤素单质、水、卤化氢等发生加成反应。烯烃的加聚反应:以乙烯为例: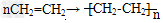 ,加聚时碳碳双键打开。
,加聚时碳碳双键打开。
③二烯烃的加成反应:以1,3-丁二烯(CH2=CH-CH=CH2)加成为例
1,2加成就是加成普通的不饱和键,和普通的烯烃和炔烃的加成一样。与氯气加成:CH2=CH-CH=CH2+Cl2→CH2Cl-CHCl-CH=CH2
1,4加成,1,4加成是分别加成两边的2个不饱和键,然后在中间重新形成一个双键。与氯气加成:CH2=CH-CH=CH2+Cl2→CH2Cl-CH=CHCH2Cl
(3)烯烃的顺反异构:根据在两个由双键连接的碳原子上所连的四个原子或基团中两个相同者的位置来决定异构体的类型。当两个相同的原子或基团处于π键平面的同侧时称“顺式异构(cis-isomerism)”;当处于π键平面的异侧时称“反式异构(trans-isomerism)”。Z表示顺,E表示反。 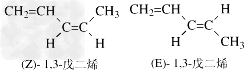
卤代烃:
1.卤代烃的定义
烃分子中的氢原子被卤素原于取代后生成的化合物,称为卤代烃,可用R—X(X为卤素原子)表示。在卤代烃分子中,卤素原子是官能团。由于卤素原子吸引电子的能力较强,使共用电子对偏移,c—x键具有较强的极性,因此卤代烃的反应活性增强。
2.卤代烃的分类 (1)根据分子中所含卤素原子种类的不同,分为氟代烃、氯代烃、溴代烃和碘代烃。
(2)根据分子中所含卤素原子个数的不同,分为一卤代烃和多卤代烃。
(3)根据烃基结构不同,分为卤代烷烃、卤代烯烃、卤代芳香烃等。
卤代烃的性质:
1.卤代烃的物理性质
(1)常温下,卤代烃中除一氯甲烷、氯乙烷、氯乙烯等少数为气体外,其余为液体或固体。
(2)一氯代烷的物理性质:随着碳原子数增加,其熔、沸点和密度逐渐增大(沸点和熔点大于相应的烃)。
(3)难溶于水,易溶于有机溶剂,除脂肪烃的一氟代物、一氯代物等部分卤代烃外,液态卤代烃的密度一般比水大。密度一般随烃基中碳原子数增加而增大。
2.卤代烃的化学性质与C2H5Br相似,可以发生水解反应和消去反应
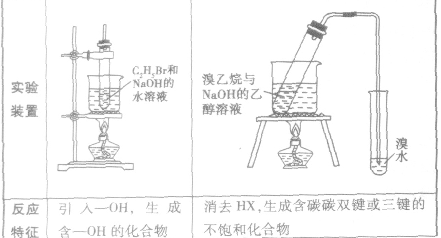

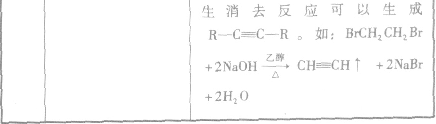
卤代烃中卤素的检验:
1.实验原理
根据AgX的颜色(白色、淡黄色、黄色)可确定卤素(氯、溴、碘):
2.实验步骤
①取少量卤代烃;
②加入NaOH溶液;
③加热煮沸;
④加入过量稀硝酸酸化;
⑤加入AgNO3溶液。
3.实验说明加热煮沸是为了加快水解速率,因不同的卤代烃水解难易程度不同;加入过量稀硝酸酸化是为了中和过量的NaOH,防止NaOH与AgNO3反应,干扰实验现象,同时也是为了检验生成的沉淀是否溶于稀硝酸。
卤代烃在有机物转化和合成中的重要桥梁作用:
1.一元代物与二元代物之间的转化关系 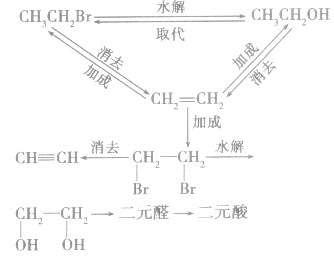
2.卤代烃的桥梁作用通过烷烃、芳香烃与X2发生取代反应,烯烃、炔烃与X2、HX发生加成反应等途径可向有机物分子中引入一X;而卤代烃的水解和消去反应均消去一X。卤代烃发生取代、消去反应后,可在更大的空间上与醇、醛、酯相联系。引入卤素原子常常是改变性能的第一步,卤代烃在有机物转化、推断、合成巾具有“桥梁”的重要地位和作用。
溴乙烷:
1.分子结构
分子式: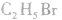
结构式: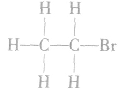
电子式: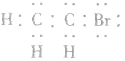
结构简式: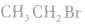
2.溴乙烷的物理性质纯净的溴乙烷是无色液体,沸点为38.4℃,密度比水大,难溶于水,易溶于乙醇等多种有机溶剂。
3.溴乙烷的化学性质
(1)水解反应:溴乙烷在NaOH存在的条件下可以跟水发生反应生成乙醇和溴化氢。 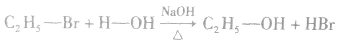
说明:溴乙烷的水解反应又属于取代反应。
溴乙烷水解生成的HBr与NaOH易发生中和反应,水解方程式也可写为:

(2)消去反应:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX)而生成含不饱和键(双键或三键)化合物的反应,叫做消去反应。
溴乙烷与强碱(NaOH或KOH)的乙醇溶液共热,从溴乙烷分子中脱去HBr,生成乙烯: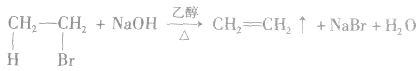
同分异构现象和同分异构体:
1.概念:化合物具有相同的分子式.但结构小同,因而产生了性质上的差异,这种现象叫同分异构现象。具有同分异构现象的化合物互为同分异构体。
2.同分异构体的基本类型
(1)碳链异构:指的是分子中碳骨架不同而产生的同分异构现象。如所有的烷烃异构都属于碳链异构。
(2)位置异构:指的是分子中官能团位置不同而产生的同分异构现象。如l一丁烯与2一丁烯、l一丙醇与2一丙醇、邻二甲苯与间二甲苯及对二甲苯。
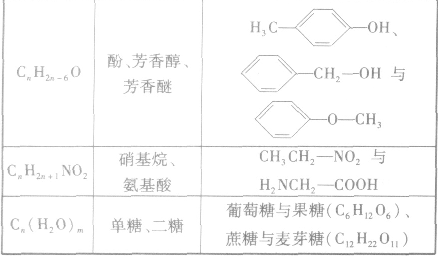
(3)官能团异构:指的是有机物分子式相同,但具有不同官能团的同分异构体的现象。常见的官能团异构关系如下表所示: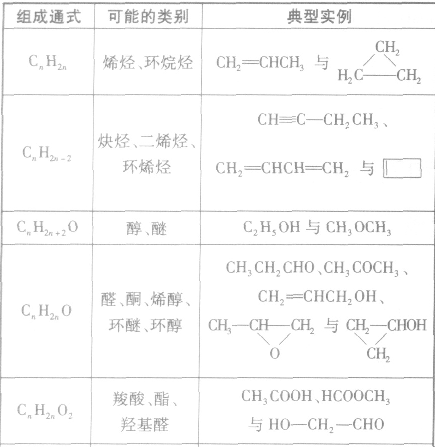
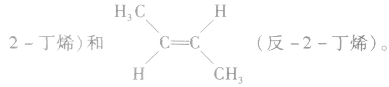
(4)顺反异构:由于碳碳双键不能旋转而导致分子中原子或原子团在空间的排列方式不同所产生的异构现象。两个相同的原子或原子团排列在双键的同一侧的称为顺式结构;两个相同的原子或原子团排列在双键的两侧的称为反式结构。如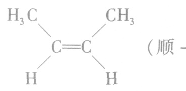
同分异构体的写法:
1.烷烃的同分异构体的写法烷烃只存在碳链异构,其书写技巧一般采用“减碳法”,可概括为“两注意,四句话”。
(1)两注意:①选择最长的碳链为主链;②找出主链的中心对称线。
(2)四句话:主链由长到短、支链由整到散,位置由心到边,排布邻、间、对。
例如,C6H14的同分异构体可按此法完整写出(为了简便,在所写结构式中删去了氢原子): 
2.烯烃的同分异构体的写法分子组成符合CnH2n的烃除烯烃外,还有环烷烃 (n≥3),并且烯烃中双键的位置不同则结构不同,有的烯烃还存在顺反异构,所以烯烃的同分异构体比烷烃复杂得多。以C5H10为例说明同分异构体的写法: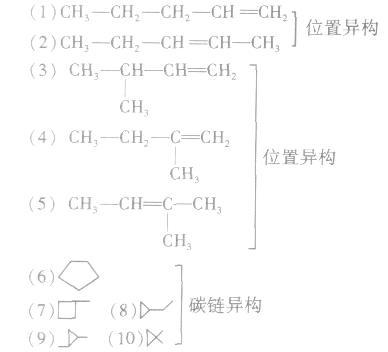
共有5种烯烃,其中(2)还存在顺反异构体,5种环烷烃,共计11种。
3.苯的同系物的同分异构体的写法由于苯环上的侧链位置不同,可以形成多种同分异构体。以C8H10为例写出其属于苯的同系物的同分异构体:
判断同分异构体数目的方法:
1.碳链异构和位置异构:先摘除官能团,书写最长碳链,移动官能团的位置;再逐渐减少碳数,移动官能团的位置。判断分子式为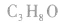 的醇的同分异构体数目:
的醇的同分异构体数目:
先摘除官能团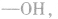 剩余
剩余 和
和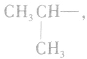 可见有两种属于醇的同分异构体;
可见有两种属于醇的同分异构体;
判断分子式为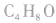 的属于醛的同分异构体数目:
的属于醛的同分异构体数目:
先摘除官能团 剩余
剩余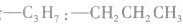 和
和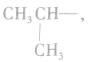 可见有两种属于醛的同分异构体。
可见有两种属于醛的同分异构体。
分子式符合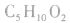 的羧酸的同分异构体数目:
的羧酸的同分异构体数目:
先摘除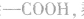 剩余
剩余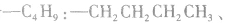
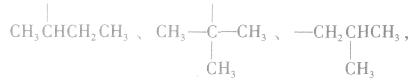 可 见有4种属于酸的同分异构体。
可 见有4种属于酸的同分异构体。
2.官能团衍变:先判断官能团的类别异构,再分别判断同种官能团的异构数目。例如分子式符合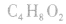 的同分异构体:符合羧酸和酯的通式,属于酸的2种(即摘除
的同分异构体:符合羧酸和酯的通式,属于酸的2种(即摘除 后剩余
后剩余 ),这样一个羧基又可以变为一个醛基和一个羟基,又可以衍变出含有两种不同含氧官能团(含有羟基和醛基)的异构体;属于酯的同分异构体:可以按羧酸和醇的碳数先分类,即酯由一个碳的酸(甲酸)和3个碳的醇(1一丙醇、2一丙醇)得到,酯由2个碳的酸(乙酸)和2个碳的醇(乙醇)得到,酯由3个碳数的酸(丙酸)和1个碳的醇(甲醇)得到,这样就会写出4种酯。
),这样一个羧基又可以变为一个醛基和一个羟基,又可以衍变出含有两种不同含氧官能团(含有羟基和醛基)的异构体;属于酯的同分异构体:可以按羧酸和醇的碳数先分类,即酯由一个碳的酸(甲酸)和3个碳的醇(1一丙醇、2一丙醇)得到,酯由2个碳的酸(乙酸)和2个碳的醇(乙醇)得到,酯由3个碳数的酸(丙酸)和1个碳的醇(甲醇)得到,这样就会写出4种酯。
3.苯环上的位置变换:例如分子式符合 的芳香酯的同分异构体:
的芳香酯的同分异构体: 
4.判断取代产物种类(“一”取代产物:对称轴法; “多”取代产物:一定一动法;数学组合法)。
5.替代法:例如二氯苯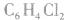 有3种,则四氯苯也为3种(将H替代C1);又如CH4的一氯代物只有一种,新戊烷C(CH3)4的一氯代物也只有一种。
有3种,则四氯苯也为3种(将H替代C1);又如CH4的一氯代物只有一种,新戊烷C(CH3)4的一氯代物也只有一种。
6.对称法(又称等效氢法):等效氢法的判断可按下列三点进行:
(1)同一碳原子上的氢原子是等效的;
(2)同一碳原子所连甲基上的氢原子是等效的;
(3)处于镜面对称位置上的氢原子是等效的(相当于平面成像时,物与像的关系)。
烃的一取代物的数目等于烃分子中等效氢的种数。
与“下列说法错误的是[ ]A.顺-2-丁烯和反-2-丁烯分别与H2加成,...”考查相似的试题有:
- 根据柠檬醛的结构简式:,判断下列各有关说法中不正确的是[ ]A.它可以使酸性高锰酸钾溶液褪色B.它可以使溴水褪色C.它与银...
- 下列化合物分子中,在核磁共振氢谱图中能给出三个信号峰的是A.CH3CH2CH3B.CH3CH2OHC.CH3CH(CH3)2D.CH3CH2CH2CH3
- 阿司匹林的有效成分是乙酰水杨酸()。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的...
- 下列实验用酸性KMnO4溶液不能达到预期目的的是A.鉴别SO2和CO2B.检验硫酸铁溶液中是否有硫酸亚铁C.鉴别苯和对二甲苯D.检验...
- 下列说法正确的是( ) A.C6H5CH2OH不属于醇类 B.油脂的硬化属于水解反应 C.苯和甲苯都能使KMnO4酸性溶液褪色 D.1-氯丙烷...
- 为了鉴别己烯、甲苯和丙醛,使用的试剂组先后关系正确的是( )A.新制Cu(OH)2悬浊液及溴水B.KMnO4酸性溶液及溴水C.银氨溶...
- 可用下图所示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:(1)试管a中需要加入浓硫酸,冰醋酸和乙醇各2 mL,...
- 有机物A的结构简式如右图,下列关于A的性质叙述中,错误的是A.A不能发生水解反应B.A能与碳酸钠溶液反应C.A与氢氧化钠溶液...
- 高血脂症是现代人的健康杀手之一,科学家最新研制的一种可用于治疗高血脂的新药H可按如下路线合成。合成中可能用到的信息信息...
- 下列说法中错误的是[ ]①化学性质相似的有机物是同系物;②分子组成相差一个或几个CH2原子团的有机物是同系物;③若烃中碳、氢元...