本试题 “(8分)某澄清溶液,可能含有NH4+、Na+、K+、Cl-、CO32-、SO42-中的一种或几种,现做如下实验:①取少量该溶液加入BaCl2溶液有白色沉淀生成,再加入足量盐...” 主要考查您对强电解质、弱电解质
电解质、非电解质
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 强电解质、弱电解质
- 电解质、非电解质
强电解质:
在水溶液里或熔融状态下,能全部电离的化合物。包括:强酸、强碱、大多数盐、活泼金属氧化物等;完全电离、不可逆、不存在电离平衡;电离方程式用“=”表示。
弱电解质:
在水溶液里或熔融状态下,不能全部电离的化合物。包括:弱酸、弱碱、少数盐等;部分电离、可逆、存在电离平衡,电离方程式用“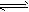 ”表示。
”表示。
在水溶液里或熔融状态下,能全部电离的化合物。包括:强酸、强碱、大多数盐、活泼金属氧化物等;完全电离、不可逆、不存在电离平衡;电离方程式用“=”表示。
弱电解质:
在水溶液里或熔融状态下,不能全部电离的化合物。包括:弱酸、弱碱、少数盐等;部分电离、可逆、存在电离平衡,电离方程式用“
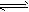 ”表示。
”表示。 强电解质和弱电解质的比较:
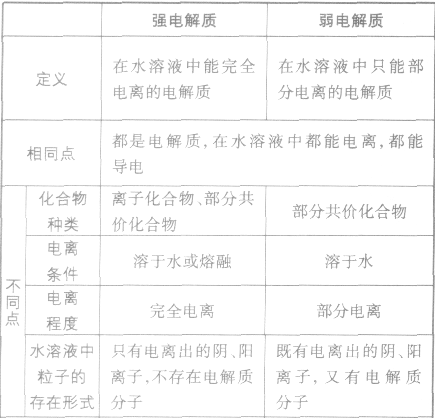
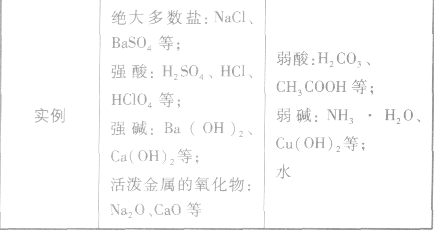
强弱电解质的判断依据:
1.在相同浓度、相同温度下,与强电解质做导电性对比实验.
2.浓度与pH的关系。如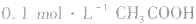 溶液的pH>1,则证明
溶液的pH>1,则证明 是弱电解质。
是弱电解质。
3.测定对应盐溶液的酸碱性。如 溶液呈碱性,则证明醋酸是弱电解质。
溶液呈碱性,则证明醋酸是弱电解质。
4.稀释前后的pH变化与稀释倍数的关系。例如,将pH=2的酸溶液稀释1000倍,若pH<5,则证明该酸为弱电解质;若pH=5,则证明该酸为强电解质。
5.采用实验证明电离平衡。如向醋酸溶液中滴人石蕊试液,溶液变红,再加入醋酸钠晶体,颜色变浅。
电解质和非电解质:
1.电解质和非电解质在水溶液里或熔融状态下能导电的化合物,叫做电解质。在水溶液里和熔融状态下都不导电的化合物,叫做非电解质。
2.电解质和非电解质的比较

说明(1)电解质、非电解质均是化合物。
(2)电解质导电必须有外界条件:水溶液或熔融状态。
(3)电解质是一定条件下本身电离而导电的化合物。CO2、SO2、SO3、NH3溶于水后也导电,但是与水反应生成的新物质电离而导电的,不是本身电离而导电的,故属于非电解质。
(4)电解质的强弱由物质的内部结构决定,与其溶解度无关。某些难溶于水的化合物,如BaSO4、AgCl,虽然溶解度很小,但溶解的部分是完全电离的,所以是强电解质。
(5)电解质不一定导电,非电解质一定不导电;导电的物质不一定是电解质,不导电的物质不一定是非电解质。
1.电解质和非电解质在水溶液里或熔融状态下能导电的化合物,叫做电解质。在水溶液里和熔融状态下都不导电的化合物,叫做非电解质。
2.电解质和非电解质的比较

说明(1)电解质、非电解质均是化合物。
(2)电解质导电必须有外界条件:水溶液或熔融状态。
(3)电解质是一定条件下本身电离而导电的化合物。CO2、SO2、SO3、NH3溶于水后也导电,但是与水反应生成的新物质电离而导电的,不是本身电离而导电的,故属于非电解质。
(4)电解质的强弱由物质的内部结构决定,与其溶解度无关。某些难溶于水的化合物,如BaSO4、AgCl,虽然溶解度很小,但溶解的部分是完全电离的,所以是强电解质。
(5)电解质不一定导电,非电解质一定不导电;导电的物质不一定是电解质,不导电的物质不一定是非电解质。
发现相似题
与“(8分)某澄清溶液,可能含有NH4+、Na+、K+、Cl-、CO32-、S...”考查相似的试题有:
- 下列物质中,能导电的电解质是( )A.石墨B.稀H2SO4C.熔融状态的NaCl D.SO2
- 下列物质在一定条件下能够导电,但是不属于电解质的是:A.铝B.食盐C.硫酸D.蔗糖
- 下列物质中,属于电解质的是A.CO2B.石墨C.K2SO4D.NaOH溶液
- 下列各项中,电离方程式正确的是A.HCO3-+H2OCO32-+ H3O+B.H2SO3=2H++SO32-C.NaHCO3Na++HCO3-D.NaHSO4(熔融)=Na++H++ SO42-
- 下列各组物质中,都是强电解质的是:A.HBr、HCl 、HFB.CaCO3、CH3COONa、NaHSC.NaOH、Ca(OH)2、NH3D.HClO、CaF2、Ba(OH)2
- 下列电离方程式,书写正确的是A.KMnO4=K++Mn7++4O2-B.NaHCO3=Na++H++CO32-C.AlCl3=Al3++Cl3-D.Al2(SO4)3=2Al3++3SO42-
- 有下列物质A.CO2;B.稀盐酸;C.BaCO3;D.NaOH; E.铜。是电解质的有: ;写出B和C反应的离子方程式:
- 在下列物质:A.烧碱B.硫酸C.干冰D.铁片E.纯碱(1)属于电解质的有______,(2)在水中所电离出自由移动阴离子只有OH-的...
- 下列物质中,不属于电解质的是( )A.氢氧化钠B.硫酸C.蔗糖D.氯化钠
- A.H2SO4B.Na2SO4C.HClD.C2H5OH