本试题 “化学课上,某小组实验桌上有一瓶无标签的无色透明溶液,从组成上看,这瓶溶液不可能是( )A.混合物B.纯净物C.含有Cu2+的盐溶液D.有机物” 主要考查您对溶液的定义、组成及特征
乙醇
离子的检验
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶液的定义、组成及特征
- 乙醇
- 离子的检验
溶液的概念:
一种或几种物质分散到另一种物质中,形成均一的,稳定的混合物,叫做溶液
溶液的组成:
(1)溶液由溶剂和溶质组成溶质:被溶解的物质溶剂:
溶液质量=溶剂质量+溶质质量
溶液的体积≠溶质的体积+溶剂的体积
(2)溶质可以是固体(氯化钠、硝酸钾等)、液体(酒精、硫酸等)或气体(氯化氢、二氧化碳等),一种溶液中的溶质可以是一种或多种物质。水是最常用的溶剂,汽油、洒精等也可以作为溶剂,如汽油能够溶解油脂,洒精能够溶解碘等。
溶液的特征:
均一性:溶液中各部分的性质都一样;
稳定性:外界条件不变时,溶液长时间放置不会分层,也不会析出固体溶质
对溶液概念的理解:
溶液是一种或儿种物质分散到另一种物质里.形成的均一、稳定的混合物。应从以下几个方面理解:
(1)溶液属于混合物;
(2)溶液的特征是均一、稳定;
(3)溶液中的溶质可以同时有多种;
(4)溶液并不一定都是无色的,如CuSO4溶液为蓝色;
(5)均一、稳定的液体并不一定郡是溶液,如水;
(6)溶液不一定都是液态的,如空气。
溶液与液体
(1)溶液并不仅局限于液态,只要是分散质高度分散(以单个分子、原子或离子状态存在)的体系均称为溶液。如锡、铅的合金焊锡,有色玻璃等称为固态溶液。气态的混合物可称为气态溶液,如空气。我们通常指的溶液是最熟悉的液态溶液,如糖水、盐水等。
(2)液体是指物质的形态之一。如通常状况下水是液体,液体不一定是溶液。
3. 溶液中溶质、溶剂的判断
(1)根据名称。溶液的名称一般为溶质的名称后加溶剂,即溶质在前,溶剂在后。如食盐水中食盐是溶质,水是溶剂,碘酒中碘是溶质,酒精是溶剂。
(2)若是固体或气体与液体相互溶解成为溶液。一般习惯将固体或气体看作溶质,液体看作溶剂。
(3)若是由两种液体组成的溶液,一般习惯上把量最多的看作溶剂,量少的看作溶质。
(4)其他物质溶解于水形成溶液时。无论,水量的多少,水都是溶剂。
(5)一般水溶液中不指明溶剂,如硫酸铜溶液,就是硫酸铜的水溶液,蔗糖溶液就是蔗糖的水溶液,所以未指明溶剂的一般为水。
(6)物质在溶解时发生了化学变化,那么在形成的溶液中,溶质是反应后分散在溶液中的生成物。如 Na2O,SO3分别溶于水后发生化学反应,生成物是 NaOH和H2SO4,因此溶质是NaOH和H2SO4,而不是 Na2O和SO3;将足量锌粒溶于稀硫酸中所得到的溶液中,溶质是硫酸锌(ZnSO4),若将蓝矾(CuSO4·5H2O) 溶于水,溶质是硫酸铜(CuSO4),而不是蓝矾。
溶液的导电性:
探究溶液导电性的实验:
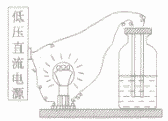
用如图所示的装置试验一些物质的导电性。可以养到蒸馏水、乙醉不导电,而盆酸、硫酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶液、碳酸钠溶液均能导电。
酸、碱、盐溶液导电的原因:
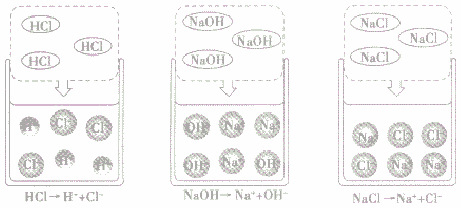
酸、碱、盐溶于水,在水分子作用下,电离成自由移动的带正(或负)电的阳(或阴)离子(如下图所示)。因此酸、碱、盐的水溶液都能导电,导电的原因是溶液中存在自由移动的离子,而蒸馏水和乙醇中不存在自由移动的离子。
定义:
乙醇的结构简式为C2H5OH,俗称酒精,它在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有特殊的、令人愉快的香味,并略带刺激性。乙醇的用途很广,可用乙醇来制造醋酸、饮料、香精、染料、燃料等。医疗上也常用体积分数为70%——75%的乙醇作消毒剂等。
性状:无色透明液体(纯酒精),有特殊香味的气味,易挥发。能与水、氯仿、乙醚、甲醇、丙酮和其他多数有机溶剂混溶,相对密度(d15.56)0.816,易燃,蒸气能与空气形成爆炸性混合物。
危险特征:本品易燃,其蒸气与空气可形成爆炸性混合物。遇明火、高热能引起燃烧爆炸。与氧化剂接触发生化学反应或引起燃烧。在火场中,受热的容器有爆炸的危险。其蒸气比空气重,能在较低处扩散到相当远的地方,遇明火会引着回燃。
乙醇的性质:
1. 物理性质:性状无色透明、易燃易挥发液体。有酒的气味和刺激性辛辣味。
熔点-117.3℃
沸点78.32℃
相对密度0.7893
闪点14℃
溶解性溶于水、甲醇、乙醚和氯仿。能溶解许多有机化合物和若干无机化合物。
2. 化学性质:
氧化反应
(1)燃烧:发出淡蓝色火焰,生成二氧化碳和水(蒸气),并放出大量的热,不完全燃烧时还生成一氧化碳,有黄色火焰,放出热量
完全燃烧:C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
不完全燃烧:2C2H5OH+5O2 2CO2+2CO+6H2O
2CO2+2CO+6H2O
安全措施:
泄漏:迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限制出入。切断火源。建议应急处理人员戴自给正压式呼吸器,穿消防防护服。尽可能切断泄漏源,防止进入下水道、排洪沟等限制性空间。
小量泄露:用砂土或其它不燃材料吸附或吸收。也可用大量水冲洗,洗水稀释后放入废水系统。
大量泄露:构筑围堤或挖坑收容;用泡沫覆盖,降低蒸气灾害。用防爆泵转移至槽车或专用收集器内,回收或运至废物处理场所处置。
灭火方法:
燃烧性:极易燃
灭火剂:抗溶性泡沫、干粉、二氧化碳、砂土。
灭火注意事项:尽可能将容器从火场移至空旷处。喷水保持容器冷却,直至灭火结束。
紧急处理:
吸入:迅速脱离现场至新鲜空气,若现象严重要尽快就医。
误食:饮足量温水,催吐。若现象严重要尽快就医。
皮肤接触:脱去被污染衣着,用流动清水冲洗。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。若现象严重要尽快就医。
实验室使用及灭火
(1)应使用火柴点燃,否则容易使酒精灯内的酒精燃烧。
(2)使用完毕后,应用灯帽将火盖灭。
(3)如不慎将酒精洒出并引燃,则应用湿抹布将其盖灭。
乙醇的用途:
溶剂;有机合成;各种化合物的结晶;洗涤剂;萃取剂;食用酒精可以勾兑白酒;用作粘合剂;硝基喷漆;清漆、化妆品、油墨、脱漆剂等的溶剂以及农药、医药、橡胶、塑料、人造纤维、洗涤剂等的制造原料、还可以做防冻剂、燃料、消毒剂等。 75%(体积分数)的乙醇溶液常用于医疗消毒。
乙醇和甲醇的区别:
①甲醇是甲烷的一个氢原子被羟基(一个氢和一个氧组成的原子团,不是氢氧根)替换后的产物。
乙醇是乙烷一个氢原子被羟基替换后的产物,俗称酒精。
②分子式不一样。
甲醇:CH3OH
乙醇:CH3CH2OH
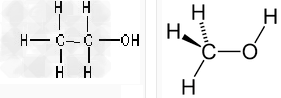
乙醇结构 甲醇结构
他们的分子式不一样,化学性质和物理性质也有区别。
③工业酒精里常含有甲醇,甲醇有毒,不能用工业酒精配制酒
乙醇汽油:
乙醇汽油也被称为(E型汽油),我国使用乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成。它可以改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放。
乙醇的结构简式为C2H5OH,俗称酒精,它在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有特殊的、令人愉快的香味,并略带刺激性。乙醇的用途很广,可用乙醇来制造醋酸、饮料、香精、染料、燃料等。医疗上也常用体积分数为70%——75%的乙醇作消毒剂等。
性状:无色透明液体(纯酒精),有特殊香味的气味,易挥发。能与水、氯仿、乙醚、甲醇、丙酮和其他多数有机溶剂混溶,相对密度(d15.56)0.816,易燃,蒸气能与空气形成爆炸性混合物。
危险特征:本品易燃,其蒸气与空气可形成爆炸性混合物。遇明火、高热能引起燃烧爆炸。与氧化剂接触发生化学反应或引起燃烧。在火场中,受热的容器有爆炸的危险。其蒸气比空气重,能在较低处扩散到相当远的地方,遇明火会引着回燃。
乙醇的性质:
1. 物理性质:性状无色透明、易燃易挥发液体。有酒的气味和刺激性辛辣味。
熔点-117.3℃
沸点78.32℃
相对密度0.7893
闪点14℃
溶解性溶于水、甲醇、乙醚和氯仿。能溶解许多有机化合物和若干无机化合物。
2. 化学性质:
氧化反应
(1)燃烧:发出淡蓝色火焰,生成二氧化碳和水(蒸气),并放出大量的热,不完全燃烧时还生成一氧化碳,有黄色火焰,放出热量
完全燃烧:C2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O 不完全燃烧:2C2H5OH+5O2
 2CO2+2CO+6H2O
2CO2+2CO+6H2O安全措施:
泄漏:迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限制出入。切断火源。建议应急处理人员戴自给正压式呼吸器,穿消防防护服。尽可能切断泄漏源,防止进入下水道、排洪沟等限制性空间。
小量泄露:用砂土或其它不燃材料吸附或吸收。也可用大量水冲洗,洗水稀释后放入废水系统。
大量泄露:构筑围堤或挖坑收容;用泡沫覆盖,降低蒸气灾害。用防爆泵转移至槽车或专用收集器内,回收或运至废物处理场所处置。
灭火方法:
燃烧性:极易燃
灭火剂:抗溶性泡沫、干粉、二氧化碳、砂土。
灭火注意事项:尽可能将容器从火场移至空旷处。喷水保持容器冷却,直至灭火结束。
紧急处理:
吸入:迅速脱离现场至新鲜空气,若现象严重要尽快就医。
误食:饮足量温水,催吐。若现象严重要尽快就医。
皮肤接触:脱去被污染衣着,用流动清水冲洗。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。若现象严重要尽快就医。
实验室使用及灭火
(1)应使用火柴点燃,否则容易使酒精灯内的酒精燃烧。
(2)使用完毕后,应用灯帽将火盖灭。
(3)如不慎将酒精洒出并引燃,则应用湿抹布将其盖灭。
乙醇的用途:
溶剂;有机合成;各种化合物的结晶;洗涤剂;萃取剂;食用酒精可以勾兑白酒;用作粘合剂;硝基喷漆;清漆、化妆品、油墨、脱漆剂等的溶剂以及农药、医药、橡胶、塑料、人造纤维、洗涤剂等的制造原料、还可以做防冻剂、燃料、消毒剂等。 75%(体积分数)的乙醇溶液常用于医疗消毒。
乙醇和甲醇的区别:
①甲醇是甲烷的一个氢原子被羟基(一个氢和一个氧组成的原子团,不是氢氧根)替换后的产物。
乙醇是乙烷一个氢原子被羟基替换后的产物,俗称酒精。
②分子式不一样。
甲醇:CH3OH
乙醇:CH3CH2OH

乙醇结构 甲醇结构
他们的分子式不一样,化学性质和物理性质也有区别。
③工业酒精里常含有甲醇,甲醇有毒,不能用工业酒精配制酒
乙醇汽油:
乙醇汽油也被称为(E型汽油),我国使用乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成。它可以改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放。
定义:
判断溶液中阴阳离子的存在情况。
几种常见离子的检验
常见酸、碱、盐的检验:
检验中的干扰和排除
在物质的检验过程中,由于待检物质中混有杂质、选用试剂不当或试剂不纯,包括仪器不清净、操作有误等.都会对检验造成干扰,应当予以排除。如鉴定CO32- 和SO42-共存时,我们不应该选用硝酸银试剂,而应选用硝酸钡或氯化钡试剂。再如,当CO32-和SO42-共存时,我们要检验出SO42-,则应先加盐酸酸化,排除CO32-离了的干扰后,再用氯化钡试剂进行检验。
检验结果的分析和判断
根据检验过程中所观察到的观象确定试样中存在哪些离子,必须把可能存在的离子全部考虑到,再根据每步检验的现象,肯定或否定某些离子的存在,逐步缩小范围,最终得出正确的结论。
判断溶液中阴阳离子的存在情况。
几种常见离子的检验
| 离子 | 所用试剂 | 方法 | 现象 | 化学方程式 |
| Cl- | AgNO3溶液和稀HNO3 | 将AgNO3溶液滴入待测液中,再加稀HNO3 | 生成白色沉淀.且不溶于稀HNO3 | AgNO3+NaCl==AgCl↓+NaNO3 |
| SO42- | BaCl2溶液和稀盐酸 | 将稀盐酸滴入待测液中,再加BaCl2溶液 | 滴加稀盐酸无现象,滴加 BaCl2溶液生成白色沉淀,且沉淀不溶于稀盐酸 | BaCl2+Na2SO4==BaSO4↓+ +2NaCl |
| CO32- | 盐酸(或HNO3) 和澄清石灰水 | 向待测液中加入盐酸(或HNO3).将产生的气体通入澄清石灰水中 | 产生无色无味的气体,此气体能使澄清的石灰水变浑浊 | Na2CO3+2HCl==2NaCl+H2O+ CO2↑ CO2+Ca(OH)2==CaCO3↓+H2O |
| OH- | 酚酞试液、紫色石蕊试液或红色石蕊试纸 | ①将酚酞试液滴入待测液中 ②将紫色石蕊试液滴入待测液中 ③将待测液滴在红色石蕊试纸上 |
①溶液变红 ②溶液变蓝 ③红色石蕊试纸变蓝 |
—— |
| H+ | 紫色石蕊试液或蓝色石蕊试纸 | ①将紫色石蕊试液滴入待测液中 ②将待测液滴在蓝色石蕊试纸上 |
①溶液变红 ②蓝色石蕊试纸变红 |
—— |
| NH4+ | 浓NaOH溶液 | 将浓NaOH溶液加入待测液中,加热,将湿润的红色石蕊试纸置于试管口(或用玻璃棒蘸浓盐酸置于试管口) | 放出有刺激性气味的气体,该气体能使湿润的红色石蕊试纸变蓝(或遇到浓盐酸产生大量白烟) | NH4Cl+NaOH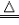 NaCl+H2O+NH3↑ NaCl+H2O+NH3↑ |
| Cu2+ | NaOH溶液 | 将NaOH溶液加入待测液中 | 生成蓝色沉淀 | CuSO4+2NaOH==Cu(OH)2↓ |
| Fe3+ | NaOH溶液 | 将NaOH溶液加入待测液中 | 生成蓝色沉淀 | FeCl3+3NaOH==Fe(OH)3↓+3NaCl |
常见酸、碱、盐的检验:
| 物质 | 检验方法 | 实验现象 | 典型化学式 |
| 硫酸及可溶性硫酸盐 | 取少量待检验溶液于试管中 (1)滴入紫色石蕊试液 (2)滴人稀盐酸和BaCl2溶液[或 Ba(NO3)2溶液] |
(1)溶液变红 (2)加入稀盐酸无明显现象,再加入BaCl2溶液有自色沉淀生成 |
H2SO4+BaCl2==BaSO4↓+2HCl Na2SO4+Ba(NO3)2==BaSO4↓+2NaNO3 |
| 盐酸及可溶性盐酸盐 | 取少量待检验溶液于试管中 (1)滴入紫色石蕊试液 (2)滴人AgNO3溶液和稀硝酸 |
(1)溶液变红 (2)有白色沉淀生成,且该沉淀不溶于稀硝酸 |
HCl+AgNO3=AgCl↓+HNO3 NaCl+AgNO3==AgCl↓+NaNO3 |
| 碳酸盐及碳酸氢盐 | 取少量待检验溶液于试管中 (1)加稀盐酸或稀硝酸 (2)将生成的气体通入澄清的石灰水中。 |
有气体生成,且该气体使澄清的石灰水变浑浊 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ NaHCO3+HCl=NaCl+H2O+CO2↑ |
| 铵盐 | 将铵盐与碱混合共热 | 有刺激性气味气体生成 | NH4Cl+NaOH NaCl+NH3↑+H2O NaCl+NH3↑+H2O |
检验中的干扰和排除
在物质的检验过程中,由于待检物质中混有杂质、选用试剂不当或试剂不纯,包括仪器不清净、操作有误等.都会对检验造成干扰,应当予以排除。如鉴定CO32- 和SO42-共存时,我们不应该选用硝酸银试剂,而应选用硝酸钡或氯化钡试剂。再如,当CO32-和SO42-共存时,我们要检验出SO42-,则应先加盐酸酸化,排除CO32-离了的干扰后,再用氯化钡试剂进行检验。
检验结果的分析和判断
根据检验过程中所观察到的观象确定试样中存在哪些离子,必须把可能存在的离子全部考虑到,再根据每步检验的现象,肯定或否定某些离子的存在,逐步缩小范围,最终得出正确的结论。
发现相似题
与“化学课上,某小组实验桌上有一瓶无标签的无色透明溶液,从组...”考查相似的试题有:
- 在一瓶某物质的饱和溶液中,在温度不变时,加入少量该溶质晶体,则( )A.溶液的质量增大B.溶质的溶解度增大C.晶体的质量...
- 花生油、盐、酱、醋是厨房中常用的调味品,将它们分别与足量水充分混合后,形成的混合物属于溶液的是( )①花生油②食盐③面酱④...
- 在家中,小明取少量的下列物质分别放入水中,充分搅拌,其中能形成溶液的是( )A.面粉B.蔗糖C.芝麻糊D.植物油
- 学习化学时可用右图描述某些相互关系,下列选项正确的是( )XYA溶质溶液B钾肥氮肥C复分解反应中和反应D原子核核外电子A.AB...
- 厨房中的物质放入足量的水中,充分搅拌,不能形成溶液的是( )A.食用油B.白醋C.白糖D.食盐
- 20℃时将a克氯化钠加入b克水中,充分溶解后得溶液c克,则a、b、c的关系表示正确的是( )A.a+b=cB.a+b≤cC.a+b≥cD.a+b>c
- 甲烷、乙醇都是生活中常用的燃料.植物的残体在隔绝空气的情况下就会产生甲烷;而乙醇主要靠人类利用高粱、玉米和薯类发酵等...
- 从农作物中提炼的乙醇被称为“生物汽油”“绿色汽油”。生物能源是中国仅次于煤与石油的第三大能源,被列为国家“863 高科技计划项...
- 以前,人们将石灰石灼烧后的固体与草木灰(主要成分是K2CO3)在水中混合,再取上层澄清液漂洗织物.兴趣小组按照上述的操作步...
- 若从Na2CO3、Na2SO4、H2SO4、NaCl、NaNO3、Cu(NO3)2、HNO3七种溶液中取出其中的两种,进行混合及有关实验,所观察到的现象...