本试题 “正确掌握好化学用语是学好化学的基础,下列有关表述正确的是[ ]A.质量数为16的氧原子:B.纯碱的化学式:NaHCO3 C.Mg2+结构示意图:D.铁丝在氯气中燃烧的...” 主要考查您对化学反应方程式
核素
离子结构示意图
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应方程式
- 核素
- 离子结构示意图
化学方程式:
用化学式来表示化学反应的式子,叫做化学方程式。化学方程式不仅表明了反应物、生成物和反应条件,同时,通过相对分子质量或相对原子质量还可以表示个物质之间的质量关系,即各物质之间的质量比。
书写化学方程式要遵守两个原则:
一是必须以客观事实为基础,绝不能凭空臆想、臆造事实上不存在的物质和化学反应;
二是要遵守质量守恒定律,等号两边各原子种类与数目必须相等。
化学方程式的意义:
化学方程式不仅表明了反应物、生成物和反应条件。同时,化学计量数代表了各反应物、生成物物质的量关系,通过相对分子质量或相对原子质量还可以表示各物质之间的质量关系,即各物质之间的质量比。对于气体反应物、生成物,还可以直接通过化学计量数得出体积比。
定义:
具有一定的质子数和中子数的一种原子叫做核素  的含义:
的含义: 表示一个质量数为A、质子数为Z的原子。
表示一个质量数为A、质子数为Z的原子。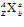 中A表示质量数,Z表示质子数,a表示粒子所带的电荷数和电性,b表示组成该粒子的原子数目。
中A表示质量数,Z表示质子数,a表示粒子所带的电荷数和电性,b表示组成该粒子的原子数目。
元素,核素与同位素的比较:
| 元素 | 同位素 | 核素 | |
| 概念 | 质子数(即核电荷数)相同的一类原子的总称 | 质子数相同而中子数不同的同一元素的不同原子互称为同位素 | 具有一定数目质子和一定数目中子的一种原子 |
| 描述对象 | 宏观物质,列同类原子而言,既有游离态,又有化合态 | 微观物质,对某种元素的原子而言,因为有同位素,所以原子种类多于元素种类 | 微观物质,指某种元素的某种原子 |
| 特征 | 以单质或化合物形式存在,性质通过形成单质或化合物来体现 | 同位素化学性质几乎相同,因为质量数不同,物理性质不同。天然存在的各种同位素所占的原子个数百分比一般不变 | 具有真实的质量,不同核素的质量不相同 |
| 实例 | H、Na、S为不同的三种元素 | 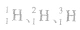 互为同位素 互为同位素 |
 是一种核素, 是一种核素, 是一种核素 是一种核素 |
正离子的离子结构示意图中核内质子数大于核外电子数;
负离子的离子结构示意图中核内质子数小于核外电子数。
原子是否满足最外层8电子结构的判断方法:
1.离子化合物
(1)阳离子:看“主族元素原子的次外层电子数+ 原子的最外层电子数一化合价数”是否等于8,若为8,则该原子满足最外层8电子结构,否则不满足。
(2)阴离子:看“其原子的最外层电子数+化合价的绝对值”是否等于8,若为8,则该原子满足最外层8 电子结构,否则不满足。
2.共价化合物计算“各原子的最外层电子数+化合价的绝对值” 是否等于8,若为8,则该原子满足最外层8电子结构,否则不满足。另外,还有一些不满足8电子结构的特殊粒子,请大家记住:
(1)主族元素形成的化合物中:
a.H、Li、Be、B元素原子不满足最外层8电子结构.
b.非最高价离子(如 Pb2+、Bi3+等)也不满足最外层8电子结构。
(2)过渡金属元素形成的离子最外层电子数一般大于8.
与“正确掌握好化学用语是学好化学的基础,下列有关表述正确的是[...”考查相似的试题有:
- 由NO、H2、CO2组成的混合气体通过过量的Na2O2后引燃,使其充分反应,得到浓度为70%的硝酸溶液(无任何气体剩余).混合气体中...
- 将一份CaCO3粉末放入500mL的盐酸中,恰好完全反应,收集到的CO2体积为44.8L(标准状况),求:(1)CaCO3的质量;(2)盐酸的...
- 下列反应的化学方程式(或离子方程式)错误的是( )A.乙醛与银氨溶液反应 CH3CHO+2[Ag(NH3)2]OH △CH3COONH4+2Ag↓+3NH3+H2...
- 实验室用17.4g的MnO2与100mL足量的浓盐酸制取氯气:MnO2+4HCl (浓) △ . MnCl2+Cl2↑+2H2O(1)求生成氯气的体积(标准状况)...
- 一种塑料增塑剂G的合成路线如下图.已知A在一定条件下发生消去反应,能得到两种互为同分异构体的产物.试回答:(1)反应类型...
- 某地有软锰矿和闪锌矿两座矿山,它们的组成如下: 软锰矿:MnO2含量≥65%,SiO2含量约20%,Al2O3含量约4%,其余为水分; 闪锌...
- 下列化学用语正确的是[ ]A.钙离子的电子式 Ca2+B.甲基的电子式C.原子核内有8个中子的碳原子D.乙烷的分子式 CH3CH3
- 下列有关化学用语表述正确的是( )A.质量数为16的氧原子:168OB.漂白粉的有效成分:NaClOC.Mg2+结构示意图:D.钠在氧气...
- 下列化学用语正确的是[ ]A.HCl的电子式B.Cl-的结构示意图C.CO2的电子式D.质量数为37的氯原子1737Cl
- 化学科学需要借助化学专用语言描述,下列有关化学用语正确的是[ ]A.CO2的电子式B.Cl-的结构示意图C.乙烯的结构简式 C2H4D...