本试题 “某蔬菜基地在种植蔬菜时,常采用下列方法.(1)施用适量的氮肥可以使种植的蔬菜叶色浓绿.①下列化肥中,属于氮肥的是_________.(填字母)A.碳酸氢铵(NH4...” 主要考查您对化肥
二氧化碳的用途
物质的除杂
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化肥
- 二氧化碳的用途
- 物质的除杂
化学肥料的概念:
化学肥料是指以矿物、空气、水做原料,经过化学加工制成含有植物生长所需的营养元素的物质,简称化肥。农作物所必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等,其中氮、磷、钾需要量较大,因此氮肥、磷肥、钾肥是最主要的化学肥料。另外还有同时含有两种或两种以上营养元素的复合肥,植物生长过程中需要量比较少的微量元素肥料。
常见化学肥料:
1、氮肥
①作用:氮是合成蛋白质、核酸和叶绿素的重要元素,氮肥充足会使植物枝繁叶茂、果实硕大。缺少氮元素,会使植物生长发育迟缓或停滞,光合作用减慢等。外观表现为植株矮小,瘦弱,叶片发黄,严重时叶脉为棕色。
②氮肥的特性
a.氮盐与碱混合受热可产生一种无色、有刺激性气味的气体,它能使湿润的红色石蕊试纸变蓝。例如: NaOH+NH4NO3=NaNO3+H2O+NH3↑
检验按根离子(NH4+)时,需有可溶性碱和红色石蕊试纸。
b.氨水是氨气的水溶液,溶于水的氨气大部分与水反应生成一水合氨。一水合氨在水中发生电离,生成铵根离子和氢氧根离子。由于氨水中存在的阴离子全部是OH-,所以氨水呈碱性,一水合氨属于碱类。请注意,通常情况下氨水指氨气溶于水后生成的一水合氨(NH3·H2O),切勿将氨水的化学式写成NH4OH,因为氨水中没有NH4OH存在。
c.碳酸氢按受热分解:NH4HCO3==NH3↑+ CO2↑+H2O↑。
③氮的固定将氮气转化为氮的化合物的方法。如:豆科植物根部的根瘤菌能把空气中的氮气转化为含氮化合物,这类植物无需或只需少量使用氮肥。
2、磷肥
①作用:磷能促进作物生长,增强抗寒、抗旱能力。若缺乏磷元素,常表现为生长迟缓、产量降低,但磷过量则会引起作物贪青晚熟,结实率下降。外观表现为植株特别矮小,叶片出现紫色。
②常见磷肥有磷矿粉[Ca3(PO4)2]、钙镁磷肥(钙和镁的磷酸盐)、过磷酸钙[磷酸二氢钙Ca(H2PO4)2 和CaSO4的混合物]等。
3、钾肥
①作用:钾肥能保证各种代谢过程的顺利进行、促进植物生民、增强抗病虫害和抗倒伏能力。若缺乏钾元素,常表现为茎秆软弱、容易倒伏、叶片的边缘和尖端呈褐色,并逐渐焦枯。
②常见钾肥有硫酸钾(K2SO4)、氯化钾(KCl)和草木灰(主要成分为K2CO3)等。
(4)复合肥
含两种或两种以土营养元素的化肥。
①特点能同时均匀地供给作物几种养分,充分发挥营养元素间的互补作用,有效成分高。
②种类磷酸按〔磷酸二氢铵NH4H2PO4和磷酸氢二按 (NH4)2HPO4的混合物」、硝酸钾(KNO3)。
常见氮肥及性质:
化肥和农家肥的比较:
使用化肥、农药的利与弊:
①利:化肥、农药对提高农作物的产量具有重要的作用。
②弊:
a.不合理施用化肥会带来很多环境问题,一方面化肥中含有一些重金属元素、有毒有机物和放射性物质,施人后会引起潜在的土壤污染;另一方面化肥在施用过程中,因某些成分的积累、流失或变化,引起土壤酸化,水域中氮和磷含量升高,氮化物和硫化物气体排放等,造成土壤退化和水、大气环境的污染。
b.农药本身有毒,在杀灭病虫害的同时也带来了对自然环境的污染和对人体健康的危害。
使用化肥的注意事项:
①铰态氮肥不能与碱性物质(如碱、草木灰等)一起使用,因为铵态氮肥中的NH4+遇到OH-会生成易挥发的NH3,降低肥效。
②使用氨水或磷酸氢铵时要防止挥发,立即灌溉或用土盖上,人要站在上风口,因氨气对人的眼、鼻等膜有刺激作用。
③硝酸按受热易分解,在高温或猛烈撞击时易发生爆炸。所以当硝酸铵受潮结块时,不要用铁锤砸碎。
④硫酸按不易长时间使用,以免造成土壤酸性增强或土壤板结。
化肥鉴别的方法:
①一看、二闻、三溶看外观,氮肥、钾肥为白色晶体,磷肥是灰白色粉末;闻气味,碳酸氢按有强烈的氨味,可直接将它与其他氮肥相区别;加水溶解,氮肥、钾肥全部溶于水,磷肥大多不溶于水。铵盐的鉴别:(NH4)2SO4、NH4NO3等和熟石灰混合研磨,放出具有刺激性气味的氨气。
②氮肥的简易鉴别氮肥中的氨水呈液态,碳酸氧钱有强烈的氨味,据此可直接将它们与其他氮肥相区别。其他常见氮肥可按下列步骤鉴别:
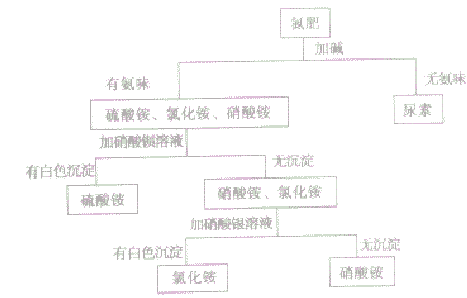
注意硫酸铵、氯化铵、硝酸铵同时鉴别时,不能先加硝酸银溶液鉴别氯化铵,因为硝酸银与硫酸铵反应,可能生成微溶物硫酸银,也可能出现沉淀。所以要区分含SO42-、Cl-和NO3-的三种物质时,一般是先加硝酸钡来鉴别出含有SO42-的物质,再加入硝酸银,鉴别出含有Cl-的物质,无现象的则是含有NO3-的物质。
③化肥鉴别歌鉴别化肥简易行,无锈铁片火烧红;化肥分别铁上放,各自现象皆不同;遇铁冒烟化成水,定是尿素不可疑;若是只熔不冒烟,刺鼻气味是磷铵;一阵烟后冒火星,必是硝铵显神通;铁上发出紫火焰,吱吱微响是硫铵;要想测知氯化铵,触铁味如浓盐酸;磷肥多为灰白色,置于红铁味难闻;放于红铁爆噼啪,无氨味者硫酸钾,氨化磷肥与有别,无烟臭气呛煞人;上述现象若不符,其中有诈须谨慎;认真鉴别把握准,防止上当把钱费。
盐的命名:
(1)只有两种元素组成的盐,读作“某化某”,如 NaCl读作氯化钠,AgI读作碘化银。
(2)构成中含有酸根的,读作“某酸某”。如Na2CO3、ZnSO4、AgNO3、KMnO4、KClO3分别读作:碳酸钠、硫酸锌、硝酸银、高锰酸钾、氯酸钾。
(3)含铵根的化合物,读作“某化铵”或“某酸铵”。如NH4Cl、(NH4)2SO4读作:氯化铵、硫酸铵。
(4)其他:Cu2(OH)2CO3读作“碱式碳酸铜”, NaHSO4读作“硫酸氢钠”, NaHCO3读作“碳酸氢钠”。
化学肥料是指以矿物、空气、水做原料,经过化学加工制成含有植物生长所需的营养元素的物质,简称化肥。农作物所必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等,其中氮、磷、钾需要量较大,因此氮肥、磷肥、钾肥是最主要的化学肥料。另外还有同时含有两种或两种以上营养元素的复合肥,植物生长过程中需要量比较少的微量元素肥料。
常见化学肥料:
1、氮肥
①作用:氮是合成蛋白质、核酸和叶绿素的重要元素,氮肥充足会使植物枝繁叶茂、果实硕大。缺少氮元素,会使植物生长发育迟缓或停滞,光合作用减慢等。外观表现为植株矮小,瘦弱,叶片发黄,严重时叶脉为棕色。
②氮肥的特性
a.氮盐与碱混合受热可产生一种无色、有刺激性气味的气体,它能使湿润的红色石蕊试纸变蓝。例如: NaOH+NH4NO3=NaNO3+H2O+NH3↑
检验按根离子(NH4+)时,需有可溶性碱和红色石蕊试纸。
b.氨水是氨气的水溶液,溶于水的氨气大部分与水反应生成一水合氨。一水合氨在水中发生电离,生成铵根离子和氢氧根离子。由于氨水中存在的阴离子全部是OH-,所以氨水呈碱性,一水合氨属于碱类。请注意,通常情况下氨水指氨气溶于水后生成的一水合氨(NH3·H2O),切勿将氨水的化学式写成NH4OH,因为氨水中没有NH4OH存在。
c.碳酸氢按受热分解:NH4HCO3==NH3↑+ CO2↑+H2O↑。
③氮的固定将氮气转化为氮的化合物的方法。如:豆科植物根部的根瘤菌能把空气中的氮气转化为含氮化合物,这类植物无需或只需少量使用氮肥。
2、磷肥
①作用:磷能促进作物生长,增强抗寒、抗旱能力。若缺乏磷元素,常表现为生长迟缓、产量降低,但磷过量则会引起作物贪青晚熟,结实率下降。外观表现为植株特别矮小,叶片出现紫色。
②常见磷肥有磷矿粉[Ca3(PO4)2]、钙镁磷肥(钙和镁的磷酸盐)、过磷酸钙[磷酸二氢钙Ca(H2PO4)2 和CaSO4的混合物]等。
3、钾肥
①作用:钾肥能保证各种代谢过程的顺利进行、促进植物生民、增强抗病虫害和抗倒伏能力。若缺乏钾元素,常表现为茎秆软弱、容易倒伏、叶片的边缘和尖端呈褐色,并逐渐焦枯。
②常见钾肥有硫酸钾(K2SO4)、氯化钾(KCl)和草木灰(主要成分为K2CO3)等。
(4)复合肥
含两种或两种以土营养元素的化肥。
①特点能同时均匀地供给作物几种养分,充分发挥营养元素间的互补作用,有效成分高。
②种类磷酸按〔磷酸二氢铵NH4H2PO4和磷酸氢二按 (NH4)2HPO4的混合物」、硝酸钾(KNO3)。
常见氮肥及性质:
| 名称 | 化学式 | 性质 | 注意事项 |
| 尿素 | CO(NH2)2 | 白色或淡黄色晶体,易溶 于水,含氮量不超过46.7%, 肥效高且持久,对土壤无 不良影响 |
—— |
| 碳酸氢铵 | NH4HCO3 | 白色晶体,易溶于水,受潮 时常温下就能分解,温度越 高,分解越快,在土壤中不 残留有害杂质,含氮量低于 17.7% |
防分解,贮存和运输时 都要密封.不要受潮或暴 晒,施肥后掩盖或立即 灌溉,不要与碱性物质 混合使用 |
| 硝酸铵 | NH4NO3 | 白色晶体,易溶于水,高温 或受猛烈撞击时易爆炸,含 氮量低于35%,对土壤无不 良影响 |
不要与易燃物质或碱性 物质混合在一起,结块 时,不要用铁锤砸碎 |
| 硫酸铵 | (NH4)2SO4 | 白色固体,易溶于水,常温 下性质稳定,不宜长期大量 使用,否则会使土壤酸化、 板结硬化 |
不能与碱性物质混合, 不宜长期大量使用 |
| 氨水 | NH3·H2O | 氨气的水溶液,易挥发,显碱性 | 运愉、扩存、使用时要 防挥发 |
化肥和农家肥的比较:
| 所含元素种类少,但营养元素含量大 | 常含有多种营养元素,但营养元素含量较少 |
| 一般易溶于水,易被农作物吸收,肥效较快 | 一般较难溶于水,经腐熟后逐步转化为可溶于水、能被作物吸收的物质,肥效慢但肥期较长 |
| 便于工业生产,成本较高 | 便于就地取材,成本低廉 |
| 长期使用会破坏土壤的结构,使果蔬、谷物含有超量化肥,影响人体健康;化肥还会造成水体污染,引起水体富营养化 | 能改良土壤结构 |
使用化肥、农药的利与弊:
①利:化肥、农药对提高农作物的产量具有重要的作用。
②弊:
a.不合理施用化肥会带来很多环境问题,一方面化肥中含有一些重金属元素、有毒有机物和放射性物质,施人后会引起潜在的土壤污染;另一方面化肥在施用过程中,因某些成分的积累、流失或变化,引起土壤酸化,水域中氮和磷含量升高,氮化物和硫化物气体排放等,造成土壤退化和水、大气环境的污染。
b.农药本身有毒,在杀灭病虫害的同时也带来了对自然环境的污染和对人体健康的危害。
使用化肥的注意事项:
①铰态氮肥不能与碱性物质(如碱、草木灰等)一起使用,因为铵态氮肥中的NH4+遇到OH-会生成易挥发的NH3,降低肥效。
②使用氨水或磷酸氢铵时要防止挥发,立即灌溉或用土盖上,人要站在上风口,因氨气对人的眼、鼻等膜有刺激作用。
③硝酸按受热易分解,在高温或猛烈撞击时易发生爆炸。所以当硝酸铵受潮结块时,不要用铁锤砸碎。
④硫酸按不易长时间使用,以免造成土壤酸性增强或土壤板结。
化肥鉴别的方法:
①一看、二闻、三溶看外观,氮肥、钾肥为白色晶体,磷肥是灰白色粉末;闻气味,碳酸氢按有强烈的氨味,可直接将它与其他氮肥相区别;加水溶解,氮肥、钾肥全部溶于水,磷肥大多不溶于水。铵盐的鉴别:(NH4)2SO4、NH4NO3等和熟石灰混合研磨,放出具有刺激性气味的氨气。
②氮肥的简易鉴别氮肥中的氨水呈液态,碳酸氧钱有强烈的氨味,据此可直接将它们与其他氮肥相区别。其他常见氮肥可按下列步骤鉴别:

注意硫酸铵、氯化铵、硝酸铵同时鉴别时,不能先加硝酸银溶液鉴别氯化铵,因为硝酸银与硫酸铵反应,可能生成微溶物硫酸银,也可能出现沉淀。所以要区分含SO42-、Cl-和NO3-的三种物质时,一般是先加硝酸钡来鉴别出含有SO42-的物质,再加入硝酸银,鉴别出含有Cl-的物质,无现象的则是含有NO3-的物质。
③化肥鉴别歌鉴别化肥简易行,无锈铁片火烧红;化肥分别铁上放,各自现象皆不同;遇铁冒烟化成水,定是尿素不可疑;若是只熔不冒烟,刺鼻气味是磷铵;一阵烟后冒火星,必是硝铵显神通;铁上发出紫火焰,吱吱微响是硫铵;要想测知氯化铵,触铁味如浓盐酸;磷肥多为灰白色,置于红铁味难闻;放于红铁爆噼啪,无氨味者硫酸钾,氨化磷肥与有别,无烟臭气呛煞人;上述现象若不符,其中有诈须谨慎;认真鉴别把握准,防止上当把钱费。
盐的命名:
(1)只有两种元素组成的盐,读作“某化某”,如 NaCl读作氯化钠,AgI读作碘化银。
(2)构成中含有酸根的,读作“某酸某”。如Na2CO3、ZnSO4、AgNO3、KMnO4、KClO3分别读作:碳酸钠、硫酸锌、硝酸银、高锰酸钾、氯酸钾。
(3)含铵根的化合物,读作“某化铵”或“某酸铵”。如NH4Cl、(NH4)2SO4读作:氯化铵、硫酸铵。
(4)其他:Cu2(OH)2CO3读作“碱式碳酸铜”, NaHSO4读作“硫酸氢钠”, NaHCO3读作“碳酸氢钠”。
二氧化碳用途:
1.二氧化碳不支持燃烧,不能燃烧,比空气重,可用于灭火
2.干冰升华时吸收大量的热,可用它做制冷剂或人工降雨
3.工业制纯碱和尿素,是一种重要的化工原料
4.植物光合作用,绿色植物吸收太阳能,利用二氧化碳和水,合成有机物放出氧气
二氧化碳中毒:
二氧化碳中毒是人吸入高浓度的二氧化碳所出现的昏迷及脑缺氧情况,一般大气中二氧化碳含量超过1%时,人即有轻度中毒反应;当超过3%时,开始出现呼吸困难;超过6%时,就会重度中毒甚至死亡。
(1)征状
中毒主要征状有:头痛、头愫晕、耳鸣、气急、胸闷、乏力、心跳加快,面颊发绀、烦躁、谵妄、呼吸困难,如情况持续,就会出现嗜睡、淡漠、昏迷、反射消失、瞳孔散大、大小便失禁、血压下降甚至死亡。
(2)补救
打开门窗、通风孔,抢救者才可进入。将病人救出后,在空气新鲜处进行人工呼吸,心脏按摩,吸氧(避免高压、高流量、高浓度给氧,以免呼吸中枢更为抑制),开始1~2L/分,随病人呼吸好转逐渐增大给氧量(4--5L/分),以至采用高压氧治疗。(最好是纯氧)
吸入兴奋剂:多种兴奋剂交替、联合使用,如洛贝林、山梗菜碱等。
防止脑和肺水肿:应用脱水剂、激素,限制液量和速度,吸入钠的份量亦应限制。
对症治疗:给予多种维生素、细胞色素C、能量合剂、高渗糖,以防感染。
抢救同时要留意有没有其他有毒气体存在,如一氧化碳等。
1.二氧化碳不支持燃烧,不能燃烧,比空气重,可用于灭火
2.干冰升华时吸收大量的热,可用它做制冷剂或人工降雨
3.工业制纯碱和尿素,是一种重要的化工原料
4.植物光合作用,绿色植物吸收太阳能,利用二氧化碳和水,合成有机物放出氧气
二氧化碳中毒:
二氧化碳中毒是人吸入高浓度的二氧化碳所出现的昏迷及脑缺氧情况,一般大气中二氧化碳含量超过1%时,人即有轻度中毒反应;当超过3%时,开始出现呼吸困难;超过6%时,就会重度中毒甚至死亡。
(1)征状
中毒主要征状有:头痛、头愫晕、耳鸣、气急、胸闷、乏力、心跳加快,面颊发绀、烦躁、谵妄、呼吸困难,如情况持续,就会出现嗜睡、淡漠、昏迷、反射消失、瞳孔散大、大小便失禁、血压下降甚至死亡。
(2)补救
打开门窗、通风孔,抢救者才可进入。将病人救出后,在空气新鲜处进行人工呼吸,心脏按摩,吸氧(避免高压、高流量、高浓度给氧,以免呼吸中枢更为抑制),开始1~2L/分,随病人呼吸好转逐渐增大给氧量(4--5L/分),以至采用高压氧治疗。(最好是纯氧)
吸入兴奋剂:多种兴奋剂交替、联合使用,如洛贝林、山梗菜碱等。
防止脑和肺水肿:应用脱水剂、激素,限制液量和速度,吸入钠的份量亦应限制。
对症治疗:给予多种维生素、细胞色素C、能量合剂、高渗糖,以防感染。
抢救同时要留意有没有其他有毒气体存在,如一氧化碳等。
混合物的分离和提纯(除杂)
1. 分离与提纯的基本原理
(1)分离:就是用物理或化学的方法将混合物巾的各组分分开,并将物质恢复到原状态。
(2)提纯和除杂:用物理或化学的方法把混合物中的杂质除去而得到纯物质。在提纯过程中,如果杂质发生了化学变化,不必恢复成原物质。二者的方法在很多情况下是相似的,但分离比提纯的步骤要多,因为各组分均要保留,绎过化学反应使混合物中各组分经转化而分离后还要复原为原来的组分物质提纯和除杂过程中经常用到分离操作,二者有时又密不可分。
2.分离和提纯应遵循的原则
(1)不能“玉石俱焚”:即试剂一般要求与杂质反应,不与要保留的物质反应。但在特殊情况下,所加试剂可和保留物质应应,但最终要转化成需要保留的物质如除去FeCl3,溶液中的NaCl,可加过量的NaOH溶液→过滤→洗涤→加适量稀盐酸。
(2)“不增““不减”:即不增加新的杂质,不减少要保留的物质如除去FeCl3中的少量Fe2(SO4)3应选用BaCl2而不应选用Ba(NO3)2,否则发生反应3Ba(NO3)2+Fe2(SO4)3==3BaSO4↓+2Fe(NO3)3溶液中又增加了Fe(NO3)3.
(3)易分离:反应后,物质的状态不同,便于分离。
(4)不污染环境:即耍求所选用的除杂方法不能产生可污染环境的物质。
(5)不能“旧貌变新颜”:即除杂结束前,要恢复保留物质的原有状态。
常见除杂的方法:
CO2(O2):将气体通过灼热的铜网
CO2(H2或CO):将气体通过灼热的氧化铜
O2或CO2或H2(含H2O):将气体通过浓硫酸或氧化钙或氯化钙等干燥剂
O2或H2或CO(含CO2或SO2):将气体通入氢氧化钠溶液中
Cu(含Fe或Mg或Zn):加入足量的稀盐酸或稀硫酸,过滤
Fe(含Cu):用磁铁将铁粉吸引出来
Cu(含CuO),Fe(含Fe2O3):高温下与H2或CO反应
CuO(含Cu或C):在空气中灼烧
CaO(含CaCO3):高温煅烧(CaCO3分解成CaO和CO2)
CaCO3(含CaO):加足量水溶解,过滤,取滤渣
Ca(OH)2(含CaO)加足量水
FeSO4溶液(含H2SO4或CuSO4),FeCl2溶液(含盐酸或CuCl2):加过量铁粉,过滤,取滤液
NaCl溶液(含Na2CO3):加适量稀盐酸
Na2SO4溶液(含CuSO4):加适量 NaOH 溶液
酸、碱、盐溶液的除杂技巧:
1.被提纯物与杂质所含阳离子相同时,选取与杂质中的阴离子不共存的阳离子,再与被提纯物中的阴离子组合出除杂试剂。如除去Na2SO4溶液中的NaOH:可选用稀H2SO4溶液为除杂试剂(2NaOH+ H2SO4==Na2SO4+2H2O)、除去KCl溶液中的 K2SO4:可选用BaCl2溶液为除杂试制(K2SO4+BaCl2 ==2KCl+BaSO4↓,过滤除去)
2.被提纯物与杂质所含阴离子相同时,选取与杂质中阳离子不共存的阴离子,再与被提纯物中的阳离子组合出除杂试剂,如除去NaCl溶液中的BaCl2:可选用 Na2SO4溶液为除杂试剂(BaCl2+Na2SO4=BaSO4↓ +2NaCl,过滤除去).再如除去KNO3溶液中的AgNO3:可选用KCl溶液为除杂试剂(AgNO3+KCl=AgCl↓ +KNO3,过滤除去)。
3.被提纯物质与杂质所含阴离子、阳离子都不相同时,应选取与杂质中阴、阳离子都不共存的阳、阴离子组合出除杂试剂。如:除去NaCl溶液中的CuSO4:可选用Ba(OH)2溶液为除杂试剂[CuSO4+Ba(OH)2= BaSO4↓+Cu(OH)2↓,过滤除去]。
分离和提纯的方法:
物质的分离和提纯有两种主要的方法,即物理方法和化学方法。实际上在实验过程中往往需通过综合法来进行。
(1)物理方法主要包括过滤,蒸馏,结晶
(2)化学方法
(3)综合法
在进行混合物的分离或提纯时,采用一种方法往往不能达到目的,而要采用几种方法才能完成,这就是综合法。综合法主要有三种:
①物理方法的综合:主要是溶解、过滤、蒸发、结晶等方法的结合:
②化学方法的综合:当某物质所含杂质不止一种时,通常需加入多种试剂除去(或分离)不同的物质。
③物理与化学方法的综合:当某物质所含杂质不止一种,且有能用物理方法除去(或分离)的杂质时,首先应考虑用物理方法除去一种或几种杂质,然后再用化学方法除去其余杂质。
(4)除杂方法的几个优化原则
①若同时有多种方法能除去杂质,要选择那些简单易行、除杂彻底的方法。
②应尽量选择既可除去杂质,又可增加保留物质的方法,即“一举两得”。
③先考虑物理方法,再用化学方法。
常见的混合物类型及分类与提纯的方法见下表:
1. 分离与提纯的基本原理
(1)分离:就是用物理或化学的方法将混合物巾的各组分分开,并将物质恢复到原状态。
(2)提纯和除杂:用物理或化学的方法把混合物中的杂质除去而得到纯物质。在提纯过程中,如果杂质发生了化学变化,不必恢复成原物质。二者的方法在很多情况下是相似的,但分离比提纯的步骤要多,因为各组分均要保留,绎过化学反应使混合物中各组分经转化而分离后还要复原为原来的组分物质提纯和除杂过程中经常用到分离操作,二者有时又密不可分。
2.分离和提纯应遵循的原则
(1)不能“玉石俱焚”:即试剂一般要求与杂质反应,不与要保留的物质反应。但在特殊情况下,所加试剂可和保留物质应应,但最终要转化成需要保留的物质如除去FeCl3,溶液中的NaCl,可加过量的NaOH溶液→过滤→洗涤→加适量稀盐酸。
(2)“不增““不减”:即不增加新的杂质,不减少要保留的物质如除去FeCl3中的少量Fe2(SO4)3应选用BaCl2而不应选用Ba(NO3)2,否则发生反应3Ba(NO3)2+Fe2(SO4)3==3BaSO4↓+2Fe(NO3)3溶液中又增加了Fe(NO3)3.
(3)易分离:反应后,物质的状态不同,便于分离。
(4)不污染环境:即耍求所选用的除杂方法不能产生可污染环境的物质。
(5)不能“旧貌变新颜”:即除杂结束前,要恢复保留物质的原有状态。
常见除杂的方法:
CO2(O2):将气体通过灼热的铜网
CO2(H2或CO):将气体通过灼热的氧化铜
O2或CO2或H2(含H2O):将气体通过浓硫酸或氧化钙或氯化钙等干燥剂
O2或H2或CO(含CO2或SO2):将气体通入氢氧化钠溶液中
Cu(含Fe或Mg或Zn):加入足量的稀盐酸或稀硫酸,过滤
Fe(含Cu):用磁铁将铁粉吸引出来
Cu(含CuO),Fe(含Fe2O3):高温下与H2或CO反应
CuO(含Cu或C):在空气中灼烧
CaO(含CaCO3):高温煅烧(CaCO3分解成CaO和CO2)
CaCO3(含CaO):加足量水溶解,过滤,取滤渣
Ca(OH)2(含CaO)加足量水
FeSO4溶液(含H2SO4或CuSO4),FeCl2溶液(含盐酸或CuCl2):加过量铁粉,过滤,取滤液
NaCl溶液(含Na2CO3):加适量稀盐酸
Na2SO4溶液(含CuSO4):加适量 NaOH 溶液
酸、碱、盐溶液的除杂技巧:
1.被提纯物与杂质所含阳离子相同时,选取与杂质中的阴离子不共存的阳离子,再与被提纯物中的阴离子组合出除杂试剂。如除去Na2SO4溶液中的NaOH:可选用稀H2SO4溶液为除杂试剂(2NaOH+ H2SO4==Na2SO4+2H2O)、除去KCl溶液中的 K2SO4:可选用BaCl2溶液为除杂试制(K2SO4+BaCl2 ==2KCl+BaSO4↓,过滤除去)
2.被提纯物与杂质所含阴离子相同时,选取与杂质中阳离子不共存的阴离子,再与被提纯物中的阳离子组合出除杂试剂,如除去NaCl溶液中的BaCl2:可选用 Na2SO4溶液为除杂试剂(BaCl2+Na2SO4=BaSO4↓ +2NaCl,过滤除去).再如除去KNO3溶液中的AgNO3:可选用KCl溶液为除杂试剂(AgNO3+KCl=AgCl↓ +KNO3,过滤除去)。
3.被提纯物质与杂质所含阴离子、阳离子都不相同时,应选取与杂质中阴、阳离子都不共存的阳、阴离子组合出除杂试剂。如:除去NaCl溶液中的CuSO4:可选用Ba(OH)2溶液为除杂试剂[CuSO4+Ba(OH)2= BaSO4↓+Cu(OH)2↓,过滤除去]。
分离和提纯的方法:
物质的分离和提纯有两种主要的方法,即物理方法和化学方法。实际上在实验过程中往往需通过综合法来进行。
(1)物理方法主要包括过滤,蒸馏,结晶
| 方法 | 适用范围 | 举例 | 注意事项 |
| 过滤 | 分离不溶性固体和液体 | 粗盐提纯 | ①过滤时要“一贴、二低,三靠”; ②必要时要洗涤沉淀物 |
| 结晶 | 利用混合物中各组分在某种溶剂中溶解度随温度变化不同的性质来分离提纯物质 | 分离氯化钠和硝酸钾混合物 | ①一般先配较高温度下的浓溶液,然后降温结晶: ②结晶后过滤,分离出晶体 |
| 蒸馏 | 沸点不同的液体混合物 | 石油的分馏 | ①温度计水银球在蒸馏烧瓶的支管口处; ②加沸石(或碎瓷片); ③冷凝管水流方向 |
(2)化学方法
| 除杂方法 | 除杂原理 | 应用实例 |
| 化气法 | 与杂质反应生成气体而除去 | 除Na2SO4中的NaCO3,可加适量稀盐酸 NaCO3+H2SO4==Na2SO4+CO2↑+H2O |
| 沉淀法 | 将杂质转化为沉淀过滤除去 | 除去NaCl中的Na2SO4.可加适量的BaCl2 Na2SO4+BaCl2==BaSO4↓+2NaCl |
| 置换法 | 将杂质通过置换反应而除去 | c除去FeSO4中的CuSO4可加过量的铁粉 CuSO4+Fe==Cu+FeSO4 |
| 溶解法 | 将杂质溶丁某种试剂而除去 | 除C粉中的CuO粉末,可加适量稀盐酸,再过滤 CuO+H2SO4==CuSO4+H2O |
| 加热法 | 杂质受热易分解,通过加热将杂质除去 | 除CaO中的CaCO3可加热 CaCO3  CaO+CO2↑ CaO+CO2↑ |
| 转化法 | 将杂质通过化学反应转化为主要成分 | 除去CO2中的CO,可将气体通过灼热的CuO CO+CuO  Cu+CO2 Cu+CO2 |
(3)综合法
在进行混合物的分离或提纯时,采用一种方法往往不能达到目的,而要采用几种方法才能完成,这就是综合法。综合法主要有三种:
①物理方法的综合:主要是溶解、过滤、蒸发、结晶等方法的结合:
②化学方法的综合:当某物质所含杂质不止一种时,通常需加入多种试剂除去(或分离)不同的物质。
③物理与化学方法的综合:当某物质所含杂质不止一种,且有能用物理方法除去(或分离)的杂质时,首先应考虑用物理方法除去一种或几种杂质,然后再用化学方法除去其余杂质。
(4)除杂方法的几个优化原则
①若同时有多种方法能除去杂质,要选择那些简单易行、除杂彻底的方法。
②应尽量选择既可除去杂质,又可增加保留物质的方法,即“一举两得”。
③先考虑物理方法,再用化学方法。
常见的混合物类型及分类与提纯的方法见下表:
| 混合物类型采用的方法 | 物理方法 | 化学方法 | |
| 固—固混合 | 可溶—可溶 | 结晶 | 把杂质变成沉淀、气体等除去 |
| 可溶—不溶 | 过滤 | —— | |
| 不溶—不溶 | — | 把杂质变成可溶物除去 | |
| 固—液混合 | 过滤 | —— | |
| 液—液混合 | —— | 把杂质变成沉淀,气体或被提纯物 | |
| 气—气混合 | —— | 把杂质变成固体、溶液或被提纯物 | |
发现相似题
与“某蔬菜基地在种植蔬菜时,常采用下列方法.(1)施用适量的氮...”考查相似的试题有:
- 下列各组物质中,在通常情况下不能发生化学反应的是A.铁与硫酸铜溶液B.氢氧化镁与稀盐酸C.碳酸钠与稀硫酸D.氮气和氧气
- 下列物质敞口露置于空气中,质量不变的是:A.氢氧化钠B.浓硫酸C.氯化钠D.浓盐酸
- 某同学在实验室配制了两瓶饱和溶液,一瓶是氢氧化钠溶液,一瓶是澄清的石灰水.由于忘了贴标签,下列方法或物质不能将二者区...
- 石灰石、生石灰、熟石灰在一定条件下可以发生如图所示转化关系.(1)生石灰是常用的干燥剂,其主要成分属于 (填序号).①酸...
- 尿素[CO(NH2)2]是一种常用的化肥,它可以促进植物的生长发育。下列说法正确的是[ ]A.尿素是一种复合化肥B.尿素中碳、氧、氮、...
- 如图是一种化肥包装袋上的部分说明,该化肥属于( ) 尿素CO(NH2)2净重:50千克含氮量:45.8%××化学工业公司A.氮肥B.磷肥...
- 在熟石灰、干冰、氧气三种物质中,可供给呼吸的是 ______,可用作致冷剂的是 ______,可用于改良酸性土壤的是 ______.
- 除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是( )选项物质(括号内为杂质)试剂操作方法AHCl( CO2)适量Na...
- 分别用一种试剂将下列物质中混入的少量杂质(括号中是混入的杂质)除去.物质加入的试剂有关化学方程式①HNO3(H2SO4)②Cu粉(...
- 为除去Na2SO4溶液中含有的杂质Na2CO3,甲、乙、丙三位同学分别选用一种试剂(适量)进行实验.请你对他们所选用的试剂进行评...