本试题 “下列说法正确的是( )A.△H>0、△S>0的反应在任何温度下都不能自发进行B.在滴有酚酞的Na2CO3溶液中,加入BaC12溶液后红色褪去C.测氯水的pH,可用干燥洁净...” 主要考查您对熵;熵变
酸碱中和滴定
pH值的测定
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 熵;熵变
- 酸碱中和滴定
- pH值的测定
在一定温度和压强下,无需外界帮助就能自动进行的过程叫做自发过程;在一定温度和压强下,无需外界帮助就可以自发进行到显著程度的化学反应叫自发反应。
化学反应方向的判据:
1.焓变对反应方向的影响:
△H<0 的化学反应也能自发进行。但有些△H>0的化学反应也能自发进行,也就是说,焓变是与化学反应能否自发进行有关的一个重要因素,但不是唯一的因素:
2.熵与熵变:
熵是用于描述体系混乱度的物理量,以符号S表示。熵值越大,体系的混乱度越大。
在一定条件下,不同物质的熵值不同;对同一物质来说,S(g)>S(l)>S(s),S(aq)>S(s)。
物质发生化学反应后熵值也发生变化,这个熵值的变化叫做反应的熵变,以符号△S表示,单位是
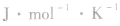 。
。△S=生成物总熵一反应物总熵
若△S为正值,表示反应过程中熵值增大,称为熵增过程;若△S为负值,表示反应过程中熵值减小,称为熵减过程。在与外界隔离的体系中,自发过程将导致体系的熵值增大,这个原理也叫做熵增原理。
3.熵变对反应方向的影响:
△S>0有利于化学反应的自发进行,有些△S>0 的化学反应在常温下不能自发进行,但在较高温度下可以自发进行,有些△S<0的化学反应也能自发进行。总之,熵变是与化学反应能否自发进行有关的一个重要因素,但不是唯一的因素。
4.焓变与熵变对反应方向的共同影响:
在温度和压强一定的条件下,化学反应的方向是反应的焓变和熵变共同影响的结果,反应方向的判据是
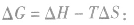
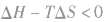 反应能自发进行
反应能自发进行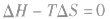 反应达到平衡状态
反应达到平衡状态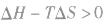 反应不能自发进行
反应不能自发进行酸碱中和滴定:
用已知物质的量浓度的酸(或碱)来测 定未知物质的量浓度的碱(或酸)的方法叫做酸碱中和滴定。
(1)原理:对于一元酸和一元碱发生的中和反应,C酸V酸=C碱V碱 或:C未知V未知=C标准V标准,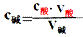
(2)仪器:a.酸式滴定管 b.碱式滴定管c.铁架台d.滴定管夹e.锥形瓶 f.烧杯g.胶头滴管等
(3)装置图: 
(4)操作步骤:
洗涤、检漏、水洗、润洗、装液、去泡、调液面记录、放待测液、加指示剂、滴定、记录、
计算、误差分析
(5)数据处理依据:
c(NaOH)=c(HCl)V(HCl)/V(NaOH)
(6)误差分析:
①仪器润洗不当:
a.盛标准液的滴定管用蒸馏水洗后未用标准液润洗;
b.盛待测液滴定(移液)管用蒸馏水洗后未用待测液润洗;
c.锥形瓶用蒸馏水洗后再用待测液润洗;
②读数方法有误:
a.滴定前仰视,滴定后俯视;
b.滴定前俯视,滴定后仰视;
c.天平或量筒的使用读数方法错误;
③操作出现问题:
a.盛标准液的滴定管漏液;
b.盛待测液的滴定管滴前尖嘴部分有气泡,终了无气泡
(或前无后有);
c.振荡锥形瓶时,不小心有待测液溅出;
d.滴定过程中,将标准液滴到锥形瓶外;
中和滴定中的误差分析:
中和滴定是一个要求较高的定量实验,每一个不当的或错误的操作都会引起误差。
对于一元酸与一元碱,由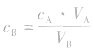 可知,
可知,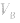 是准 确量取的体积,
是准 确量取的体积, 是标准溶液的浓度,它们均为定值,所以
是标准溶液的浓度,它们均为定值,所以 的大小取决于
的大小取决于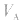 的大小,
的大小,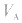 大则
大则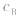 大,
大,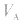 小则
小则 小。
小。
以标准酸溶液滴定末知浓度的碱溶液(酚酞作指示剂)为例,常见的不正确操作对实验结果的影响见下表: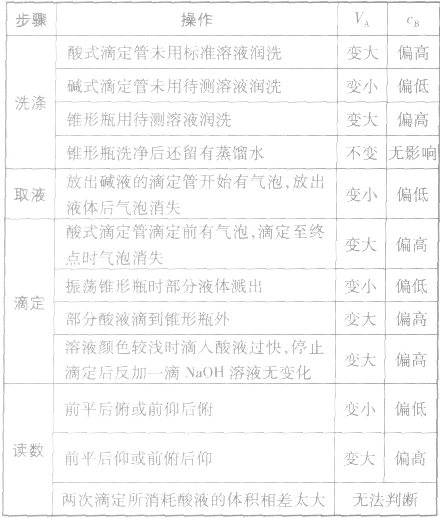
中和滴定应注意的问题:
1.中和滴定中指示剂的使用与选择
(1)用量不能太多,常用2~3滴,冈指示剂本身也是有机弱酸或有机弱碱,若用量太多,会使中和滴定中需要的酸或碱的量增多或减少。
(2)指示剂的选择:中和滴定时一般选用的指示剂有酚酞和甲基橙。石蕊试液由于颜色变化不明显,不易辨别,在滴定过程中不宜使用。
(3)酸、碱恰好完全反应时,终点溶液的pH应在指示剂的变色范围内,如强酸溶液滴定弱碱溶液应选用甲基橙作指示剂;强碱溶液滴定弱酸溶液应选用酚酞作指示剂。
(4)指示剂的变色:最好由浅到深,这样对比明显。如用强碱滴定强酸用酚酞作指示剂较好,当酚酞从无色变为粉红色(或浅红色)且半分钟内不褪色时即达到滴定终点。
2.欲减小实验误差的三点做法
(1)半分钟:振荡,半分钟内颜色不褪去,即为滴定终点。
(2)l一2min:滴定停止后,必须等待l~2min,让附着在滴定管内壁的溶液流下后,再进行读数。
(3)重复:同一实验,要做两到三次,两次滴定所用标准溶液的体积的差值不能超过0.02mL,再取平均值。
pH的测定:
1.酸碱指示剂法:只能粗略测定溶液的pH范围
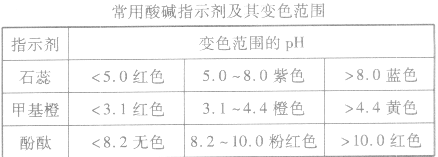
2.pH试纸法:用洁净的玻璃棒蘸取待测溶液点在一小片pH试纸(干燥的)的中部,变色后与标准比色卡对照,读出溶液的pH(粗略的整数值)。
3.pH计法(酸度计):能精确测定溶液的pH(精确到小数点后两位)。
与“下列说法正确的是( )A.△H>0、△S>0的反应在任何温度下都...”考查相似的试题有:
- 下列关于化学反应的熵变的叙述中,正确的是( )A.化学反应的熵变与反应的方向无关B.化学反应的熵变直接决定了反应的方向C...
- 当用酸滴定碱时,下列操作使测定结果(碱的浓度)偏高的是[ ]A.酸式滴定管滴至终点,俯视读数B.碱液移入锥形瓶后,加入10mL...
- 在氧化还原反应中,氧化过程和还原过程是同时发生的两个半反应.Cu2O-2e-+2H+═2Cu2++H2O是一个半反应式.下列五种物质FeSO4、...
- 下列各表述与示意图一致的是[ ]A.图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的量与加入NaOH溶液体积的关系...
- 某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:① 用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液...
- 下列有关化学实验操作合理的是( )①在配铜FeSO4溶液时常向其中加入一定量铁粉和稀硫酸②配制100mL 1.00mol/L的NaCl溶液时,可...
- 用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考下图,下列选项正确的是[ ]锥形瓶中的溶液 滴定管中的溶液选用指示剂选用滴...
- 为测定NaOH溶液的浓度,实验如下:用标准稀盐酸溶液进行滴定(1)配制100 mL 0.1000mol·L-1盐酸标准溶液所需仪器除量筒、小烧...
- 常温下,用0.1 mol·L-1的HCl溶液滴定a mL NaOH稀溶液。反应恰好完全时,消耗HCl溶液b mL。此时溶液中氢氧根离子的浓度c(OH-)...
- 下列有关实验原理或实验操作结论正确的是[ ]A. 配制酸性KMnO4溶液时,用盐酸酸化B. 用水湿润pH试纸测量某溶液的pH值C. 实验室...