本试题 “下列有关金属及其化合物的说法正确的是[ ]A.1L生理盐水(0.9%NaCl溶液)中含有9molNa+B.出土的古代铜制品表面覆盖着铜绿,其主要成分是CuOC.装修门窗使用...” 主要考查您对氧化铜
金属的焰色反应
合金
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化铜
- 金属的焰色反应
- 合金
氧化铜:
(1)物理性质:氧化铜是不溶于水的黑色固体(粉末),能溶于烯酸中,主要用于制造人造丝、陶瓷、釉、电池、杀虫剂,也用于制氢,做催化剂使用。
(2)化学性质:①氧化铜有金属氧化物的性质,常温下能与烯酸反应:CuO+2H+ Cu2++H2O
Cu2++H2O
②氧化铜具有氧化性,加热条件下可以与还原剂发生氧化还原反应:H2+CuO Cu+H2O
Cu+H2O
③氧化铜在高温下可发生分解反应:4CuO 2Cu2O+O2↑
2Cu2O+O2↑
(3)冶炼:一般通过加热分解Cu(OH)2的方式得到CuO,化学方程式为:Cu(OH)2 CuO+H2O
CuO+H2O
注意: 溶液中的Cu2+常为蓝色(浓CuCl2溶液呈绿色,稀CuCl2溶液呈蓝色),其颜色可作为Cu2+的判断依据。Cu2+与碱发生反应生成蓝色沉淀Cu(OH)2,其溶于氨水形成蓝色溶液。
氧化铜的特性:
| 气味 | 无味 |
| 颜色 | 黑色或者棕黑色 |
| 外观 | 无定形或结晶性粉末 |
| 性状 | 稍有吸湿性 |
| 相对质量 | 79.55 |
| 溶解性(水) | 不可溶 |
| 溶解度 | 不溶于水和乙醇,溶于酸、氯化铵及氰化钾溶液,氨溶液中缓慢溶解 |
| 稳定性 | 稳定 |
| 储存 | 密封干燥保存 |
| 用途 | 做有机反应的催化剂,制作人造丝和其他铜化合物等 |
氧化铜和氢氧化铜的性质比较:
名称
氧化铜
氢氧化铜
化学式
CuO
Cu(OH)2
物理性质
不溶水的黑色固体(粉末)
不溶于水的蓝色固体
化学性质
CuO+2H+
 Cu2++H2O
Cu2++H2O
CuO+H2 Cu+H2O
Cu+H2O
CuO+CO Cu+CO2
Cu+CO2Cu(OH)2+2H+  Cu2++2H2O
Cu2++2H2O
Cu(OH)2 CuO+H2O
CuO+H2O
Cu(OH)2+4NH3·H2O Cu(NH3)4(OH)2+4H2O
Cu(NH3)4(OH)2+4H2O
制法
Cu(OH)2
 CuO+H2O
CuO+H2OCu2++2OH-  Cu(OH)2↓
Cu(OH)2↓
例题:铜在自然界存在于多种矿石中,如:黄铜矿(CuFeS2)、斑铜矿(Cu5FeS4)、辉铜矿(Cu2S)、孔雀石(CuCO3·Cu(OH)2
请回答下列问题:
(1)、上表所列铜化合物中,铜的质量百分含量最高的是__Cu2S
)、工业上以黄铜矿为原料。采用火法熔炼工艺生产铜。改工艺的中间过程会发生反应:
2Cu2O+Cu2S 6Cu+SO2↑,反应的氧化剂是Cu2S和Cu2O
6Cu+SO2↑,反应的氧化剂是Cu2S和Cu2O
(3)、二氧化硫尾气直接排放到大气中造成环境污染的后果是形成酸雨,会对植物和建筑物等造成严重危害;该尾气可得到有价值的化学品,写出其中1中酸和1中盐的名称硫酸、硫酸钠。
(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需要进一步采用电解法精制。请简述粗铜电解得到精铜的大批量:以硫酸铜-硫酸溶液为电解质。电解时,粗铜(阳极)中的铜以及比铜活泼的金属失去电子进入溶液,不如铜活泼的金属沉入电解槽形成“阳极泥”;溶液中的Cu2+得到电子沉积在纯铜(阴极)上。
氧化铜与铜化合物之间的转换图:
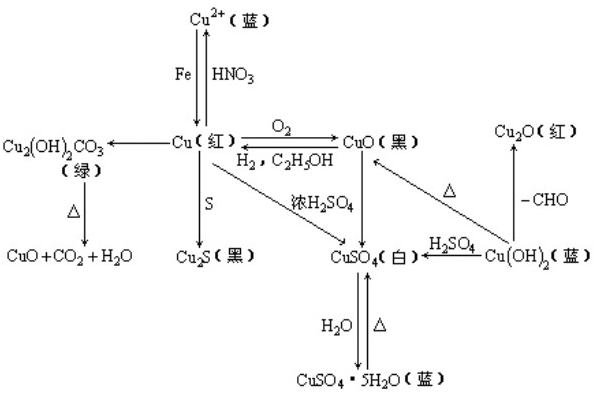
需要记住这些单质、化合物的颜色和状态,可以做为实验题的切入点。
知识扩展:
溶液中的Cu2+常为蓝色(浓CuCl2溶液呈绿色,稀CuCl2溶液呈蓝色),其颜色可作为Cu2+的判断依据。Cu2+与碱发生反应生成蓝色沉淀Cu(OH)2,其溶于氨水形成蓝色溶液。
反应方程为:CuCl2+2NaOH Cu(OH)2↓+2NaCl;Cu(OH)2+4NH3·H2O
Cu(OH)2↓+2NaCl;Cu(OH)2+4NH3·H2O Cu(NH3)4(OH)2+4H2O
Cu(NH3)4(OH)2+4H2O
(1)有些金属或它们的化合物在灼烧时会使火焰呈现出特色的颜色的想象。
(2)操作:
①洗:用盐酸洗去铂丝表面的杂质
②烧:将铂丝在酒精灯火焰上灼烧至于酒精灯颜色一致
③蘸:蘸取试样
④烧:在火焰上灼烧
⑤观:观察火焰颜色(若检验钾要透过钴玻璃观察)
(3)常见的颜色反应
Li Na K Ca Sr Ba Cu
紫红 黄 紫(透过蓝色钴玻璃片) 砖红 洋红 黄绿 绿
①焰色反应为物理变化过程。
②焰色现象与金属元素的存在有关,与物质组成无关。如:钠元素的焰色为黄色,包括钠单质以及钠的所有化合物。
合金的概念:
由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
合金的特性:
合金与各成分金属相比,具有许多优良的物理、化学和机械性能。
(1)合金的硬度一般比它的成分金属的大。
(2)合金的熔点一般比它的成分金属的低。
钢:
(1)钢和生铁同属于铁的合金。将铁矿石冶炼成生铁,生铁进一步冶炼可成为钢。
(2)钢是用量最大、用途最广的合金,按其化学成分可分为两大类:碳素钢和合金钢。
(3)碳素钢俗称普通钢。根据含碳量的多少,碳素钢又可以分为三类,见下表:
| 合金名称 | 含碳 | 主要性质 |
| 低碳钢 | <0.3% | 韧性、焊接性好,但强度低 |
| 中碳钢 | 0.3%~0.6% | 强度高,韧性及加工性好 |
| 高碳钢 | >0.6% | 硬而脆,热处理后弹性好 |
| 名称 | 其他主要合金元素 | 主要特性 | 主要用途 |
| 锰钢 | 锰 | 韧性好,硬度大 | 钢轨、轴承、钢磨、挖掘机铲斗、坦克装甲 |
| 不锈钢 | 铬、镍 | 抗腐蚀性好 | 医疗器械、容器、炊具等 |
| 硅钢 | 硅 | 导磁性好 | 变压器、发电机和电动机的铁芯 |
| 钨钢 | 钨 | 耐高温,硬度大 | 刀具 |
其他几种常见合金的主要成分,性能和用途:
| 合金 | 主要成分 | 主要性能 | 主要用途 |
| 球墨铸铁 | 铁,碳,硅,锰 | 机械强度好 | 在某些场合可代替钢 |
| 黄铜 | 铜,锌 | 强度高、可塑性 好、易加工、耐腐蚀 |
机器零件、仪表、日用品 |
| 青铜 | 铜,锡 | 强度高、可塑性好、 耐磨、耐腐蚀 |
机器零件如轴承、齿轮等 |
| 白铜 | 镍,铜 | 光泽好、耐磨、 耐腐蚀、易加工 |
钱币、代替银做饰品 |
| 焊锡 | 锡,铅 | 熔点低 | 焊接金属 |
| 硬铝 | 铝,铜,锰,镁,硅 | 强度和硬度好 | 火箭、飞机、轮船等制造业 |
| 钛合金 | 钛,铝,钒 | 耐高温、耐腐蚀、高强度 | 用于宇航、飞机、造船,化学工业 |
| 金合金 | 金,银,铜,稀土元素 | 有光泽、易加工、耐磨、耐腐蚀、易导电 | 金饰品、电子元件、钱币、笔尖 |
| Ti-Fe合金 | Ti,Fe | 室温下吸收H2快,且吸收H2量大,稍稍加热放H2速率快 | 储氢合金 |
合金的分类:
(1)铝合金:常见的有镁铝合金、硬铝等。硬铝密度小,强度高,具有较强的抗腐蚀能力,是制造飞机和字宙飞船的理想材料。
(2)铜合金
(3)
(4)新型合金:钛合金、耐热合金和形状记忆合金等。
几种有色金属材料的比较及新型金属材料:
1.金,银,铜的重要物理性质,性能及应用比较
| 金 | 银 | 铜 | ||
| 物理性质 | 颜色 | 黄色 | 银白色 | 紫红色 |
| 硬度 | Au<Ag<Cu | |||
| 延展性 | Au>Ag>Cu | |||
| 导电性 | Ag>Cu>Au | |||
| 导热性 | Ag>Cu>Au | |||
| 性能 | 极高的抗腐蚀性 | 催化,抗腐蚀性 | 在潮湿空气中易锈蚀 | |
| 应用 | 电子工业,航空,航天工业 | 有机合成,能源开发,医用材料制造 | 电气和电子工业,建筑材料 | |
2.新型金属材料
(1)铀(U)用作核电站反应堆的核燃抖
(2)镅(Am)在烟雾探测器中用作烟雾监测材料
(3)钛(Ti)被誉为“21世纪的金属”,是一种“亲生物金属”
金属资源的合理开发和利用:
1.合理开采矿物地球上的金属矿产资源是有限的,而且是不可再生的。随着人类不断地开发利用,矿产资源日渐减少,节约并合理地开采矿产资源是合理利用金属资源最直接,最基本水的措施
2.防止金属腐蚀金属制品在使用过程中会因腐蚀而损坏,每年因腐蚀造成的钢铁资源损失占当年总产量的10%以上,因此防腐是避免金属资源损失、浪费的重要手段
3.回收和利用废旧金属回收的废旧金属制品,大部分可以重新制成金属或它们的化合物,再进行使用。例如废旧钢铁可以用于炼钢;废铁屑可用于制铁盐
4.寻找金属替代品随着金属资源的目益减少,利用可再生资源开发、研制出新型材料代替金属材料的应用,是当今社会的一项重要科研课题,例如已经研制出并已实际运用的高硬度、耐高温材料;新型的替代钢铁的无机非金属材料料;有机化工合成的各种强度的橡胶、塑料,复合材料等
与“下列有关金属及其化合物的说法正确的是[ ]A.1L生理盐水(0.9...”考查相似的试题有:
- 黄铜矿(CuFeS2)是炼钢和炼铜的主要原料.在高温下灼烧生成二氰化二铁和氧化铜。三氧化二铁和氧化亚铜都是红色粉末.常用作...
- 下列说法中,正确的是A.利用铁加入硫酸铜溶液中的反应可以比较Cu、Fe2+的还原性B.足量的铜跟一定量的浓硝酸反应只产生一种...
- (6分)现有一种铜和铁的混合物样品。为测定该样品中铁的含量,某学生取10.0 g此样品置于烧瓶中,将80.0 mL稀硫酸分四次加入烧...
- ag铁粉与含有H2SO4的CuSO4溶液完全反应后,得到ag铜,则参与反应的CuSO4与H2SO4的物质的量之比为 ( )A.1 :7B.7 :1C.7 ...
- (12分)两组同学对铁及其化合物的性质进行探究。(1)一组同学用图1所示装置对铁与浓硫酸的反应进行实验。已知:2Fe + 6H2SO...
- 已知氯化铁溶液中通入硫化氢可发生反应:2FeCl3+H2S→2FeCl2+S↓+2HCl。在标准状况下,向 100mLFeCl3溶液中通入aL的H2S气体恰好...
- 亚铁盐在空气中易被氧化,但形成复盐可稳定存在。硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O]是一种重要化学试剂,实验室可用纯铁片来...
- 科学家冶炼出了纯度高达99.9999%的铁,你估计它不会具有的性质是A.在潮湿的空气中放置不易生锈B.硬度比生铁小C.与3 mol/L...
- 某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②氯化钠溶液、溴化钾、铜都是电解质;③冰和干冰既是纯净物又是化合...
- 美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )A.铝钠合...