本试题 “下列表述正确的是( ) A.7.8gNa202晶体中含有的离子总数为0.4NAB.C.二氧化硫、氨、煤的液化均为物理变化D.在鸡蛋白溶液中加入浓Na2SO4溶液,蛋白质的性质会...” 主要考查您对化学反应和物理变化
化学键与化学反应中能量变化的关系
乙醇
氨基酸
化学科学探究
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应和物理变化
- 化学键与化学反应中能量变化的关系
- 乙醇
- 氨基酸
- 化学科学探究
化学变化:在化学反应中,分子破裂成原子,原子重新排列组合生成新物质的过程,称为化学反应。在反应中常伴有发光发热变色生成沉淀物等现象。
物理变化:在物理变化中没有新物质生成,一般只是物质的形状或状态发生变化。
物质变化对比:
| 物理变化 | 化学变化 | |
| 特征 | 没有新物质生成 | 有新物质生成 |
| 实质 | 构成物质的粒子间隔发生变化,物质的组成、结构没有变化,无新物质生成 | 物质的组成、结构发生变化,物质中原子重新组合,有新物质生成 |
| 关系 | 化学变化中一定有物理变化,但物理变化中一定没有化学变化 | |
(1)化学变化中常伴随着发光、发热和颜色变化,但有发光、发热或颜色变化的变化不一定是化学变化,如在常压下将氧气冷却到-184℃时,O2变成淡蓝色的液体。
(2)原子的裂变、聚变中虽有新物质形成,但它不属于中学化学变化研究的范畴。
化学反应的实质:
判断一个反应是否为化学反应的依据是反应是否生成新的物质。化学反应的实质是旧键的断裂和新键的形成。
断开化学键要吸收能量,形成化学键要释放能量,通过化学键的键能可以计算断开化学键或形成化学键所需的能量。
反应热与键能的关系:
化学反应的热效应来源于化学反应过程中断裂旧化学键并形成新化学键时的能量变化。当破坏旧化学键所吸收的能量小于形成新化学键所释放的能量时,为放热反应;
当破坏旧化学键所吸收的能量大于形成新化学键所释放的能量时,为吸热反应。

若
 反应为放热反应;若
反应为放热反应;若 或
或 ,反应为吸热反应。
,反应为吸热反应。乙醇分子的组成与结构:
乙醇分子可以看成是乙烷分子中的一个氢原子被羟基(一OH)取代而形成的。乙醇分子的组成与结构见下表: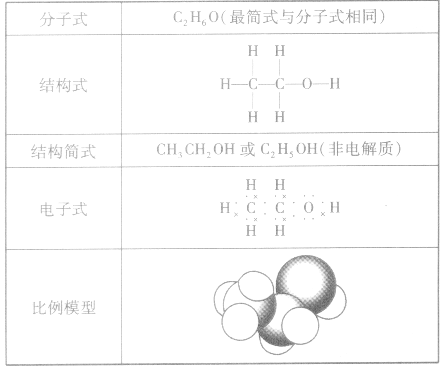
乙醇的性质:
(1)物理性质:俗称酒精,它在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有特殊的、令人愉快的香味,并略带刺激性。
(2)乙醇的化学性质:
①乙醇可以与金属钠反应,产生氢气,但不如水与金属钠反应剧烈。
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
活泼金属(钾、钙、钠、镁、铝)可以将乙醇羟基里的氢取代出来。
②乙醇的氧化反应:
2CH3CH2OH+O2→2CH3CHO+2H2O(条件是在催化剂Cu或Ag的作用下加热)
③乙醇燃烧:发出淡蓝色火焰,生成二氧化碳和水(蒸气),并放出大量的热,不完全燃烧时还生成一氧化碳,有黄色火焰,放出热量
完全燃烧:C2H5OH+3O2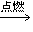 2CO2+3H2O
2CO2+3H2O
④乙醇可以和卤化氢发生取代反应,生成卤代烃和水。
C2H5OH+HBr→C2H5Br+H2O
注意:通常用溴化钠和硫酸的混合物与乙醇加热进行该反应。故常有红棕色气体产生。
⑤乙醇可以在浓硫酸和高温的催化发生脱水反应,随着温度的不同生成物也不同。
A. 消去(分子内脱水)制乙烯(170℃浓硫酸) C2H5OH→CH2=CH2↑+H2O (消去反应)
B. 缩合(分子间脱水)制乙醚(140℃ 浓硫酸) 2C2H5OH→C2H5OC2H5+H2O(取代反应)
有关醇类的反应规律:
1.消去反应的规律
总是消去和羟基所在碳原子相邻的碳原子上的氢原子,没有相邻的碳原子(如CH3OH)或相邻的碳原子上没有氢原子(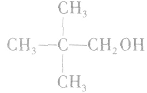 )就不能发生消去反应。能发生消去反应的醇的结构特点为:
)就不能发生消去反应。能发生消去反应的醇的结构特点为: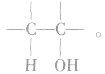
2.催化氧化反应的规律:
与羟基相连的碳原子上若有2个或3个氢原子,羟基则易被氧化为醛;若有1个氢原子,羟基则易被氧化为酮;若没有氢原子,则羟基一般不能被氧化。即
3.酯化反应的规律
醇与羧酸或无机含氧酸发生酯化反应,一般规律是“酸去羟基醇去氢”即酸脱去一OH,醇脱去一H。
例如: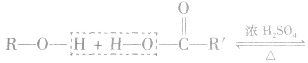

可用氧的同位素: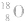 作为示踪原子来确定反应机理。如:
作为示踪原子来确定反应机理。如: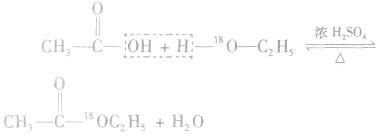
乙醇的工业制法:
(1)乙烯水化法:
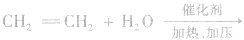
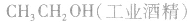
(2)发酵法:

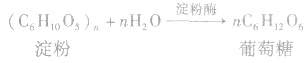
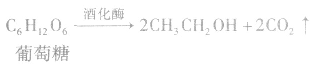
氨基酸的结构:
氨基酸是羧酸分子烃基上的氢原子被氨基取代的化合物。组成蛋白质的氢基酸几乎都是α一氨基酸,其结构简式为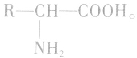
如甘氨酸(氨基乙酸):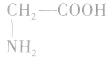
丙氨酸(α一氨基丙酸):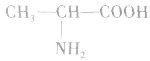
谷氨酸(2一氨基一1,5一戊二酸):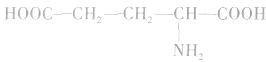
氨基酸的性质:
(1)物理性质天然的氨基酸均为无色晶体,熔点较高,在200~ 300℃熔化时分解。它们能溶于强酸或强碱溶液,除少数外一般都能溶于水,而难溶于乙醇、乙醚。
(2)化学性质
a.氨基酸的两性
氨基酸分子中一COOH是酸性基团,一NH2是碱性基因。因此,氨基酸是两性化合物,它既可以与酸反应,也可以与碱反应,且都生成盐。 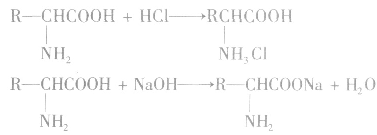
b.成肽反应
两个氨基酸分子(可以相同,也可以不同),在酸或碱的存在下加热,通过一分子的氨基与另一分子的羧基问脱去一分子水,缩合形成含有肽踺的化合物,称为成肽反应。由两个氨基酸分子脱水后形成的含有肽键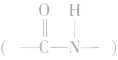 的化合物称为二肽。二肽还可以继续与其他氨基酸分子脱水生成三肽、四肽、五肽以至生成长链的多肽。
的化合物称为二肽。二肽还可以继续与其他氨基酸分子脱水生成三肽、四肽、五肽以至生成长链的多肽。
四个环节:查阅资料、提出假设、实验探究、结论分析
提出问题→猜想假设→制定计划→进行实验→收集证据→解释与结论→反思与评价 →表达与交流
与“下列表述正确的是( ) A.7.8gNa202晶体中含有的离子总数为0.4...”考查相似的试题有:
- 下例各组数值是相应元素的原子序数,其中所表示的原子能以离子键结合成稳定化合物的是A.1与6B.2与8C.9与11D.8与14
- 下列说法正确的是 ( )①离子化合物含离子键,也可能含极性键或非极性键②共价化合物含共价键,也可能含离子键③含金属元素的化...
- 下列叙述正确的是( )A.含有共价键的化合物一定是共价化合物B.气态单质分子中一定存在共价键C.共价化合物中一定存在共价...
- 下列叙述中正确的是A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件下和点燃条件下的AH不同B.常温下,反应2A(s)+B(g)=2C(g)+...
- 下列说法正确的是[ ]A.乙烯和苯都能发生加成反应B.乙醇和乙酸都能与氢氧化钠溶液反应C.淀粉和蛋白质水解产物都是氨基酸D.葡萄...
- 做葡萄糖被新制Cu(OH)2氧化的实验时,有以下步骤:①加入0.5 mL葡萄糖溶液;②加入2%CuSO4溶液4到5滴;③加入10% NaOH溶液2 mL...
- A.3B.2C.1D.不可计算
- 下列试剂不能令蛋白质变性的是( )A.Na2SO4溶液B.浓硝酸C.碘酒D.硫酸铜溶液
- 下列说法中正确的是:[ ]①只要能源充足而且价格低廉,废弃物中的原子都可以成为有用物质的原料②化学家能合成大量自然界中并不...
- 全世界每年因生锈损失的钢铁约占世界钢铁年产量的1/4。某学生想探究铁生锈的条件,他将干净的铁钉分别同时入放A、B、C三支试...