本试题 “下列有关实验的叙述中,正确的是( )A.用氨水不能鉴别Al(NO3)3、AgNO3、KNO3三种溶液B.图所示的装置可用于干燥、收集并吸收多余的氨气C.除去CO2中少量...” 主要考查您对二氧化硫
蔗糖
淀粉
氨气的制取
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 二氧化硫
- 蔗糖
- 淀粉
- 氨气的制取
①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:


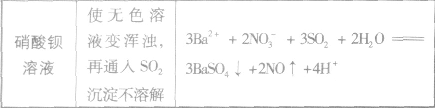
SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表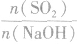 ,如下数轴所示:
,如下数轴所示: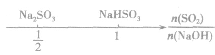
分析数轴可得:
(1)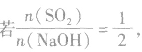 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2)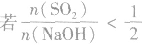 ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3)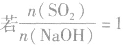 ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4)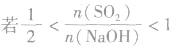 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5)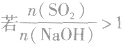 ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。
二氧化硫的制备:
工业制法:

实验室制法:
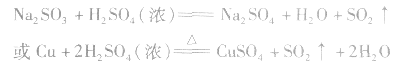
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

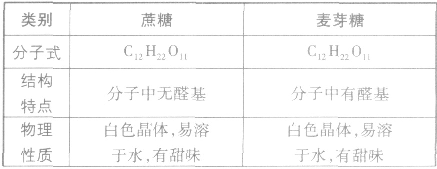
分子是为C12H22O11,与麦芽糖互为同分异构体。蔗糖水解生成一份子葡萄糖和一份子果糖。蔗糖存在甘蔗和甜菜中。蔗糖分子中没有醛基,不能与银氨溶液和新制氢氧化铜悬浊液反应,为非还原性糖。
蔗糖和麦芽糖:

淀粉的结构:
分子组成:
结构特点:由几百个到几千个单糖单元构成的高分子化合物。有直链及支链结构
淀粉的性质:
1、物理性质:无气味、无味道的粉末状物质,它不溶于冷水,在热水里淀粉颗粒会膨胀破裂,有一部分淀粉溶解在水里。另一部分淀粉悬浮在水里,形成胶状淀粉糊(即糊化作用)
2、化学性质:
①不与银氨溶液发生银镜反应,是一种非还原性糖
②在酸或酶的作用下发生水解,最终产物是葡萄糖,反应方程式为: 

③淀粉遇碘后显蓝色
淀粉水解程度的判断:
淀粉在酸或酶的作用下水解,最终生成葡萄糖。淀粉遇碘变蓝色,不能发生银镜反应;而产物葡萄糖遇碘不变蓝色,能发生银镜反应。依据这两种物质的性质,可用银氨溶液和碘水来检验淀粉是否水解或水解的程度。
实验步骤如下: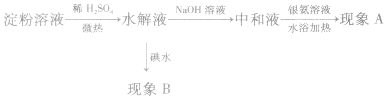
实验现象与结论见下表:
(1)实验室用氢氧化钙和氯化铵制取氨气
2NH4Cl+Ca(OH)2 CaCl2+2NH3+2H2O
CaCl2+2NH3+2H2O
(2)仪器:铁架台,铁夹,酒精灯,两个大试管,棉花;氯化铵固体,氢氧化钙固体。
(3)装置图: 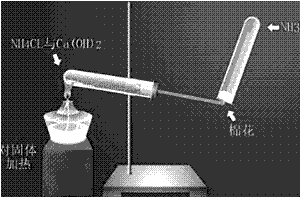
(4)注意:
a. 一般用Ca(OH)2,而不用NaOH,因NaOH碱性太强,对大试管腐蚀比Ca(OH)2强。
b. 选用Ca(OH)2时要检验消石灰是否变质, 因经过长期存放后消石灰部分变成碳酸钙,最好用新制的消石灰。
c. NH4CL与Ca(OH)2质量比5:8为宜,如用(NH4)2SO4代替NH4CL,则质量比为1:1,消石灰过量,以防止生成氨合物。
d. 试管口(盛固体药品的试管)要略向下倾斜;
e. 固体药品要平铺试管底部;
f.导出氨气的导管要短,收集氨气的导管要长,伸入试管底部;
g.为使氨气收集更多,防止空气中的水蒸汽进入收集氨气的试管,在试管口防一块,但不能堵死
h.酒精灯加热用外焰,先均匀加热,后对固体加热。
(5)收集方法: 用向下排气法取气法收集。因氨气极易溶于水,比空气轻。
干燥氨气: 用碱石灰,不能用浓硫酸和氯化钙干燥氨气。
检验氨气:用湿润的红色石蕊试纸,氨气能使湿润的红色石蕊试纸变蓝。
与“下列有关实验的叙述中,正确的是( )A.用氨水不能鉴别Al(N...”考查相似的试题有:
- (15分)为研究硫酸的性质,研究性学习小组设计以下两个实验。实验一:检查好装置的气密性后,在如图一所示甲的试管中加入足...
- 关于硫的叙述正确的是A.硫的非金属性较强,所以只以化合态存在于自然界B.分离黑火药中的硝酸钾、炭、硫要用到二硫化碳、水...
- “绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对环境的副作用,下列反应不符合这一理念的是()A.消除硝酸工...
- (6分)32g Cu与一定量的浓硫酸加热后,恰好完全反应,反应方程式如右: Cu + 2H2SO4CuSO4 + SO2↑+ 2H2O问:(1)得到SO2气体的体...
- 从物质A(某正盐)的水溶液出发有如下图所示的一系列变化。写出A、B、C、D、E、F的分子式: A____,B____,C____,D____, E____,F...
- 某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。请回答下列问题:(1)装置A中盛放亚硫酸钠的仪器名称是_______,其...
- 为除去混入CO2中的SO2和O2,下列试剂的使用顺序正确的是( )①饱和Na2CO3溶液 ②饱和NaHCO3溶液 ③浓H2SO4溶液 ④灼热铜网 ⑤...
- 下列为中学化学常见物质的相互反应关系图(生成物中H2O 均未列出)。A、B、C、G都属于氧化物,A为固体、B为液体、C、E、G为气体...
- 使用类似数轴的方法研究一些化学问题可以收到的直观形象的效果。下列表达正确的A.Fe在Cl2中的燃烧产物:B.氨水与SO2反应后...
- 将淀粉浆和淀粉酶的混合物放入半透膜袋中,扎好后浸入流动的温水中,经过足够长的时间,取出袋内的液体,分别与①碘水 ②新制C...