本试题 “甲、乙两池的电极材料都是铁棒与碳棒(如下图)。请回答下列问题(1)若两池中均盛放CuSO4溶液,反应一段时间后:①有红色物质析出的是:甲池中的________棒;乙池...” 主要考查您对原电池原理的应用
电解池电极反应式的书写
电解饱和氯化钠溶液
电化学有关的计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原电池原理的应用
- 电解池电极反应式的书写
- 电解饱和氯化钠溶液
- 电化学有关的计算
(1)根据形成原电池判断金属的活动性根据活泼金属为负极,不活泼金属为正极,可通过组成原电池判断金属活动性。
(2)形成原电池可以加快反应速率纯锌与稀H2SO4反应速率较慢,当加入CuSO4溶液以后,反应速率加快,因为Zn+Cu2+=Cu+Zn2+析出的Cu与Zn接触,在稀H2SO4中形成原电池,加快反应速率。
(3)根据原电池原理可以判断电池的正负极、电解质溶液、判断溶液pH的变化
(4)根据原电池原理可以保护金属不被腐蚀
(5)判断金属腐蚀程度的快慢
原电池原理的应用:
1.比较不同金属的活动性强弱
根据原电池原理可知,在原电池反应过程中,一般活动性强的金属作负极,而活动性弱的金属(或能导电的非金属)作正极。
若有两种金属A和B,用导线将A和B连接后,插入到稀硫酸中,一段时间后,若观察到A极溶解,而B 极上有气体放出,说明在原电池工作过程中,A被氧化成阳离子而失去电子作负极,B作正极,则金属A的金属活动性比B强。
2.加快氧化还原反应的速率
因为形成原电池后,产生电位差,使电子的运动速率加快,从而使反应速率增大,如Zn与稀H2SO4反应制氧气时,可向溶液中滴加少量CuSO4溶液,形成Cu—Zn原电池,加快反应速率 3.用于金属的防护要保护一个铁制闸门,可用导线将其与一锌块相连,使锌作原电池的负极,铁制闸门作正极。
4.设计制作化学电源设计原电池时要紧扣构成原电池的条件。
(1)首先要将已知氧化还原反应拆分为两个半反应:
(2)然后根据原电池的电极反应特点,结合两个半反应找出正、负极材料(一般负极就是失电子的物质,正极用比负极活泼性差的金属或导电的非金属)及电解质溶液:
①电解质溶液的选择电解质溶液一般要能够与负极发生反应,或者能与电极产物发生反应。但如果两个半反应分别在两个容器中进行(中间连接盐桥),左右两个容器中的电解质溶液应选择与电极材料相同的阳离子。如在铜一锌一硫酸铜构成的原电池中,负极金属锌浸泡在含有 Zn2+“的电解质溶液中,而正极铜浸泡在含有Cu2+的溶液中.
②电极材料的选择在原电池中,选择较活泼的金属或还原性较强的物质作为负极,较不活泼的金属或能导电的非金属或氧化性较强的物质作为正极。一般,原电池的负极能够与电解质溶液反应,容易失去电子,因此负极一般是活泼的金属材料(也可以是还原性较强的非金属材料如H2、CH4等)。
(3)举例根据以下反应设计原电池: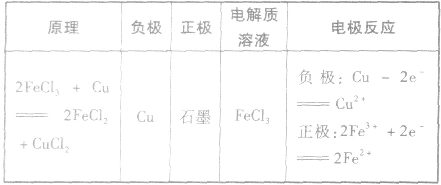
1.根据装置书写电极反应式
(1)根据电源确定阴、阳两极→确定阳极是否是活性电极→据电极类型及电解质溶液中阴、阳离子的放电顺序写出电极反应式。
(2)在确保阴、阳两极转移电子数目相同的条件下,将两极电极反应式合并即得总反应式。
2.由氧化还原反应方程式书写电极反应式
(1)找出发生氧化反应和还原反应的物质→确定两极名称和生成物→利用电子守恒分别写出两极反应式。
(2)若写出一极反应式,而另一极反应式不好写,可用总反应式减去已写出的电极反应式,即得另一电极反应式。
在小烧杯(或U型管)里装入饱和食盐水,滴入几滴酚酞试液。用导线把碳棒、电池、电流表和铁钉相连(如图)。接通直流电源后,注意观察电流表的指针是否偏转,以及小烧杯内发生的现象,并用湿润的碘化钾淀粉试纸检验阳极放出的气体。
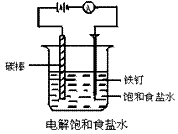
注:粗铁钉要与直流电源的阴极相连,碳棒与阳极相连。
用玻璃棒沾湿润的KI淀粉试纸检验阳极气体。
(1)饱和食盐水电解时,电流表指针发生偏转,阴、阳极均有气体放出,阳极气体有刺激性气味,并能使湿润的KI淀粉试纸变蓝,且阴极区溶液变红。
(2) 阳极:2Cl--2e-==Cl2↑
阴极:2H++2e-==H2↑(或2H2O+2e-==2OH-+H2↑)
总反应式:2NaCl+2H2O
 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑ (3)阴极区溶液变红的原因:这是由于饱和食盐水中,水所电离出的H+在阴极放电,破坏了水的电离平衡
(H2O
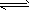 H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。
H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。 (4)例用电解饱和食盐水溶液可制取氢气、氯气和烧碱。
电化学计算的基本方法和技巧:
原电池和电解池的计算包括两极产物的定量计算、溶液的pH计算、相对原子质量的计算,根据电量求产物的量或根据产物的量求电量等。通常有下列三种方法。
1.根据电子守恒法
计算用于串联电路中阴、阳两极产物或正、负两极产物的量的计算,其依据是电路中转移的电子数相等。
2.根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列比例式计算。
3.根据关系式计算
运用得失电子守恒建立已知量与未知量之间的关系式。如以通过4mole一为桥梁可构建电极产物之间的如下关系式: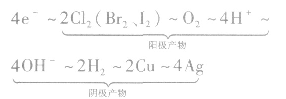
该关系式具有总揽电化学计算的作用和价值,熟记电极反应式,灵活运用这个关系式便能快速解答常见的电化学计算问题。
特别提醒:在电化学计算中,还常利用 和
和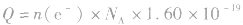 来计算电路中通过的电量。
来计算电路中通过的电量。
与“甲、乙两池的电极材料都是铁棒与碳棒(如下图)。请回答下列问...”考查相似的试题有:
- 下列关于原电池的叙述中,正确的是A.原电池中,正极就是阳极,负极就是阴极B.原电池工作时,在负极上发生氧化反应C.原电池...
- 下列有关原电池的说法不正确的是A.锌锰干电池中锌电极是负极,工作时锌被还原B.锌与稀硫酸反应时,加入少量硫酸铜溶液可使...
- 下列各反应属于原电池反应的是A.氧化铝膜破坏后,金属铝被迅速氧化B.锌与稀硫酸反应中加入少量CuSO4溶液,反应放出H2的速率...
- 根据下图,下列判断中正确的是A.烧杯a中的溶液H+增大B.烧杯b中发生氧化反应C.烧杯a中发生的反应为:2H++2e-=H2D.烧杯b中...
- 下列说法正确的是( )A.吸热反应一定是反应物能量低于生成物能量B.由于燃料的燃烧是一次性的,所以燃料电池属于一次电池C...
- 研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:。下列“水...
- 把a、b、c、d四块金属片浸人稀酸中,用导线两两相连组成原电池。若a、b相连时,a为负极,c、d相连时,电流由d到c;a、c相连时...
- 以惰性电极电解足量CuSO4和FeSO4溶液,若在阳极上产生气体的的体积在标准状况下为2.24L,则阴极上析出的固体的质量为A.6.4gB...
- 右图装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中所列各项对应关系均正确的一组是:选项电源X极实验前U形 管...
- 电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72—+6Fe2++14H+2Cr3++6Fe3++7...