本试题 “下列说法正确的是[ ]A. 用甘氨酸()和丙氨酸()缩合最多可形成4种二肽B. 0.1 mol/L Na2S溶液中:c(OH-)= c(H+)+ c(HS-)+ c(H2S)C. 标准状况下,2.2...” 主要考查您对氧化还原反应的配平
阿伏加德罗常数
粒子浓度大小的比较
氨基酸
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化还原反应的配平
- 阿伏加德罗常数
- 粒子浓度大小的比较
- 氨基酸
配平简介:
化学反应方程式严格遵守质量守恒定律,书写化学反应方程式写出反应物和生成物后,往往左右两边各原子数目不相等,不满足质量守恒定律,这就需要通过配平来解决。
配平原则:
(1)电子守恒原则:反应中还原剂失去电子的总数与氧化剂得到电子的总数相等
(2)电荷守恒原则:若为离子反应,反应前后离子所带正负电荷总数相等
(3)质量守恒原则:反应前后各元素的原子个数相等
配平步骤:
(1)一标:标明反应前后化合价有变化的元素的化合价
(2)二等:通过求最小公倍数使化合价升降总值相等
(3)三定:确定氧化剂与还原剂的化学计量数
氧化剂(还原剂)化学计量数=降(升)价的最小公倍数÷1mol氧化剂(还原剂)降(升)价总数
(4)四平:用观察法配平其他物质的化学计量数
(5)五查:检查质量与电荷、电子是否分别守恒
配平技巧:
(1)逆向配平法:部分氧化还原反应、自身氧化还原反应等可用逆向配平法,即选择氧化产物、还原产物为基准物来配平(一般从反应物很难配平时,可选用逆向配平法)
例:
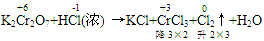
通过表明氧化产物、还原产物化合价的升降,确定CrCl3、Cl2的计量数为2和3,然后再用观察法配平。
(2)设“1”配平法:设某一反应物或生成物(一般选用组成元素较多的物质作基准物)的化学计量数为1,其余各物质的化学计量数可根据原子守恒原理列方程求得。
例:P4O+Cl2→POCl3+P2Cl6
可令P4O前的系数为1,Cl2的系数为x,则
1P4O+xCl2→POCl3+3/2P2Cl6 ,再由Cl原子守恒得2x=3+3/2×6 得x=6 即可配平
(3)零价配平法:先令无法用常规方法确定化合价的物质中各元素均为零价,然后计算出各元素化合价的升降值,并使元素化合价升降总数相等,最后用观察法配平其他物质的化学计量数。
例:Fe3C+HNO3=Fe(NO3)3+CO2↑+NO2↑+H2O
复杂化合物Fe3C按照常规方法分析,无法确定其Fe和C的具体化合价,此时可令组成物质的各元素化合价为零价,根据化合价升降法配平。
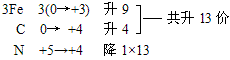
再用观察法确定物质的化学计量数。
(4)整体标价法:当某元素的原子在某化合物中有数个时,可将它作为一个整体对待,根据化合物中元素化合价代数和为零原则予以整体标价。
例:S+Ca(OH)2→CaSx+Ca2S2O3+H2O
生成物CaSx、Ca2S2O3中的Sx、S2作为一个整体标价为-2、+4价,则化合价升降关系为:
Sx 0→-2 降2×2
S2 0→+4 升4×1
即可配平。
(5)缺项配平法:一般先确定氧化剂、还原剂、氧化产物、还原产物的化学计量系数,再通过比较反应物与生成物,确定缺项(一般为H2O、H+或OH-),最后观察配平。
(6)有机氧化还原反应的配平:有机物中元素的化合价一般来讲,氢元素显+1价,氧元素显-2价,然后再根据化合价的代数和为零求酸碳元素的平均化合价。
氧化还原反应方程式配平的一般方法与步骤:
- 一般方法:从左向右配。
- 步骤:标变价,找变化,求总数,配系数。
- 标出元素化合价变化的始态和终态
- 求升价元素或降价元素化合价的变化数
- 求化合价变化数的最小公倍数,分别作为氧化剂或还原剂的系数
- 配平变价元素
- 用观察法配平其他元素
- 检查配平后的方程式是否符合质量守恒定律(离子方程式还要看电荷是否守恒)
如: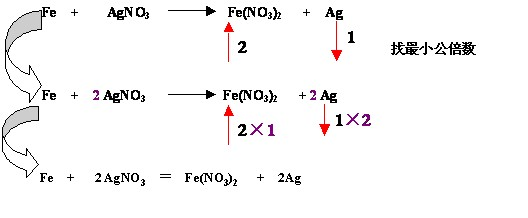
特殊技巧:
配平时若同一物质内既有元素的化合价上升又有元素的化合价下降,若从左向右配平较困难,可以采用从右向左配平,成为逆向配平法。
阿佛加德罗常数:
1mol粒子集体所含离子数与0.012kg碳12中所含的碳原子数相同,约为6.02×1023。
把1mol任何粒子的粒子数叫阿伏加德罗常数。
符号:NA,通常用6.02×1023mol-1表示
阿佛加德罗常数的单位:
阿佛加德罗常数是有单位的量,其单位是:mol-1,需特别注意。
阿佛加德罗常数的正误判断:
关于阿伏加德罗常数(NA)的考查,涉及的知识面广,灵活性强,是高考命题的热点。解答该类题目时要细心审题,特别注意题目中的关键性字词,留心“陷阱”。主要考查点如下:
1.考查“标准状况”、“常温常压”等外界条件的应用
(1)在标准状况下非气态物质:如H2O、SO3、戊烷、CHCl3、CCl4、苯、乙醇等,体积为22.4L时,其分子数不等于NA。
(2)注意给出气体体积是否在标准状况下:如11.2LH2的分子数未必是0.5NA。
(3)物质的质量、摩尔质量、微粒个数不受外界条件的影响。
2.考查物质的组成
(1)特殊物质中所含微粒(分子、原子、电子、质子、中子等)的数目:如Ne、D2O、18O2、H37Cl、—OH等。
(2)某些物质的阴阳离子个数比:如NaHSO4晶体中阴、阳离子个数比为1∶1,Na2CO3晶体中阴、阳离子个数比为1∶2。
(3)物质中所含化学键的数目:如H2O2、CnH2n+2中化学键的数目分别为3、3n+1。
(4)最简式相同的物质中的微粒数目:如NO2和N2O4,乙烯和丙烯等。
3.考察氧化还原反应中电子转移的数目
如:Na2O2、NO2与H2O的反应;Cl2与H2O、NaOH溶液、Cu或Fe的反应;电解AgNO3溶液、NaCl溶液等。
4.考查弱电解质的电离及盐的水解
如1L0.1mol/L的乙酸溶液和1L0.1mol/L的乙酸钠溶液中的CH3COO-的数目不相等且都小于0.1NA;1L0.1mol/L的NH4NO3溶液中c(NH4+)<0.1mol/L,但含氮原子总数仍为0.2NA;1molFeCl3水解生成Fe(OH)3胶粒的数目远远小于NA。
5.考查一些特殊的反应
如, 1molN2与3H2反应实际生产中得不到2molNH3,因是可逆反应;标准状况下2.24LO2和2.24LNO混合后,由于发生:2NO+O2==2NO2和
1molN2与3H2反应实际生产中得不到2molNH3,因是可逆反应;标准状况下2.24LO2和2.24LNO混合后,由于发生:2NO+O2==2NO2和![]() 两个反应,使2.24L<V<3.36L。
两个反应,使2.24L<V<3.36L。
有关NA的问题中常见的几种特殊情况:
有关NA的问题分析中易忽视如下问题而导致错误:
(1)碳原子超过4个的烃类物质、标准状况下的SO3等均不是气体,不能使用“22.4L/mol”来讨论问题。
(2)Na2O2由Na+和O22-构成,而不是由Na+和O2-构成,阴阳离子个数比为1:2而不是1:1.
(3)SiO2结构中只有原子无分子,1molSiO2中含有共价键数为4NA
离子浓度大小比较方法:
(1)考虑水解因素:如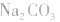 溶液
溶液 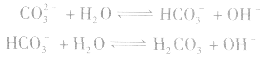
所以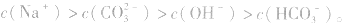
(2)不同溶液中同一离子浓度的比较要看溶液中其他离子对它的影响。如相同浓度的
 三种溶液中,
三种溶液中, 由大到小的顺序是c>a>b。
由大到小的顺序是c>a>b。
(3)混合液中各离子浓度的比较要综合分析水解因素、电离因素。如相同浓度的 的混合液中,离子浓度顺序为:
的混合液中,离子浓度顺序为: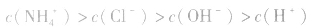
 的电离程度大于
的电离程度大于 的水解程度。
的水解程度。
盐溶液的“三大守恒”:
①电荷守恒:电解质溶液中所有阳离子所带有的正电荷数与所有的阴离子所带的负电荷数相等。如NaHCO3溶液中:
推出: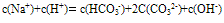
②物料守恒:电解质溶液中由于电离或水解因素,离子会发生变化变成其它离子或分子等,但离子或分子中某种特定元素的原子的总数是不会改变的。如NaHCO3溶液中nc(Na+):nc(C)=1:1,
推出: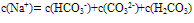
③质子守恒:电解质溶液中分子或离子得到或失去质子(H+)的物质的量应相等。例如在NH4HCO3溶液中H3O+、H2CO3为得到质子后的产物;NH3、OH-、CO32-为失去质子后的产物,故有以下关系: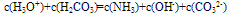
(2)粒子浓度大小比较的方法:
①单一溶液中离子浓度大小的比较
A. 一元弱酸盐溶液中离子浓度的关系是:
c(不水解离子)>c(水解离子)>c(显性离子)>c(水电离出的另一离子)
如:在CH3COONa溶液中各离子浓度大小关系: 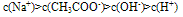
B. 二元弱酸盐溶液中离子浓度的关系是:
c(不水解离子)>c(水解离子)>c(显性离子)> c(二级水解离子)>c(水电离出的另一离子)
如:Na2CO3溶液中离子浓度的关系: 
②比较不同电解质溶液中同一种粒子浓度的大小。应注意弱酸、弱碱电离程度的大小以及影响电离度的因素,盐类水解及水解程度对该粒子浓度的影响。
③比较经过反应化学反应后离子浓度的大小:
A. 确定电解质溶液的成分
B. 确定溶液中含哪些粒子(分子、离子),此时要考虑物质的电离和水解情况
C. 确定各种粒子的浓度或物质的量的大小
D. 根据题目要求做出判断
注:要抓住“两小”。即弱电解质电离程度小,故未电离的弱电解质分子数远多于已电离出离子数目;盐的水解程度小,故未水解的粒子数目远多于水解生成的粒子数目
氨基酸的结构:
氨基酸是羧酸分子烃基上的氢原子被氨基取代的化合物。组成蛋白质的氢基酸几乎都是α一氨基酸,其结构简式为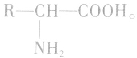
如甘氨酸(氨基乙酸):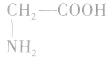
丙氨酸(α一氨基丙酸):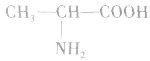
谷氨酸(2一氨基一1,5一戊二酸):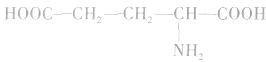
氨基酸的性质:
(1)物理性质天然的氨基酸均为无色晶体,熔点较高,在200~ 300℃熔化时分解。它们能溶于强酸或强碱溶液,除少数外一般都能溶于水,而难溶于乙醇、乙醚。
(2)化学性质
a.氨基酸的两性
氨基酸分子中一COOH是酸性基团,一NH2是碱性基因。因此,氨基酸是两性化合物,它既可以与酸反应,也可以与碱反应,且都生成盐。 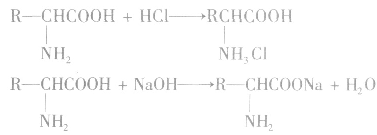
b.成肽反应
两个氨基酸分子(可以相同,也可以不同),在酸或碱的存在下加热,通过一分子的氨基与另一分子的羧基问脱去一分子水,缩合形成含有肽踺的化合物,称为成肽反应。由两个氨基酸分子脱水后形成的含有肽键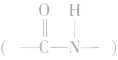 的化合物称为二肽。二肽还可以继续与其他氨基酸分子脱水生成三肽、四肽、五肽以至生成长链的多肽。
的化合物称为二肽。二肽还可以继续与其他氨基酸分子脱水生成三肽、四肽、五肽以至生成长链的多肽。
与“下列说法正确的是[ ]A. 用甘氨酸()和丙氨酸()缩合最多可...”考查相似的试题有:
- 常温下,在下列溶液中发生如下反应①16H++10Z-+2XO4-→2X2++5Z2+8H2O ②2A2++B2→2A3++2B- ③2B-+Z2→B2+2Z-由此判断下列说法错误的...
- 亚硝酸钠(NaNO2)具有致癌作用,许多腌制食品中含NaNO2.酸性KMnO4溶液与亚硝酸钠发生的离子反应为MnO4-+NO2-+H+-→Mn2++NO3-...
- 依据离子反应:1N2H5++4Fe3+===4Fe2++aY+……(a是配平后Y的系数),在水溶液中N2H5+将Fe3+还原为Fe2+,则N2H5+被氧...
- (6分)在反应Fe3O4+4CO3Fe+4CO2中, 是氧化剂, 元素被氧化,氧化产物和还原产物的物质的量之比为 ,若生成的CO2在标准状...
- 设阿伏加德罗常数的值为NA,则下列说法不正确的是[ ]A.氯气参加氧化还原反应时电子转移2NAB.与所含有的氧原子数相等C.与足...
- 燃烧FeS2生成Fe2O3和SO2,转移电子总数为m个,生成SO2n mol,则阿伏加德罗常数为[ ]A、8m/11nB、4m/11nC、2m/11nD、m/11n
- 下列浓度关系正确的是[ ]A.氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO-)]B.氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)C.等体积等...
- 现有A、B、C、D、E五种可溶强电解质,它们在水中可电离产生下列离子(各种离子不重复)。已知:①A、B两溶液呈碱性;C、D、E溶...
- 下列关于蛋白质的叙述中,不正确的是( )A.向蛋白质溶液里加(NH4)2SO4溶液可提纯蛋白质B.在豆浆中加入少量的石膏,能使豆...
- 下列关于蛋白质的叙述中,不正确的是( ) A.蛋白质水解的最终产物为葡萄糖 B.酒精消毒的原理是酒精能使蛋白质变性 C.重金...