本试题 “下列有关实验的说法正确的是( )A.用pH试纸蘸取NaOH溶液,立刻与比色卡对比,测定NaOH溶液的pHB.通过观察图中导管水柱的变化,验证铁钉生锈的原因主要是吸...” 主要考查您对盐类水解判断溶液酸碱性或比较溶液pH值的大小
金属的电化学腐蚀
金属的化学腐蚀
金属的电化学防护
金属的表面防护
基本仪器的使用
pH值的测定
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 盐类水解判断溶液酸碱性或比较溶液pH值的大小
- 金属的电化学腐蚀
- 金属的化学腐蚀
- 金属的电化学防护
- 金属的表面防护
- 基本仪器的使用
- pH值的测定
(1)盐水解的规律:
①谁弱谁水解,谁强显谁性,越弱越水解,都弱都水解,无弱不水解
②多元弱酸根、正酸根离子比酸式酸根离子水解程度大得多,故可只考虑第一步水解
(2)具体分析一下几种情况:
①强碱弱酸的正盐:弱酸的阴离子发生水解,水解显碱性;如:Na2CO3、NaAc等
②强酸弱碱的正盐:弱碱的阳离子发生水解,水解显酸性;如:NH4Cl、FeCl3、CuCl2等;
③强酸强碱的正盐,不发生水解;如:Na2SO4、NaCl、KNO3等;
④弱酸弱碱的正盐:弱酸的阴离子和弱碱的阳离子都发生水解,溶液的酸碱性取决于弱酸和弱碱的相对强弱,谁强显谁性;
⑤强酸的酸式盐只电离不水解,溶液显酸性,如:NaHSO4;而弱酸的酸式盐,既电离又水解,此时必须考虑其电离和水解程度的相对大小:若电离程度大于水解程度,则溶液显酸性,如:NaHSO3、NaH2PO4;若水解程度大于电离程度,则溶液显碱性,如:NaHCO3、NaHS、Na2HPO4等。
(3)几种盐溶液pH大小的比较强酸强碱盐pH=7、强碱弱酸盐pH>7、强酸弱碱盐pH<7
根据其相应的酸的酸性大小来比较,盐溶液对应的酸的酸性越强,其盐溶液的pH越小如:HClO酸性小于H2CO3,溶液pH NaClO>Na2CO3
酸式盐溶液酸碱性的判断:
酸式盐的水溶液显什么性,要看该盐的组成微粒。
1.强酸的酸式盐只电离,不水解,溶液一定显酸性。如 溶液:
溶液: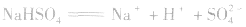
2.弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。
(1)若电离程度小于水解程度,溶液显碱性。例如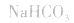 溶液中:
溶液中: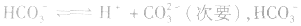
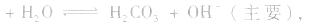
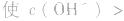
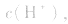 溶液显碱性。NaHS溶液、Na2HPO4溶液亦显碱性
溶液显碱性。NaHS溶液、Na2HPO4溶液亦显碱性
(2)若电离程度大于水解程度,溶液显酸性。例如 溶液中:
溶液中: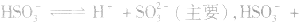
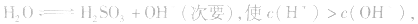 溶液显酸性
溶液显酸性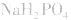 溶液亦显酸性。
溶液亦显酸性。
盐溶液蒸干后所得物质的判断:
1.考虑盐是否分解。如加热蒸干 溶液,因
溶液,因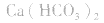 分解,所得固体应是
分解,所得固体应是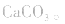
2.考虑氧化还原反应。如加热蒸干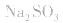 溶液,因
溶液,因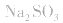 易被氧化,所得固体应是
易被氧化,所得固体应是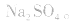
3.盐水解生成挥发性酸时,蒸干后一般得到弱碱,如蒸干 溶液,得
溶液,得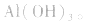 盐水解生成不挥发性酸时,蒸干后一般仍为原物质,如蒸干
盐水解生成不挥发性酸时,蒸干后一般仍为原物质,如蒸干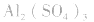 溶液,得
溶液,得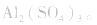
4.盐水解生成强碱时,蒸干后一般得到原物质,如蒸干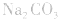 溶液,得到
溶液,得到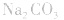 等。
等。
5.有时要多方面考虑,如加热蒸干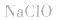 溶液时,既要考虑水解,又要考虑
溶液时,既要考虑水解,又要考虑 的分解,所得固体为
的分解,所得固体为
金属的腐蚀:
1.金属腐蚀的概念金属与周围的气体或液体物质发生氧化还原反应而引起损耗的现象。
2.金属腐蚀的实质金属原子(M)失去电子而被氧化的过程。
M-ne-==M n+
金属的电化学腐蚀:
不纯的金属或合金因发生原电池反应而造成的腐蚀。最普遍的钢铁腐蚀是:
负极:2Fe-4e-=2Fe2+
正极:O2+2H2O+4e-=4OH- (注:在少数情况下,若周围介质的酸性较强,正极的反应是:2H++2e-=H2↑)
金属的腐蚀以电化腐蚀为主.例如,钢铁生锈的主要过程为
(1)吸氧腐蚀:金属在酸性很弱或中性溶液里,空气里的氧气溶解于金属表面水膜中而发生的电化腐蚀。
①发生条件:水膜的酸性很弱或呈中性
②反应本质:形成原电池
③铁为负极,(氧化反应);正极反应:(还原反应)
(2)析氢腐蚀:在酸性较强的溶液中发生电化腐蚀时放出氢气,这种腐蚀叫做析氢腐蚀。
①发生条件:水膜的酸性较强
②反应本质:形成原电池
③铁为负极,(氧化反应);正极反应:(还原反应)
钢铁的电化学腐蚀的两种类型:


金属腐蚀快慢的判断:
金属腐蚀的快慢与下列两个因素有关:
(1)与构成原电池的材料有关,两极材料的活泼性差别越大,电动势越大,氧化还原反应的速率越快,活泼金属被腐蚀的速率就越快。
(2)与金属所接触的电解质溶液的性质有关,活泼金属在电解质溶液中的腐蚀快于在非电解质溶液中的腐蚀,在强电解质溶液中的腐蚀快于在弱电解质溶液中的腐蚀。一般来说,可用下列原则判断:电解原理引起的腐蚀>原电池原理引起的腐蚀> 化学腐蚀>有防护措施的腐蚀
金属的化学腐蚀:
1、定义:金属跟接触到的干燥气体(如O2、Cl2、SO2 等)或非电解质液体 (如石油)等直接发生化学反应而引起的腐蚀
2、条件:金属跟氧化剂直接接触
3、现象:无电流产生
4、本质:金属被氧化而腐蚀
5、反应速率:v(电化学腐蚀)>v(化学腐蚀)
(1)外加电流的阴极保护法。如把金属连接在电源的负极上,这样就能消除引起金属腐蚀的原电池反应。
(2)牺牲阳极的阴极保护法。如在金属上铆接比它更活泼的另一种金属,发生金属腐蚀时是较活泼的金属被腐蚀而金属本身受到保护。
金属的表面防护:
(1)改变金属的组成或结构。如在铁中加入一定比例的铬炼制的铬钢,具有很强的耐腐蚀性。既含铬又含镍的铬镍不锈钢,其耐腐蚀性更好。
(2)在金属表面覆盖一层保护膜,使金属与周围具有腐蚀性的气体或电解质溶液隔离,便可保护金属,防止金属腐蚀。如在金属表面喷漆、电镀或表面钝化等。
基本仪器的使用:
1、可加热的仪器:
| 名称和图片 | 主要用途 | 使用注意事项 |
 |
常用作少量试剂的溶解或反应的容器,也可用于收集少量气体、装配小型气体发生器 | 可直接加热。硬质试管能耐约700℃的高温,普通试管不耐高温。加热前试管外壁要擦干,加热时必须用试管夹夹持或用铁夹固定在铁架台上,切不可拿在手中,加热时还要先使试管均匀受热,然后重点加热其有药品的部位。加热固体时,要使管口略向下倾斜,固体要平铺于试管底部;加热液体时,要使管口向上,使试管与桌面成 45。角,且液体量不超过试管容积的1/3,管口切忌向着有人的方向。热的试管不要骤冷,以防炸裂。在常温下的物质溶解或发生化学反应,试管内液体体积不要超过试管容积的1/2。拿取试管时,用中指、食指、拇指拿住距试管口1/3处 |
 |
常用来配制、浓缩溶液,用作试剂用量较多的加热或不加热反应的容器,向其他容器中转移液体的容器,代作水浴锅 | 加热时要垫石棉网且外壁干燥,或用水浴加热。加热时液体量不要超过容积的2/3,也不可把液体蒸干。热的烧杯不可骤冷。搅拌时玻璃棒不可触及杯壁和杯底 |
 |
常用作在加热或不加热条件下有液体试剂参加的化学反应的容器 | 平底烧瓶一般不用作加热反应容器。圆底烧瓶在加热时要垫石棉网且外壁要干燥,或用水浴加热,加热时液体量不要超过容积的1/2,也不要把液体蒸干。热的烧瓶不可骤冷 |
 |
常用作液态混合物的蒸馏或分馏容器,也可用作气体发生器 | 同圆底烧瓶,但要加碎瓷片防暴沸。蒸馏(分馏)时温度计水银球要在支管口处 |
 |
主要用作滴定实验的反应器,也可用作其他化学反应、液体收集的容器,还可用于组装洗气瓶 | 同圆底烧瓶 |
| 名称和图形 | 主要用途 | 使用注意事项 |
 |
用来量取要求不太严格的液体体积,是一种粗略的液体体积计量仪器 | 使用前要洗净,使用时要在桌面上放平稳,读数时,视线要与液体凹液面的最低点相平。不可用作反应器,不可加热,也不能用来配制溶液 |
 |
常用于配制一定体积、浓度准确的溶液,如配制一定体积、一定物质的量浓度的溶液 | 不能用作反应容器,不可加热,瓶和瓶塞是一一对应的,瓶塞不能互换,瓶塞要用结实的细绳系在瓶颈上,以防损坏或丢失。使用前要检查是否完好、瓶口处是否漏水,不漏水的容量瓶才能使用。配制溶液用的溶质,要先在烧杯里用适量的蒸馏水溶解,并使溶液恢复到室温后才能转入容量瓶中,不可直接在容量瓶中溶解溶质。向容量瓶里加入溶液或蒸馏水时,要用玻璃棒引流,至距刻度线23cm时,改用胶头滴管滴加蒸馏水,不能让液体流经刻度线以上的内壁。定容时,要使液体凹液面与瓶颈部的刻度线相切,并平视观察。手持容量瓶时,不能用手掌握瓶颈和瓶体,要用手指肚触瓶的方式持瓶。容量瓶内不能长期储存溶液。容量瓶使用完毕,应冼净、晾干,玻璃磨砂瓶塞与瓶口处垫张纸条,以免瓶口与瓶塞粘连 |
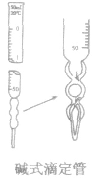  |
主要用于精确地放出一定体积的溶液,如酸碱中和滴定、配制一定物质的量浓度的硫酸溶液,都要用到滴定管。酸式滴定管用来盛装酸性溶液,碱式滴定管用来盛装碱性溶液,棕色滴定管用来盛装见光易分解的溶液 | 酸式滴定管与碱式滴定管不能互换使用。滴定管在使用前要先检查是否漏液。对酸式滴定管还要检查玻璃活塞是否转动灵活,对碱式滴定管还要检查橡胶管是否老化失去弹性。只有检查合格的滴定管才能使用。向滴定管内装入实验所用的溶液前,要用该溶液润洗滴定管23次,装入溶液后要赶走滴定管尖嘴内的气泡,然后将液面调在“0”刻度或“0”刻度以下。从滴定管里放出液体时,要将滴定管垂直固定在滴定管夹上,用左手操作滴定管。读数时,要在停止放出液体后1~2min后进行,要使视线与凹液面保持水平,读取与液体凹液面相切处的刻度值。滴定管用毕要立即洗净,长期不用时要在活塞处垫上小纸条,防止活塞粘连 |
 |
常用于精确度不高的物质质量的称量 | 使用时要放平稳。称量前要先调零。称量一般的药品时,要先在两盘上各放一张大小相同的纸片后再加砝码和药品;易潮解、强腐蚀性的药品,要盛在烧杯或表面皿中称量;热的物质要待冷却至室温后再称量。称量时,左盘放称量物,右盘放砝码。砝码要用镊子由大到小夹取,最后移动游码(用镊子)。称量完毕,要把砝码收回砝码盒内,游码拨回到标尺的零处 |
 |
用于测量物体的温度 | 测量物体某一部位的温度,温度计的感温泡就要放在这一部位。选用温度计时,要使温度计的最大显示温度高于被测物体温度。处在高温下的温度计不可骤冷。切忌以温度计代替玻璃棒去搅拌液体或固体 |
| 名称和图形 | 主要用途 | 使用注意事项 |
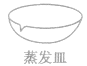 |
蒸发液体、浓缩溶液或干燥固体 | 能耐高温,可在火焰上直接加热,但不能骤冷。在加热蒸发液体时,液体体积一般不超过蒸发皿容积的2/3,要用玻璃棒不断搅拌液体,以免液体飞溅。热的蒸发皿不能直接放在实验桌上。取用蒸发皿要用坩埚钳 |
 |
在化学实验中常用来高温灼烧固体 | 能耐商温,可在火焰上直接加热,但不能骤冷。定量实验的冷却应在干燥器中。熔融NaOH等强碱时要在铁坩埚中进行。夹持坩埚和坩埚盖时都要用坩埚钳 |
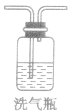 |
让不纯的气体通过装入的有关液体,除去杂质 | 装入洗液的量勿超过容积的2/3。使用之前要检验气密性,不漏气者才可使用。进气口和出气口不要接错。气体进入的速率不能太快,以便有效吸收杂质。改作量气装置时,液体要加满,且短进长出 |
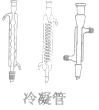 |
使热的蒸气冷却凝结为液体 | 要使冷却水的进口在组装仪器的低处,出水口在组装仪器的高处,以保证隔套内充满冷却水,提高冷却效率 |
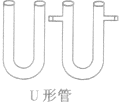 |
内装固体干燥剂或吸收剂时,用于干燥或吸收气体;也可作电解、电泳等实验的容器;还可用于装配简易启普发生器 | 两管之间不能用力挤压或拉扯,以防在弯管处断裂 |
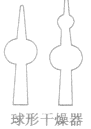 |
用于内装固体干燥剂吸收某些气体,也可用于组装简易启普发生器 | 气体要从大口进,小口出。球体和细管的连接处一般要塞一个小棉花球或玻璃丝球,防止干燥剂颗粒进入细管内 |
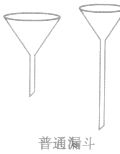 |
用于过滤操作和向小口容器里倾注液体。还用作装配易溶于水的气体的吸收装置(防倒吸) | 过滤时应“一贴、二低、三靠”,即滤纸紧贴漏斗内壁,无缝隙,无气泡;滤纸低于漏斗口上沿0.5cm,滤液液面低于滤纸的边缘;漏斗下端管口紧靠烧杯内壁,玻璃棒末端轻轻地斜靠在三层滤纸处,烧杯引水口紧靠在玻璃棒上 |
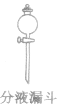 |
用于两种互不相溶的液体的分离,也用于装配制备物质的反应器,用它向容器里加入液体反应物 | 使用前要检查活塞处和上口处是否漏水。分液时,上层液体从上口倒出,下层液体由下口放出。从下口放出液体时,要将上端玻璃塞的小孔或凹槽对准颈部的小孔使漏斗内外相通,及时关闭活塞,防止上层液体流出 |
4、其他常用仪器
| 名称和图形 | 主要用途 | 使用注意事项 |
 |
用于中、低温度的加热。进行焰色反应 | 点燃酒精灯时,要把灯放正,用火柴点燃,严禁以灯点灯、向灯体内加酒精时,要先熄灭酒精灯,再通过漏斗加入酒精,严禁向燃着的酒精灯内添加酒精。熄灭酒精灯时,要用灯帽盖灭,不可吹灭。灯体内酒精的量要在灯体容积的 之间 之间 |
 |
用来粉碎硬度不太大的固态物质,也可用来拌匀粉末状固态反应物 | 不能用火加热。研磨时必须稍加压力,使研杵在研钵里缓慢地转动并加以挤压,使固体粉碎,切不可用研杵敲击 |
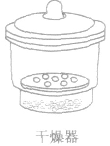 |
用于保存干燥的物质或者使热的物质在干燥的环境下冷却 | 干燥剂放在瓷板的下面,不能使用液体干燥剂(如浓H2SO4),固态干燥剂一般为无水CaCl2或硅胶,被干燥的物质放在瓷板上.太热的物质要待稍冷却后再放入。打开干燥器时,要一只手握住盖上的圆球,另一只手揽住容器,沿水平方向推移盖子。搬动干燥器时,要用拇指压住盖子,防止盖子滑落摔碎 |
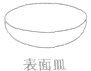 |
用作烧杯盖,或微量物质反应的容器 | 不能用火加热 |
 |
分装多种化学试剂。广口瓶也可用于装配洗气瓶、在常温下进行的化学反应的容器 | 不能加热。塞子、盖子不可乱换,取下的塞子、盖子要倒放在桌面上,倾倒液体时要使标签向着手心。盛固体试剂用广口瓶,盛液体试剂用细口瓶;盛见光易分解的试剂用棕色瓶,盛见光不分解的试剂既可用无色瓶也可用棕色瓶;盛碱性试剂要用配塑料塞的试剂瓶,盛强氧化性试剂、有机溶剂要用配玻璃塞的试剂瓶 |
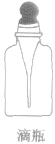 |
盛装少量液体试剂,用滴管吸取液体滴加到其他的容器中或试纸上。普通胶头滴管的用途与该滴管相同 | 滴管不能调换。滴瓶不能盛强碱性溶液及强挥发腐蚀橡胶的试剂 (如浓溴水、浓硝酸等)。取液时,要先提起滴管,捏紧胶头排出空气和液体后,再插入瓶中吸取液体,吸有液体的滴管不能平放和倒放。滴试剂时,滴管下端切勿接触接收器的器壁。不能用一支滴管吸取多种液体。滴液完毕要立即把滴管插入原滴瓶中。普通胶头滴管的使用方法及注意事项,与滴瓶上的滴管相同 |
 |
主要用于收集气体,也可用作洗气瓶、气体跟气体反应的容器、固体在气体中燃烧反应的容器 | 一般不能加热。当用作固体在气体中燃烧反应的容器时,一般要在瓶底留有少量水或铺一层细沙。盛不同密度的气体放置时瓶口方向不同 |
pH的测定:
1.酸碱指示剂法:只能粗略测定溶液的pH范围
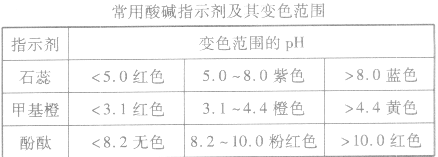
2.pH试纸法:用洁净的玻璃棒蘸取待测溶液点在一小片pH试纸(干燥的)的中部,变色后与标准比色卡对照,读出溶液的pH(粗略的整数值)。
3.pH计法(酸度计):能精确测定溶液的pH(精确到小数点后两位)。
与“下列有关实验的说法正确的是( )A.用pH试纸蘸取NaOH溶液,...”考查相似的试题有:
- 已知0.1molL-1的二元酸H2A溶液的pH=4.0则下列说法中正确的是A.在Na2A、NaHA两溶液中,离子种类不相同B.在溶质物质的量相等...
- 下列过程或现象与盐类水解无关的是A.草木灰不能与铵混合使用态氮肥B.铁在潮湿的环境下生锈C.加热氯化铁溶液颜色变深D.浓...
- A、B、C、D、E、F六种短周期元素的原子序数依次增大。A、D同族,B、C同周期;B原子最外层电子数是次外层的两倍;在周期表中A...
- 下列叙述正确的是( )①硫酸钡难溶于水和酸,可做X光透视肠胃的药剂②蛋白质遇酒精会变性,医疗中用75%的乙醇溶液进行消毒③棉...
- 用“>”“
- 下列水解反应的离子方程式正确的是( )A.NH4++H2ONH3·H2O+H+B.CO32-+2H2OH2CO3+2OH-C.CH3COOH+H2OCH3COO-+H3O...
- 下图装置(Ⅰ)是一种可充电电池,装置(Ⅱ)为电解池。装置(Ⅰ)的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为2Na...
- 下列说法正确的是( )A.埋在潮湿地下的铁管道比地上的铁管道更耐腐蚀B.在钢铁表面涂上一层油漆,不能达到防止钢铁锈蚀的目...
- 下列几种铁板,在镀层被破坏后,最耐腐蚀的是( )A.镀锌铁板B.镀铜铁板C.镀铅铁板D.镀锡铁板
- 下列现象与电化学腐蚀无关的是( )A.黄铜(铜锌合金)制作的铜锣不易产生铜绿B.生铁比软铁心(几乎是纯铁)容易生锈C.铁...