本试题 “常温下,两种溶液①0.1mol/L NH3•H2O ②0.1mol/L NH4Cl中:(1)溶液①的pH______ 7(填“>”、“<”或“=”),其原因是______(用离子方程式表示).(2)溶液②呈_...” 主要考查您对弱电解质的电离
盐水解的影响因素
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 弱电解质的电离
- 盐水解的影响因素
定义:
在一定温度、浓度的条件下,弱电解质在溶液中电离成离子的速率与离子结合成分子的速率相等时,电离过程就到了电离平衡状态,叫弱电解质的电离平衡。

电离平衡的特征:
(1)等:
(2)动: 的动态平衡
的动态平衡
(3)定:条件一定,分子与离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。
在一定温度、浓度的条件下,弱电解质在溶液中电离成离子的速率与离子结合成分子的速率相等时,电离过程就到了电离平衡状态,叫弱电解质的电离平衡。

电离平衡的特征:
(1)等:

(2)动:
 的动态平衡
的动态平衡(3)定:条件一定,分子与离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。
影响盐类水解平衡的因素:
主要因素是盐本身的性质,组成的盐的酸根对应的酸越弱(或阳离子对应的碱越弱),水解程度就越大,另外还受温度、浓度及外加酸碱等因素的影响。
(1)温度:盐的水解是吸热反应,因此升高温度水解程度增大;
(2)浓度:盐的浓度越小,水解程度越大,但溶液的酸碱性一般越弱;
(3)外加酸碱:外加酸碱能促进或抑制盐的水解,使盐的水解程度降低,但由于酸(或碱)的加入,使溶液的酸(碱性)增强。
例如: 外界条件对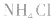 水解平衡
水解平衡
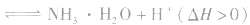 的影响
的影响
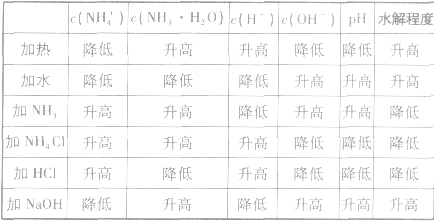
(4)能水解的阳离子与能水解的阴离子混合,会相互促进水解。常见的含下列离子的两种盐混合时,会发生较彻底的双水解反应:阳离子:Fe3+、Al3+;阴离子:CO32-、HCO3-、S2-、HS-、AlO2-、SO32-、HSO3-等。
(5)Fe3+与S2-、HS-、SO32-、HSO3-等还原性离子发生氧化还原反应,而不是发生双水解反应。
(6)HCO3-与AlO2-在溶液中也不能共存,可发生反应产生白色沉淀,但不是由于双水解反应,而是:
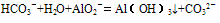
主要因素是盐本身的性质,组成的盐的酸根对应的酸越弱(或阳离子对应的碱越弱),水解程度就越大,另外还受温度、浓度及外加酸碱等因素的影响。
(1)温度:盐的水解是吸热反应,因此升高温度水解程度增大;
(2)浓度:盐的浓度越小,水解程度越大,但溶液的酸碱性一般越弱;
(3)外加酸碱:外加酸碱能促进或抑制盐的水解,使盐的水解程度降低,但由于酸(或碱)的加入,使溶液的酸(碱性)增强。
例如: 外界条件对
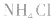 水解平衡
水解平衡
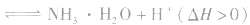 的影响
的影响
(4)能水解的阳离子与能水解的阴离子混合,会相互促进水解。常见的含下列离子的两种盐混合时,会发生较彻底的双水解反应:阳离子:Fe3+、Al3+;阴离子:CO32-、HCO3-、S2-、HS-、AlO2-、SO32-、HSO3-等。
(5)Fe3+与S2-、HS-、SO32-、HSO3-等还原性离子发生氧化还原反应,而不是发生双水解反应。
(6)HCO3-与AlO2-在溶液中也不能共存,可发生反应产生白色沉淀,但不是由于双水解反应,而是:
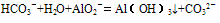
盐类水解程度大小比较规律:
1.盐水解生成的弱酸(或弱碱)越弱,水解程度越大。常据此判断弱酸(或弱碱)的相对强弱:如等浓度的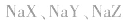 三种盐溶液,pH依次增大,则弱酸根离子
三种盐溶液,pH依次增大,则弱酸根离子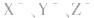 的水解程度依次增大,所以酸性HX>HY>HZ。
的水解程度依次增大,所以酸性HX>HY>HZ。
2.相同条件下:正盐>相应酸式盐。如水解程度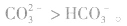
3.相互促进水解的盐>单水解的盐>相互抑制水解的盐。如水解程度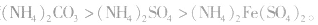
发现相似题
与“常温下,两种溶液①0.1mol/L NH3•H2O ②0.1mol/L NH4Cl中:(1...”考查相似的试题有:
- 常温下,pH=3的醋酸溶液和pH=11的NaOH溶液混合,下列有关说法中一定正确的是[ ]A.水电离出的氢离子浓度:NaOH溶液>醋酸溶液B...
- 已知25℃时有关弱酸的电离平衡常数:弱酸CH3COOHHCNH2CO3电离平衡常数1.8×l0-54.9×l0-10K1=4.3×l0-7 K2=5.6×l0-11 25℃下,下列...
- 下列说法正确的是A.向AgCl悬浊液中加入少量NaCl固体后振荡,c(Cl-)增大,KsP(AgCl)增大B.某溶液中由水电离出的时,则该溶...
- 下列各物质溶解于水时,电离出的阴离子能使水的电离平衡向右移动的是( )A.CH3COOHB.Na2SO4C.NH4ClD.HF
- 下列过程或现象与盐类水解无关的是A.纯碱溶液去油污B.稀醋酸溶液加热时其pH 减小C.小苏打溶液与AlCl3溶液混合产生气体和沉...
- 等体积的下列溶液,阴离子的总物质的量浓度最大的是()A.0.2mol·L-1K2CO3B.0.1mol·L-1Ba(OH)2C.0.2mol·L-1NaClD.0.2mol·...
- 对滴有酚酞试液的下列溶液,操作后红色变深的是( )A.AlCl3溶液中在融入AlCl3B.CH3COONa溶液加热C.氨水中假如少量NH4Cl固...
- 下列物质的水溶液因发生水解而显酸性的是A.NH4ClB.KHSO4C.NaHCO3D.H2SO4
- 如图表示某物质发生的是( )
- 下列液体均处于25℃,有关叙述正确的是A.某物质的溶液pH < 7,则该物质一定是酸或强酸弱碱盐B.pH=4的NH4Cl溶液,溶液中c(H+...