本试题 “下列说法正确的是[ ]A.所有的非金属氧化物都是酸性氧化物B.BaSO4难溶于水,是弱电解质C.福尔马林、盐酸、明矾、纯碱都是混合物D.某温度下,NaCl的溶解度...” 主要考查您对溶液的质量分数
物质的简单分类
强电解质、弱电解质
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶液的质量分数
- 物质的简单分类
- 强电解质、弱电解质
溶液质量分数= ×100%
×100%
用溶解度表示:
有关溶液的计算:

物质的量浓度与质量分数(质量百分比浓度)的比较:
| 物质的量的浓度 | 溶质的质量分数 | |
| 常用溶质的量的单位 | mol | g |
| 常用溶液的量的单位 | L | g |
| 表达式 | c(B)=n(B)/V | 溶质的质量分数= |
| 特点 | 体积相同,物质的量浓度也相同的任何溶液中,所含溶质的物质的量相同,但溶质的质量不一定相同 | 质量相同,溶质的质量分数相同的任何溶液中,所含溶质的质量相同,但溶质的物质的量不一定相同 |
物质的量浓度与质量分数之间的转化关系:
(1)基本公式: ,c为溶质的物质的量的浓度,单位mol·L-1,ρ为溶液密度,单位为g·cm-3,ω为溶质的质量分数,M为溶质的摩尔质量,单位g·mol-1。
,c为溶质的物质的量的浓度,单位mol·L-1,ρ为溶液密度,单位为g·cm-3,ω为溶质的质量分数,M为溶质的摩尔质量,单位g·mol-1。
(2)公式的推导(按溶液体积为V升推导)
 或
或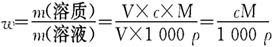
溶质的质量分数:
溶质的质量分数又叫溶液的质量百分比浓度。一般来说,(对大多数溶液)物质的量浓度越大,溶液的密度越大,质量百分比浓度也越大。但是,对于氨水、酒精溶液,物质的量浓度越大,密度越小。
溶液的混合定律:
溶质相同、质量分数分别为a%、b%的两溶液混合:
⑴等体积混合
- 当溶液的密度大于1mol/mL时,必然是溶液浓度越大,密度越大,(如硫酸、硝酸、盐酸、氢氧化钠等多数溶液)等体积混合后,质量分数
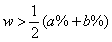 ;
; - 当溶液的密度小于1mol/mL时,必然是溶液浓度越大,密度越小,(如酒精、氨水溶液)等体积混合后,质量分数
 。
。
⑵等质量混合
两溶液等质量混合时,(无论ρ>1g/mL还是ρ<1g/mL),则混合后溶液中溶质的质量分数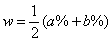
混合物、纯净物、单质、化合物的概念:
(1)混合物:由两种或多种物质混合而成的物质。
(2)纯净物:由单一物质组成的物质 注:由同位素原子组成的物质是纯净物,如H2O和D2O混合后仍为纯净物。
(3)单质:由同种元素组成的纯净物,可分为金属单质和非金属单质。
(4)化合物:由不同种元素组成的纯净物。从不同角度可见化合物分为离子化合物,共价化合物,电解质和非电解质,有机化合物和物质化合物,酸碱盐和氧化物等。
混合物、纯净物、单质、化合物的概念:
(1)混合物:由两种或多种物质混合而成的物质
混合物没有固定的组成,一般没有固定的熔沸点
常见特殊名称的混合物:氨水、氯水、王水、天然水、硬水、软水、盐酸、浓硫酸、福尔马林、水玻璃、爆鸣气、水煤气、天然气、焦炉气、高炉煤气、石油气、裂解气、空气、合金、过磷酸钙、漂白粉、黑火药、铝热剂、水泥、铁触媒、玻璃、煤、石油、石油的各种馏分
注:由同素异形体组成的物质为混合物,如红磷和白磷。
(2)纯净物:由单一物质组成的物质
注:由同位素原子组成的物质是纯净物,如H2O和D2O混合后仍未纯净物。
(3)单质:由同种元素组成的纯净物,可分为金属单质和非金属单质
(1)金属单质:如Fe、Al、Cu等
(2)非金属单质:如Cl2、O2、S等
(4)化合物:由不同种元素组成的纯净物。从不同角度可见化合物分为离子化合物,共价化合物,电解质和非电解质,有机化合物和物质化合物,酸碱盐和氧化物等。
(5)酸、碱、盐、氧化物
①酸:电离理论认为电解质电离出阳离子全部是H+的化合物
常见的强酸:HClO4 H2SO4 HCl HNO3等
常见的弱酸:H2SO3 H3PO4 HF H2CO3 CH3COOH等
②碱:电离理论认为电解质电离出阴离子全部是OH-的化合物
常见强碱:NaOH KOH Ba(OH)2 Ca(OH)2等
常见弱碱:NH3·H2O Al(OH)3 Fe(OH)3等
③盐:电离时生成金属阳离子(NH4+)和酸根离子的化合物,可分为:正盐、酸式盐、碱式盐、复盐
a正盐:Na2SO4 Na2CO3 (NH4)2SO4 等
b酸式盐:NaHCO3 NaHSO4 NaH2PO4 Na2HPO4等
c碱式盐:Cu(OH)2CO3 Mg(OH)2CO3等
d复盐:KAl(SO4)2·H2O (NH4)2Fe(SO4)2·6H2O等
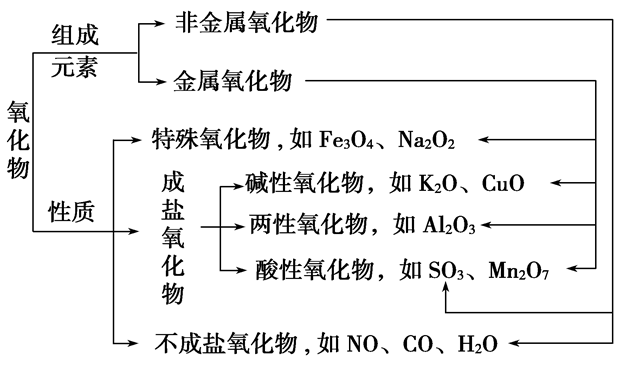
(6)氧化物:由两种元素组成,其中一种元素是氧的化合物
①按组成分:
金属氧化物:Na2O Al2O3 Fe3O4等
非金属氧化物:NO2 SO2 CO2等
②按性质分:
不成盐氧化物:CO NO等
酸性氧化物:CO2 SO2等
碱性氧化物:Na2O CuO等
两性氧化物:Al2O3 ZnO等
过氧化物:Na2O2 H2O2等
超氧化物:KO2等
特殊例子提醒:
(1)胆矾、明矾等结晶水合物是纯净物,不是物质和水的混合物。
(2)碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物(如Mn2O7为酸性氧化物、Al2O3为两性氧化物、Na2O2为过氧化物)。
(3)酸性氧化物不一定是非金属氧化物(如Mn2O7);非金属氧化物也不一定是酸性氧化物(如CO、NO)。
(4)酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱(如SiO2、CuO)。
(5)与水反应生成酸的氧化物不一定是酸性氧化物(如NO2);与水反应生成碱的氧化物不一定是碱性氧化物(如Na2O2)。
无机物分类:

氧化物的分类:
在水溶液里或熔融状态下,能全部电离的化合物。包括:强酸、强碱、大多数盐、活泼金属氧化物等;完全电离、不可逆、不存在电离平衡;电离方程式用“=”表示。
弱电解质:
在水溶液里或熔融状态下,不能全部电离的化合物。包括:弱酸、弱碱、少数盐等;部分电离、可逆、存在电离平衡,电离方程式用“
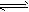 ”表示。
”表示。 强电解质和弱电解质的比较:
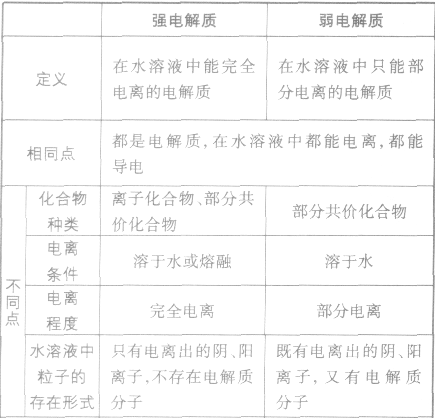
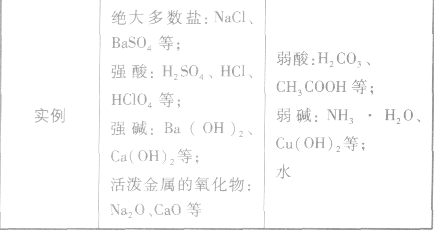
强弱电解质的判断依据:
1.在相同浓度、相同温度下,与强电解质做导电性对比实验.
2.浓度与pH的关系。如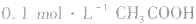 溶液的pH>1,则证明
溶液的pH>1,则证明 是弱电解质。
是弱电解质。
3.测定对应盐溶液的酸碱性。如 溶液呈碱性,则证明醋酸是弱电解质。
溶液呈碱性,则证明醋酸是弱电解质。
4.稀释前后的pH变化与稀释倍数的关系。例如,将pH=2的酸溶液稀释1000倍,若pH<5,则证明该酸为弱电解质;若pH=5,则证明该酸为强电解质。
5.采用实验证明电离平衡。如向醋酸溶液中滴人石蕊试液,溶液变红,再加入醋酸钠晶体,颜色变浅。
与“下列说法正确的是[ ]A.所有的非金属氧化物都是酸性氧化物B....”考查相似的试题有:
- 下列四个图象分别代表对应的四种过程,其中正确的是[ ]A.分别加热等质量的氯酸钾与高锰酸钾,反应过程中生成氧气的质量变化B...
- 分类是化学学习和研究的常用手段。下列分类依据和结论都正确的是[ ]A.H2O、HCOOH、(NH3)2Fe(SO4)2均含有氧,都是氧化物B.HC...
- 下列叙述正确的是[ ]A.碱性氧化物都能与强酸反应B.酸性氧化物都能与水反应C.酸性氧化物均不与酸反应D.两种酸混合后溶液一...
- (4分)下列几组物质:A.金属石和石墨B.C2H6和C5H12C.C2H4和C2H6D.CH3CH2CH2CH3E.35Cl和37Cl(1)属于同分异构体的是___...
- 下列说法中错误的是A.磺化、硝化、风化、钝化都是化学变化B.蒸馏、干馏、常压分馏、减压分馏、都是物理变化C.甘油不是油,...
- 分类是学习和研究化学的一种重要方法,下列分类合理的是( )A.烧碱和纯碱都属于碱B.硫酸和盐酸都属于含氧酸C.Na2SiO3和Na...
- (8分)有以下物质 ①Fe、 ②AgCl固体、 ③ 熔融Ba(OH)2、 ④Al2(SO4)3溶液、 ⑤SO2、⑥蔗糖溶液、 ⑦食盐水、 ⑧ H2CO3、 ⑨无水乙醇(...
- 下列属于非电解质的是A.铜丝B.氢氧化钠C.蔗糖D.食盐水
- 2010年10月,海南省大部分地区遭暴雨洪涝灾害,食盐、蔗糖、醋酸、纯碱、“84”消毒液等是灾后居民日常生活中经常使用的物质,...
- 下列物质中属于非电解质的是( )。A.NaOHB.O2C.Na2CO3D.乙醇