本试题 “用下列实验装置完成对应的实验,能达到实验目的是( )A.制取并收集乙炔B.比较NaHCO3、Na2CO3对热稳定性C.吸收多余的NH3D.实验室中制取少量乙酸乙酯” 主要考查您对气体的收集、净化、干燥
乙酸乙酯的制备
通过实验装置图判断实验的可行性
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 气体的收集、净化、干燥
- 乙酸乙酯的制备
- 通过实验装置图判断实验的可行性
收集方法及装置:
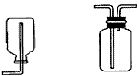
a.排水集气法:适用于收集不溶于水,不与水反应的气体。装置如下:如采用第二个装置,气体应短进长出。

b.向上排空气法:适用于收集密度比空气大不与空气反应的气体,装置如下:如采用第二个装置,气体应长进短出。

c.向下排空气法:适用于收集密度比空气小不与空气反应的气体。装置如下:如采用第二个装置,气体应短进长出。
气体净化:
装置: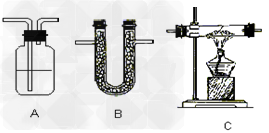

气体干燥:
(1)干燥原则:
干燥剂只能吸收气体中含有的水分而不能与气体发生反应。
①酸性干燥剂不能干燥碱性气体。
②碱性干燥剂不能干燥酸性气体。
③具有强氧化性的干燥剂不能干燥具有强还原性的气体。注意H2、CO、SO2虽具有还原性,但可用浓H2SO4干燥。
(2)常见物质干燥
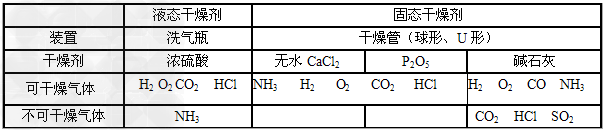
a.排水集气法:适用于收集不溶于水,不与水反应的气体。装置如下:如采用第二个装置,气体应短进长出。

b.向上排空气法:适用于收集密度比空气大不与空气反应的气体,装置如下:如采用第二个装置,气体应长进短出。

c.向下排空气法:适用于收集密度比空气小不与空气反应的气体。装置如下:如采用第二个装置,气体应短进长出。

气体净化:
装置:


气体干燥:
(1)干燥原则:
干燥剂只能吸收气体中含有的水分而不能与气体发生反应。
①酸性干燥剂不能干燥碱性气体。
②碱性干燥剂不能干燥酸性气体。
③具有强氧化性的干燥剂不能干燥具有强还原性的气体。注意H2、CO、SO2虽具有还原性,但可用浓H2SO4干燥。
(2)常见物质干燥

乙酸乙酯的制备:
(1)实验目的:
掌握用醇和羧酸制备酯的方法。
(2)试剂:
乙醇、冰醋酸、浓硫酸、饱和碳酸钠水溶液、饱和食盐水、饱和氯化钙、无水硫酸镁(或无水硫酸钠) 2~3g (用于干燥乙酸乙酯)
(3)反应原理:
主反应: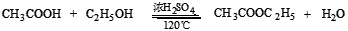
副反应: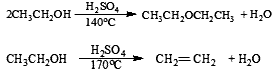
(4)反应装置图:
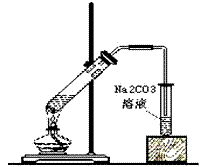
(5)操作步骤
①在一个大试管里注入乙醇2mL,再慢慢加入0.5mL浓硫酸、2mL乙酸,连接好制备乙酸乙酯的装置。
②用小火加热试管里的混合物。把产生的蒸气经导管通到3mL饱和碳酸钠溶液的上方约2mm~3mm处,注意观察盛碳酸钠溶液的试管的变化,待有透明的油状液体浮在液面上,取下盛有碳酸钠溶液的试管,并停止加热。振荡盛有碳酸钠溶液的试管,静置,待溶液分层后,观察上层液体,并闻它的气味。
③加热混合物一段时间后,可看到有气体放出,在盛碳酸钠溶液的试管里有油状物。
(6)注意事项:
1、酯化反应所用仪器必须无水,包括量取乙醇和冰醋酸的量筒也要干燥。
2、加热之前一定将反应混合物混合均匀,否则容易炭化。
3、分液漏斗的正确使用和维护。。
4、用10%碳酸钠水溶液洗涤有机相时有二氧化碳产生,注意及时给分液漏斗放气,以免气体冲开分液漏斗的塞子而损失产品。
5、正确进行蒸馏操作,温度计的位置影响流出温度,温度计水银球的上沿与蒸馏头下沿一平。
6、有机相干燥要彻底,不要把干燥剂转移到蒸馏烧瓶中。
7、反应和蒸馏时不要忘记加沸石。
8、用CaCl2溶液洗之前,一定要先用饱和NaCl溶液洗,否则会产生沉淀,给分液带来困难。
(1)实验目的:
掌握用醇和羧酸制备酯的方法。
(2)试剂:
乙醇、冰醋酸、浓硫酸、饱和碳酸钠水溶液、饱和食盐水、饱和氯化钙、无水硫酸镁(或无水硫酸钠) 2~3g (用于干燥乙酸乙酯)
(3)反应原理:
主反应:
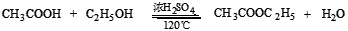
副反应:
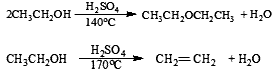
(4)反应装置图:

(5)操作步骤
①在一个大试管里注入乙醇2mL,再慢慢加入0.5mL浓硫酸、2mL乙酸,连接好制备乙酸乙酯的装置。
②用小火加热试管里的混合物。把产生的蒸气经导管通到3mL饱和碳酸钠溶液的上方约2mm~3mm处,注意观察盛碳酸钠溶液的试管的变化,待有透明的油状液体浮在液面上,取下盛有碳酸钠溶液的试管,并停止加热。振荡盛有碳酸钠溶液的试管,静置,待溶液分层后,观察上层液体,并闻它的气味。
③加热混合物一段时间后,可看到有气体放出,在盛碳酸钠溶液的试管里有油状物。
(6)注意事项:
1、酯化反应所用仪器必须无水,包括量取乙醇和冰醋酸的量筒也要干燥。
2、加热之前一定将反应混合物混合均匀,否则容易炭化。
3、分液漏斗的正确使用和维护。。
4、用10%碳酸钠水溶液洗涤有机相时有二氧化碳产生,注意及时给分液漏斗放气,以免气体冲开分液漏斗的塞子而损失产品。
5、正确进行蒸馏操作,温度计的位置影响流出温度,温度计水银球的上沿与蒸馏头下沿一平。
6、有机相干燥要彻底,不要把干燥剂转移到蒸馏烧瓶中。
7、反应和蒸馏时不要忘记加沸石。
8、用CaCl2溶液洗之前,一定要先用饱和NaCl溶液洗,否则会产生沉淀,给分液带来困难。
通过实验装置图判断实验的可行性:
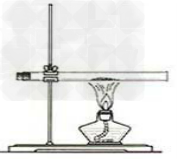
1.红磷转换成白磷装置图
2.氨气易溶于水(喷泉实验)

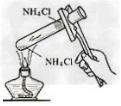
3.氯化铵受热分解
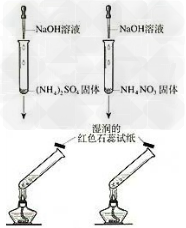
4.铵盐与碱反应
5.实验室制取氨气装置图

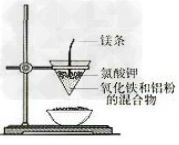
6.铝热反应实验装置
7.铁与水蒸气反应实验装置图

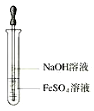
8.氢氧化亚铁的生成
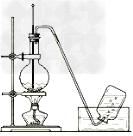
9.实验室制取乙烯的装置图
10.乙烯使高锰酸钾、溴水褪色

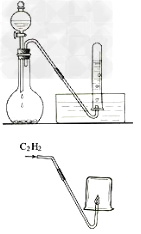
11.乙炔的制取和燃烧
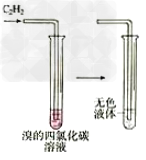
12.乙炔使溴水褪色
13.苯不能使高锰酸钾褪色

14.溴乙烷的水解反应
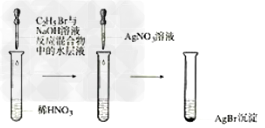
15.苯酚的显色反应
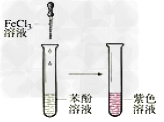
16.乙酸乙酯的制备

17.油脂的水解
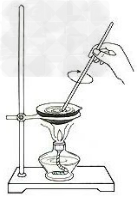
18.中和热的测定
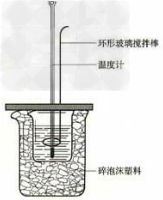
19.电镀铜实验装置
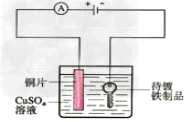
20.点解饱和食盐水
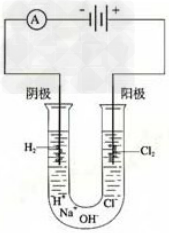
1.红磷转换成白磷装置图

2.氨气易溶于水(喷泉实验)

3.氯化铵受热分解

4.铵盐与碱反应

5.实验室制取氨气装置图

6.铝热反应实验装置

7.铁与水蒸气反应实验装置图

8.氢氧化亚铁的生成

9.实验室制取乙烯的装置图

10.乙烯使高锰酸钾、溴水褪色

11.乙炔的制取和燃烧

12.乙炔使溴水褪色

13.苯不能使高锰酸钾褪色

14.溴乙烷的水解反应

15.苯酚的显色反应

16.乙酸乙酯的制备

17.油脂的水解

18.中和热的测定

19.电镀铜实验装置

20.点解饱和食盐水

发现相似题
与“用下列实验装置完成对应的实验,能达到实验目的是( )A.制...”考查相似的试题有:
- 下图是产生和收集气体的实验装置,该装置适合于A.用H2O2溶液和MnO2反应制取O2B.用浓盐酸和MnO2反应制取C12C.用稀硫酸与石...
- 硫酸铜是一种应用广泛的化工原料,实验室中可通过不同途径制取硫酸铜溶液和胆矾(CuSO4·5H2O),其中一种流程如下:(1)操作I具...
- 用下图实验装置(可添加加热或尾气处理装置)进行以下实验,无法达到目的的是A.实验室制取并收集少量NO2B.实验室制取并收集...
- 制取硝酸铜的以下三种方案的叙述中,不正确的是①2Cu+O22CuO,CuO+2HNO3="=" Cu(NO3)2+ H2O②3Cu+8HNO3(稀)3Cu(NO3)2+2NO↑+4H...
- 某学习小组按右图在实验室制取氨气并探究铜的有关性质(部分夹持仪器未画出)。请回答:(1)制取氨气的化学方程式是 。(2)...
- 化合物KxFe(C2O4)y·3H2O(Fe为+3价)是一种光敏材料,实验室可以用如下的方法来制备这种材料并测定这种材料的组成。Ⅰ.制备K...
- 利用下列装置可以完成的实验组合是 ( ) 选项制气装置洗气瓶中试剂瓶中气体A氯酸钾 MnO2浓硫酸O2B石灰石 稀盐酸NaHCO3溶液CO2C...
- 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。⑴图中的两处明显的错误是____________________________________...
- 实验来源于生活且服务于生活,请回答些列问题:(1)正确的实验操作是实验成功的重要因素,下列实验操作错误的是______(2)...
- 实验室可以通过以下三条途径按不同要求制取氮气:①加热NaNO2(一种致癌物质,有毒)与NH4Cl的混合物浓溶液制取N2;②将空气通...