本试题 “在一节化学实验探究课上,张老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。我们对此气体展开了一系列探究...” 主要考查您对氢气的制取和收集
二氧化碳的制取和收集
氢气的检验和验满
二氧化碳的检验和验满
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氢气的制取和收集
- 二氧化碳的制取和收集
- 氢气的检验和验满
- 二氧化碳的检验和验满
实验室里通常用稀硫酸跟金属锌起反应来制取氢气,也可以用盐酸代替硫酸,用镁或铁代替锌来制取氢气。
氢气的实验室制法:
| 化学药品 | 锌粒和稀硫酸 |
| 反应原理 | Zn + H2SO4== ZnSO4+ H2↑ |
| 发生装置 | 反应物状态为固态和液态,反应条件为室温,可选择实验室制CO2的反应装置(或用过氧化氢溶液制氧气的反应装置)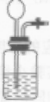 |
| 收集装置 | 向下排空气法或排水法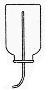  |
| 实验步骤 | ①检验装置的气密性 ②装锌粒(注意将试管横放,把锌粒放入试管口,再慢慢竖起) ③把试管固定在铁架台上 ④加入稀硫酸 ⑤收集气体 |
| 注意事项 | ①不能用浓H2SO4代替稀H2SO4,浓H2SO4具有强氧化性 ②不能用金属活动性顺序表中排在氢后面的金属,如铜,也不能用排在氢前的金属,如钠,一般常用Zn、Al、Fe、Mg等。 ③长颈漏斗末端应在液而以下,防止氢气从长颈漏斗逸出 |
氢气的工业制法:
| 制取方法 | 原理 | 优缺点 |
| 电解水 | 2H2O 2H2↑+O2 2H2↑+O2 |
优点:得到氢气纯度高 缺点:耗能高 |
| 水煤气 | C+H2O(g) CO+H2 CO+H2 |
优点:成本低 缺点:需要设备多(需要除去CO中的杂质) |
| 天然气 | CH4 C+2H2 C+2H2 |
优点:原料丰富 缺点:氢气纯度低 |
| 电解饱和食盐水 | 2NaCl+2H2O 2NaOH+H2↑+Cl2↑ 2NaOH+H2↑+Cl2↑ |
优点:是氯碱化工的副产品 缺点:纯度低 |
| 理想模式:利用太阳能、高效催化剂分解水 | 2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
优点:不耗费电能、热能,环保 缺点:人类未能寻找到高效催化剂,还未能实际应用 |
二氧化碳的制取和收集:
1.原理和药品:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
2.装置:固液混合不加热
(1)发生装置
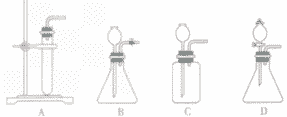
A装置为简易装置,不便于加液体;
B,C使用了长颈漏斗,便于添加液体,使用B、C装置时应注意,长颈漏斗下端管日应伸入液面以下,防止产生的气体从长颈漏斗逸出;
D装置使用了分液漏斗,便于加酸,还可以利用活塞控制反应。
(2)收集装置:二氧化碳溶于水,所以不能用排水法收集;其密度比空气大,所以可采用向上排空气法收集。
如图:
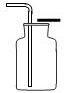
3.现象:块状固体不断溶解,产生大量气泡。
4.检验:把产生的气体通入澄清石灰水,若澄清石灰水变浑浊,证明是二氧化碳。
5.验满:将燃着的木条放在集气瓶口,如果木条的火焰熄灭,证明已集满。
6.实验步骤
a.检查装置的气密性;
b.装入石灰石(或大理石);
c. 塞紧双孔塞;
d.从长颈漏斗中加入稀盐酸;
e.收集气体;
f.验满。
7.注意事项:反应物不能用浓盐酸、硫酸、因为浓盐酸易挥发,会挥发出氯化氢气体,使制得的二氧化碳不纯;硫酸不会挥发,但会生成硫酸钙沉淀,沉淀的硫酸根附着在碳酸钙(或石灰石)表面,使碳酸钙(或石灰石)与酸的接触面积变小,最后反应停止!
实验室制取二氧化碳的选择:
实验室用大理石或石灰石(主要成分是碳酸钙)和稀盐酸制取二氧化碳。
注意:
(1)不能选用稀硫酸,因为稀硫酸与碳酸钙反应生成微溶于水的硫酸钙会橙盖在碳酸钙的表面,阻止反应继续进行。
(2)不能选用浓盐酸,因为浓盐酸易挥发,得不到纯净的二氧化碳气体。
(3)不能用碳酸钠代替石灰石,因为反应太剧烈,产生的气体难以收集。反应速率的快慢与反应物的质量分数和接触面积有关。反应物的接触面积越大,反应物的质量分数越大,反应速率就越快,反之,则越慢。
各组物质反应情况如下表所示:
| 药品 | 反应速率 |
| 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| 石灰石粉末和稀盐酸 | 产生气泡速率很快 |
| 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
氢气检验和验满方法:
1.检验:点燃待检测的气体,在火焰上方罩一个干燥的烧杯有水珠出现,滴入澄清石灰水
不变浑浊,则证明有氢气的存在
2.验满:一般使用排水法收集比较纯净的氢气,可以根据液面的高度判断。
向下排空气法:把带火星的木条放到瓶口,若有轻微的爆鸣声,说明氢气已满。
1.检验:点燃待检测的气体,在火焰上方罩一个干燥的烧杯有水珠出现,滴入澄清石灰水
不变浑浊,则证明有氢气的存在
2.验满:一般使用排水法收集比较纯净的氢气,可以根据液面的高度判断。
向下排空气法:把带火星的木条放到瓶口,若有轻微的爆鸣声,说明氢气已满。
二氧化碳的检验和验满:
1.检验:用燃着的木条检验,如果木条熄灭,则证明有二氧化碳存在;
或用澄清石灰水检验,如果澄清石灰水变浑浊,则证明有二氧化碳存在

2.验满:将燃着的木条放在瓶口,若熄灭则证明二氧化碳已满
常见气体的检验:
1.检验:用燃着的木条检验,如果木条熄灭,则证明有二氧化碳存在;
或用澄清石灰水检验,如果澄清石灰水变浑浊,则证明有二氧化碳存在

2.验满:将燃着的木条放在瓶口,若熄灭则证明二氧化碳已满
常见气体的检验:
| 物质 | 检验试剂或方法或装置或步骤 | 反应现象 | 结论和化学式 |
| O2 | 带火星的木条 | 木条复燃 | 氧气能支持燃烧 |
| CO2 | 澄清石灰水 | 澄清石灰水变浑浊 | CO2+Ca(OH )2==CaCO3↓+H2O |
| CO | 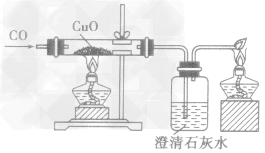 |
氧化铜由黑色变成红色,澄清石灰水变浑浊 | CO+CuO Cu+CO2 Cu+CO2Ca(OH)2+CO2==CaCO3↓+H2O |
| H2 |  |
氧化铜由黑色变成红色,无水CuSO4变成蓝色 | H2+CuO H2O+Cu H2O+CuCuSO4+5H2O==CuSO4·5H2O |
| H2O(g) |  |
无水CuSO4变蓝 | CuSO4+5H2O==CuSO4·5H2O |
| CH4 | (1)点燃 (2)火焰上方罩一个干燥的烧杯 (3)罩一个内壁用澄清石灰水润洗过的烧杯 |
(1)产生蓝色火焰 (2)烧杯内壁有水珠生成 (3)澄清石灰水变浑浊 |
CH4+O2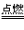 CO2+H2O CO2+H2OCa(OH)2+CO2==CaCO3↓+H2O |
| NH3 | (1)闻气味 (2)利用湿润的红色石蕊试纸检验 |
(1)有氨臭味 (2)湿润的红色石蕊试纸变蓝 |
—— |
发现相似题
与“在一节化学实验探究课上,张老师拿出两瓶无标签的试剂,分别...”考查相似的试题有:
- 请根据下列装置图回答问题。① ② A B C D E F(1)写出图中仪器①、②的名称 ① ,② 。(2)小李在实验室中用氯酸钾和另一种固体...
- 下列装置中,不能用作实验室制取二氧化碳发生装置的是小试管 A B C D
- 下图A与B是实验室常用来制取气体的装置,根据所学知识回答以下问题:(1) 装置B表示正在用高锰酸钾制取氧气,其中还缺少的仪...
- (2012•南充)在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探...
- 化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合下列实验装置图回答问题:(1)写出指...
- 氯气有毒,实验室制取氯气的原理是:MnO2+4HCl(浓)MnCl2+Cl2↑+2X.下列说法错误的是( )A.可采用制取二氧化碳的装置制取...
- 实验室制取二氧化碳所用的酸是___________,不能用硫酸,这是因为________________;也不能用浓盐酸代替稀盐酸,因为浓盐酸有...
- 下列A-D是初中化学中的四个实验,请按要求填空:(1)D实验中烧杯③的作用是__________ ,(2)B实验成功的关键是____________...
- 实验室有如图所示的实验装置:(1) 写出图中有标号仪器的名称:a._____________ b._____________(2) 实验室制取气体时均应先...
- 对实验进行改进是创新的表现方式之一.下图是某研究性学习小组设计的几种装置,请你分析并回答下列问题:(1)A装置中所用玻...