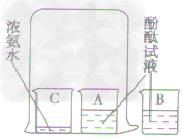
本试题 “下图所示的实验不能达到实验目的的是[ ]A.B.C.D.” 主要考查您对测容器—量筒
二氧化碳的性质实验
验证分子特点的实验
空气的成分
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 测容器—量筒
- 二氧化碳的性质实验
- 验证分子特点的实验
- 空气的成分
概念:
量筒是用来量取液体的一种玻璃仪器。量筒是量度液体体积的仪器。规格以所能量度的最大容量(ml)表示,常用的有10ml、25ml、50ml、100ml、250ml、500ml、1000ml等。外壁刻度都是以ml为单位,10ml量简每小格表示0.2ml,而50ml量筒每小格表示1ml。可见量筒越大,管径越粗,其精确度越小,由视线的偏差所造成的读数误差也越大。所以,实验中应根据所取溶液的体积,尽量选用能一次量取的最小规格的量筒。分次量取也能引起误差。如量取70ml液体,应选用100ml量筒。
量筒的使用:
(1)怎样把液体注入量筒?
向量筒里注入液体时,应用左手拿住量筒,使量筒略倾斜,右手拿试剂瓶,使量筒量筒瓶口紧挨着量筒口,使液体缓缓流入。待注入的量比所需要的量稍少时,把量筒放平,改用胶头滴管滴加到所需要的量。
(2)量筒的刻度应向哪边?
量筒没有“0”的刻度,一般起始刻度为总容积的1/10。不少化学书上的实验图,量筒的刻度面都背着人,这很不方便。因为视线要透过两层玻璃和液体,若液体是浑浊的,就更看不清刻度,而且刻度数字也不顺眼。所以刻度面对着人才好。
(3)什么时候读出所取液体的体积数?
注入液体后,等1~2分钟,使附着在内壁上的液体流下来,再读出刻度值。否则,读出的数值偏小。
(4)怎样读出所取液体的体积数?
应把量筒放在平整的桌面上,观察刻度时,视线与量筒内液体的凹液面的最低处保持水平,再读出所取液体的体积数。否则,读数会偏高或偏低。
(5)量筒能否加热或量取过热的液体?
量筒面的刻度是指温度在20℃时的体积数。温度升高,量筒发生热膨胀,容积会增大。由此可知,量筒是不能加热的,也不能用于量取过热的液体,更不能在量筒中进行化学反应或配制溶液。
(6)从量筒中倒出液体后是否要用水冲洗量筒?
这要看具体情况而定。如果仅仅是为了使测量准确,没有必要用水冲洗量筒,因为制造量筒时已经考虑到有残留液体这一点。相反,如果冲洗反而使所取体积偏大。如果要用同一量筒再量别的液体,就必须用水冲洗干净,为防止杂质的污染。 注:量筒一般只能用于精度要求不很严格时使用,通常应用于定性分析方面,一般不用于定量分析,因为量筒的误差较大。量筒一般不需估读,因为量筒是粗量器,但有时也需估读,如物理电学量器中的电流表,是否估读尚无定论。
(7)关于量筒仰视与俯视的问题:在看量筒的容积时是看水面的中心点,俯视时视线斜向下视线与筒壁的交点在水面上所以读到的数据偏高,实际量取溶液值偏低,仰视是视线斜向上视线与筒壁的交点在水面下所以读到的数据偏低,实际量取溶液值偏高。
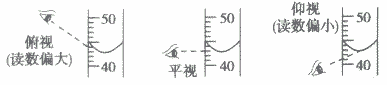
(8)量筒不能直接加热不能在量筒里进行化学反应不能在量筒里配制溶液的原因:
①量筒容积太小,不适宜进行反应
②不能在量筒内稀释或配制溶液,不能对量筒加热,所以不易配制溶液。
③不能在量筒里进行化学反应,以免对量筒产生伤害,有时甚至会发生危险。
④反应可能放热 注意:在量液体时,要根据所量的体积来选择大小恰当的量筒(否则会造成较大的误差),读数时应将量筒垂直平稳放在桌面上,并使量筒的刻度与量筒内的液体凹液面的最低点保持在同一水平面。一般来说量筒是直径越细越好,这样的精确度更高,因为圆形的面积只能计算粗略数,所以直径愈大,误差愈大。
(9)量筒的刻度是从几开始?
最低刻度通常来说是最大刻度的十分之一。比如最大刻度为10mL量筒标准最低刻度1mL,500mL的量筒则最低刻度应为50mL。
解题技巧:
(1)定物量液:是指对某一未知体积的液态物质用量筒量其体积。
例:要量出一杯酒精的体积。方法:
①选择大小合适的量筒。即选用体积略大于一杯酒精灯体积的量筒。
②将烧杯中的酒精倒入量筒中。
③将量筒放平,平视凹液向的最低点,读数即为这杯酒精的体积。若俯视,读数偏高;若仰视,则读数偏低。
(2)定量量液:是指用量筒量取一定体积的某液态物质。例:要量取80mL的水。方法:
①选择100mL的量筒。
②向量筒中倾倒水至接近80mL.刻度线时,改用胶头滴管滴加水至视线在同一水平线上,所量取水的体积即为80mL。若俯视读数,则实际量偏低;若仰视读数,则实际量偏高。
量筒是用来量取液体的一种玻璃仪器。量筒是量度液体体积的仪器。规格以所能量度的最大容量(ml)表示,常用的有10ml、25ml、50ml、100ml、250ml、500ml、1000ml等。外壁刻度都是以ml为单位,10ml量简每小格表示0.2ml,而50ml量筒每小格表示1ml。可见量筒越大,管径越粗,其精确度越小,由视线的偏差所造成的读数误差也越大。所以,实验中应根据所取溶液的体积,尽量选用能一次量取的最小规格的量筒。分次量取也能引起误差。如量取70ml液体,应选用100ml量筒。
量筒的使用:
(1)怎样把液体注入量筒?
向量筒里注入液体时,应用左手拿住量筒,使量筒略倾斜,右手拿试剂瓶,使量筒量筒瓶口紧挨着量筒口,使液体缓缓流入。待注入的量比所需要的量稍少时,把量筒放平,改用胶头滴管滴加到所需要的量。
(2)量筒的刻度应向哪边?
量筒没有“0”的刻度,一般起始刻度为总容积的1/10。不少化学书上的实验图,量筒的刻度面都背着人,这很不方便。因为视线要透过两层玻璃和液体,若液体是浑浊的,就更看不清刻度,而且刻度数字也不顺眼。所以刻度面对着人才好。
(3)什么时候读出所取液体的体积数?
注入液体后,等1~2分钟,使附着在内壁上的液体流下来,再读出刻度值。否则,读出的数值偏小。
(4)怎样读出所取液体的体积数?
应把量筒放在平整的桌面上,观察刻度时,视线与量筒内液体的凹液面的最低处保持水平,再读出所取液体的体积数。否则,读数会偏高或偏低。
(5)量筒能否加热或量取过热的液体?
量筒面的刻度是指温度在20℃时的体积数。温度升高,量筒发生热膨胀,容积会增大。由此可知,量筒是不能加热的,也不能用于量取过热的液体,更不能在量筒中进行化学反应或配制溶液。
(6)从量筒中倒出液体后是否要用水冲洗量筒?
这要看具体情况而定。如果仅仅是为了使测量准确,没有必要用水冲洗量筒,因为制造量筒时已经考虑到有残留液体这一点。相反,如果冲洗反而使所取体积偏大。如果要用同一量筒再量别的液体,就必须用水冲洗干净,为防止杂质的污染。 注:量筒一般只能用于精度要求不很严格时使用,通常应用于定性分析方面,一般不用于定量分析,因为量筒的误差较大。量筒一般不需估读,因为量筒是粗量器,但有时也需估读,如物理电学量器中的电流表,是否估读尚无定论。
(7)关于量筒仰视与俯视的问题:在看量筒的容积时是看水面的中心点,俯视时视线斜向下视线与筒壁的交点在水面上所以读到的数据偏高,实际量取溶液值偏低,仰视是视线斜向上视线与筒壁的交点在水面下所以读到的数据偏低,实际量取溶液值偏高。
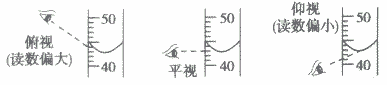
(8)量筒不能直接加热不能在量筒里进行化学反应不能在量筒里配制溶液的原因:
①量筒容积太小,不适宜进行反应
②不能在量筒内稀释或配制溶液,不能对量筒加热,所以不易配制溶液。
③不能在量筒里进行化学反应,以免对量筒产生伤害,有时甚至会发生危险。
④反应可能放热 注意:在量液体时,要根据所量的体积来选择大小恰当的量筒(否则会造成较大的误差),读数时应将量筒垂直平稳放在桌面上,并使量筒的刻度与量筒内的液体凹液面的最低点保持在同一水平面。一般来说量筒是直径越细越好,这样的精确度更高,因为圆形的面积只能计算粗略数,所以直径愈大,误差愈大。
(9)量筒的刻度是从几开始?
最低刻度通常来说是最大刻度的十分之一。比如最大刻度为10mL量筒标准最低刻度1mL,500mL的量筒则最低刻度应为50mL。
解题技巧:
(1)定物量液:是指对某一未知体积的液态物质用量筒量其体积。
例:要量出一杯酒精的体积。方法:
①选择大小合适的量筒。即选用体积略大于一杯酒精灯体积的量筒。
②将烧杯中的酒精倒入量筒中。
③将量筒放平,平视凹液向的最低点,读数即为这杯酒精的体积。若俯视,读数偏高;若仰视,则读数偏低。
(2)定量量液:是指用量筒量取一定体积的某液态物质。例:要量取80mL的水。方法:
①选择100mL的量筒。
②向量筒中倾倒水至接近80mL.刻度线时,改用胶头滴管滴加水至视线在同一水平线上,所量取水的体积即为80mL。若俯视读数,则实际量偏低;若仰视读数,则实际量偏高。
探究二氧化碳的三个性质实验:
1.证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
2.二氧化碳溶于水显酸性
3.二氧化碳能溶于水
二氧化碳性质探究实验:
1.证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
(1)装置: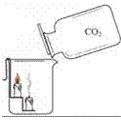
(2)现象:蜡烛由低到高依次熄灭
结论:证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
2.二氧化碳溶于水显酸性
(1)装置:
(2)现象:1和4实验中的白花变红,2和3白花不变色
(3)结论:二氧化碳不能使紫色石蕊试液变红,二氧化碳的水溶液能使紫色石蕊试液变红。
(或二氧化碳溶于水显酸性)
3.二氧化碳能溶于水
(1)装置: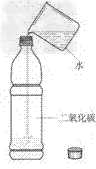
(2)现象:塑料瓶变瘪
(3)结论:二氧化碳能溶于水。
1.证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
2.二氧化碳溶于水显酸性
3.二氧化碳能溶于水
二氧化碳性质探究实验:
1.证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
(1)装置:

(2)现象:蜡烛由低到高依次熄灭
结论:证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
2.二氧化碳溶于水显酸性
(1)装置:

(2)现象:1和4实验中的白花变红,2和3白花不变色
(3)结论:二氧化碳不能使紫色石蕊试液变红,二氧化碳的水溶液能使紫色石蕊试液变红。
(或二氧化碳溶于水显酸性)
3.二氧化碳能溶于水
(1)装置:

(2)现象:塑料瓶变瘪
(3)结论:二氧化碳能溶于水。
验证分子特点的实验:
通过对分子特点的探究,可以让学生直观的感受到微观世界里分子构成物质的特点。
探究分子运动的实验:
| 实验装置 |
| ||
| 实验步骤 | 步骤1 | 步骤2 | 步骤3 |
| 在盛有约40ml 蒸馏水的烧杯中加 如5一6滴酚酞试液,搅拌均匀, 观察现象 |
取步骤I得到的溶液,置于 试管中,再向其中滴加浓 氨水,观察现象 |
将烧杯中的溶液分别倒入 A、B两个小烧杯中,另取 一个小烧杯C,加入约5ml 浓 氨水。用一个大烧杯罩住 A,C两个小烧杯,烧杯B 置于大烧杯外 | |
| 实验现象 | 无明显现象 | 溶液由无色变成红色 | 烧杯A中液体由无色变为红色,烧杯B中无变化 |
| 实验解释 | 烧杯中的浓氨水挥发出氛分子,氨分了进人烧杯A中,使溶液变成红色.而烧杯B中没有氨分子进入 | ||
探究分子间有间隙的实验:
| 实验原理 | 分子之间存在间隙且分子总是做不停地无规则运动。将水和酒精充满容量瓶,混合均匀后,若液面发生下降,则可验证分子间存在间隙。 | ||
| 实验用品 | 100ml 容量瓶 1 只、 100ml 烧杯 2 只、餐纸、保鲜膜、棉线一根、无水酒精、 纯净水、品红溶液。 | ||
| 实验装置 | 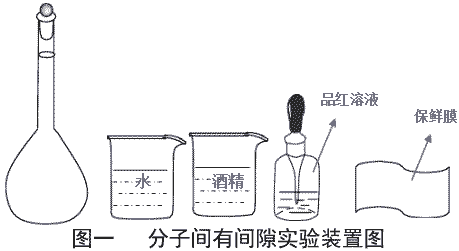 | ||
| 实验步骤 | 实验结果 | 实验结论 | |
| 实验方案一 | (1) 打开容量瓶,用小烧杯移取 70ml 已滴加了品红溶液的水于容量瓶中。 (2) 用小烧杯移取酒精于容量瓶中直至容量瓶满。 (3) 塞上容量瓶塞,有液体溢出,用餐纸擦干。倒置容量瓶几次,使液体充分混 合,观察液面下降情况。 |
液面下降 1.5cm 左右,实验现象非常明显 | 优点: (1) 酒精用量少,该实验只需耗费 30ml 左右的酒精 (2) 滴入品红溶液的水呈红色,可明显观察到在容量瓶倒置前,容量瓶中液体分 层,上层无色,下层红色。而倒置后溶液呈均匀红色。 (3) 倒置前容量瓶充满液体,排除了会有部分液体残留在容量瓶上导致的误差。 (4) 实验现象明显,混合后液面下降 1.5cm 左右 (5) 实验操作简单,实验用品少 缺点:将充满的容量瓶塞上容量瓶塞会有液体溢出,这个操作不规范。 |
| 实验方案二 | (1) 打开容量瓶,用小烧杯移取 70ml 已滴加了品红溶液的水于容量瓶中。 (2) 用小烧杯移取酒精于容量瓶中直至容量瓶满。 (3) 用保鲜膜迅速包裹容量瓶,然后将保鲜膜用细线捆紧。用手掌压住容量瓶口, 倒置容量瓶几次,使液体充分混合,观察液面下降情况。 |
液面下降 1cm 左右,实验现象非常明显。用无水硫酸铜检验容量瓶外壁, 并无液体溢出。 | 优点: (1) 酒精用量少,该实验只需耗费 30ml 左右的酒精 (2) 滴入品红溶液的水呈红色,可明显观察到在容量瓶倒置前,容量瓶中液体分 层,上层无色,下层红色。而倒置后溶液呈均匀红色。 (3) 倒置前容量瓶充满液体,排除了会有部分液体残留在容量瓶上导致的误差。 (4) 实验现象明显,混合后液面下降 1cm 左右 (5) 实验操作简单,实验用品少 (6) 方案二很好的解决了方案一的缺陷,且实验效果好。 |
空气的成分:
氧气,二氧化碳,氢气,氮气,稀有气体;按体积分:N2占78%,O2占21%,稀有气体占0.94%,二氧化碳占0.03%,其他气体和杂质占0.03%。
易错点:
空气中各成分的含量在一定时间和一定范围内基本恒定,但随着人类活动的延续,气体的排放,空气的成分也在不停地变化,因此不能认为空气的成分是一成不变的。
氧气,二氧化碳,氢气,氮气,稀有气体;按体积分:N2占78%,O2占21%,稀有气体占0.94%,二氧化碳占0.03%,其他气体和杂质占0.03%。
易错点:
空气中各成分的含量在一定时间和一定范围内基本恒定,但随着人类活动的延续,气体的排放,空气的成分也在不停地变化,因此不能认为空气的成分是一成不变的。
发现相似题
与“下图所示的实验不能达到实验目的的是[ ]A.B.C.D.”考查相似的试题有:
- 看图回答问题(1)下列实验操作图中,正确的是______、______(填字母).(2)指出上图中两个不正确的实验操作及可能造成的...
- 下列有关仪器使用或用途的叙述中正确的是A.试管:用酒精灯加热试管里的液体时,试管内的液体不应超过试管容积的 2/3B.胶头...
- 下图所示实验基本操作正确的是( )A.给试管里的液体加热B.读取液体体积C.物质的称量D.点燃酒精灯
- 在化学实验中,对于用剩的化学药品,处理方法正确的是A.为节约倒回原试剂瓶 B.带回家做家庭小实验C.倒入下水道以防止污染...
- 下列反应属于置换反应的是( )A.3NO2+H2O=2HNO3+NOB.2KMnO4K2MnO4+MnO2+O2↑C.C+H2OCO+H2D.CO+CuOCu+CO2
- (6分)小明和小红对市场上销售的一种分袋包装的豆奶粉发生了兴趣,因为豆奶粉装在充满气体的小塑料袋内,袋内的气体充得鼓鼓...
- (2011?张掖)收获季节一进入四会、广宁、德庆的橘园,就可以闻到柑橘的香味.这是因为( )A.分子在不停运动B.分子间有间...
- 唐代诗人李峤有一首绝句:“解落三秋叶,能开二月花.过江千尺浪,入林万竿斜”.诗中揭示的自然现象是 ______,证明了 ______...
- 下列物质中含有氧气的是( )A.二氧化锰B.氯酸钾C.空气D.氧化镁
- 实验操作必须规范,下列操作其结果可能偏小的是( )A.50g浓硫酸敞口放置于空气中一段时间后溶液的质量B.用水润湿后的pH试...