本试题 “下列叙述正确的是[ ]A.H2O2、SO2、氯水、过氧化钠、臭氧、活性炭都有漂白性,其原理相同B.将SO2通入BaCl2溶液中可生成BaSO4沉淀C.检验SO2中含有CO2的方法...” 主要考查您对过氧化钠
氯水
二氧化硫
臭氧
过氧化氢
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 过氧化钠
- 氯水
- 二氧化硫
- 臭氧
- 过氧化氢
过氧化钠(Na2O2)的基本性质:
淡黄色固体,较稳定,可用作供氧剂、漂白剂
(1)与水反应:2Na2O2+2H2O==4NaOH+O2↑
(2)与CO2反应:2Na2O2+2CO2==2Na2CO3+ O2
(3)与HCl反应:2Na2O2+4HCl==4NaCl+2H2O+ O2↑
过氧化钠的特性及计算:
1.过氧化钠的强氧化性
2.Na2O2与CO2、H2O(g)反应的重要关系
(1)气体体积差的关系
2Na2O2+2CO2===2Na2CO3+O2 气体体积差 ①
2 1 ΔV=1
2Na2O2+2H2O(g)===4NaOH+O2 气体体积差 ②
2 1 ΔV=1
由此可见,若CO2和水蒸气的混合气体(或单一气体)通过足量Na2O2,气体体积的减少量是原气体体积的1/2,即为生成氧气的量。
(2)先后顺序关系
一定量的Na2O2与一定量的CO2和H2O(g)的混合物反应,可视为Na2O2首先与CO2反应,剩余的Na2O2再与H2O(g)反应。
(3)电子转移关系
当Na2O2与CO2或H2O反应时,每产生1molO2就转移2mol电子。
(4)固体质量变化关系
①足量过氧化钠与水、CO2反应的计算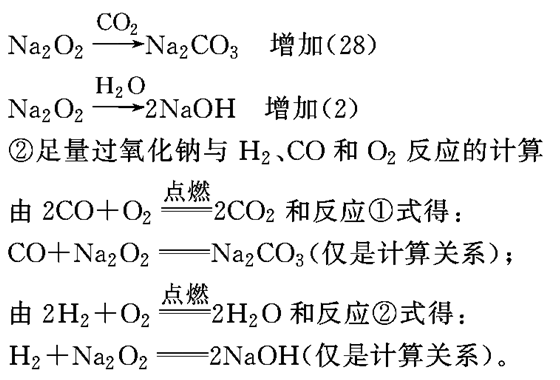
所以,有ag通式符合(CO)m(H2)n(m=0,1,2,3…,n=0,1,2,3…)的物质(包括纯净物和混合物)在氧气中燃烧,将其通过足量过氧化钠,反应完毕后,固体增重ag。
氧化钠与过氧化钠的比较:
| 物质 | 氧化钠 | 过氧化钠 |
| 色态 | 白色固体 | 淡黄色固体 |
| 类别 | 碱性氧化物 |
过氧化物(不属于碱性氧化物) |
| 化学键类型 | 仅含离子键 | 离子键和非极性键 |
| 电子式 | 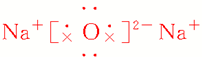 |
 |
| 生成条件 | 常温 | 点燃或加热 |
| 氧的化合价 | -2 | -1 |
| 阴阳离子个数比 | 1:2 | 1:2 |
| 稳定性 | 不稳定 | 稳定 |
| 转化关系 | 2Na2O+O2=2Na2O2 | |
| 用途 | 用于制取少量过氧化钠 | 供氧剂、漂白剂、氧化剂 |
| 与水反应方程式 | 2Na2O+2H2O=2NaOH | 2Na2O2+2H2O=4NaOH+O2↑ |
| 与CO2反应 | Na2O+CO2=NaCO3 | 2Na2O2+2CO2=2Na2CO3+O2↑ |
| 与HCl反应 | Na2O+2HCl=2NaCl+H2O | 2Na2O2+4HCl=4NaCl+2H2O+O2↑ |
| 保存 | 隔绝空气、密封保存 | 隔绝空气、远离易燃物、密封保存 |
特别提醒:
(1)用脱脂棉包裹住过氧化钠,滴加少量水时脱脂棉可以燃烧,不仅可以说明Na2O2与H2O反应生成O2,还可以说明该反应放热。
(2)Na2O2与H2O反应时H2O既不是氧化剂也不是还原剂。
方法技巧:Na2O与Na2O2的结构与性质
(1)Na2O中只含离子键,Na2O2中既含离子键,又含非极性键。
(2)等物质的量的Na2O与Na2O2分别于等量且足量的H2O反应,所得溶液的成分浓度相同
氯水的成分:
新制氯水中存在的分子有盐酸(HCl)、次氯酸(HClO),水(H2O)、还有氯气
氯水的性质:
新制氯水呈黄绿色、有刺激性气味,属于混合物,其所含的多种微粒使氯水的化学性质表现出多重性。
①氯水的Cl2氧化性,只表现氯水的氧化性
A. 在某些含非金属阴离子的溶液中加氯水。
| 氯水滴加溶液 | 反应方程式 | 实验现象 |
| KI溶液 | 2KI+Cl2==2KCl+I2 | 溶液由无色变橙黄色 |
| NaBr溶液 | 2NaBr+Cl2==NaCl+Br2 | 溶液由无色变橙色 |
| K2S溶液 | K2S+Cl2==2KCl+S↓ | 溶液变浑浊 |
| Na2SO3溶液 | Na2SO3+Cl2+H2O==Na2SO4+2HCl | 氯水颜色褪去 |
C. 某些强还原性的气体通入氯水中,氯气将其氧化。
| 通入的气体 | 化学方程式 | 实验现象 |
| H2S | H2S+Cl2==2HCl+S↓ | 溶液出现浑浊 |
| HBr | 2HBr+Cl2==2HCl+Br2 | 溶液由浅黄绿色变橙色 |
| HI | 2HI+Cl2==2HCl+I2 | 溶液由浅黄色变橙黄色 |
| SO2 | SO2+Cl2+2H2O==H2SO4+2HCl | 溶液浅黄色褪去 |
A. 新制氯水滴入NaOH溶液等强碱溶液中,氯水褪色:
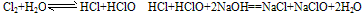
B. 新制氯水中滴加紫色石蕊试液时,溶液先变红色,后褪色,是盐酸的强酸性和次氯酸的强氧化性共同作用的结果。 ③氯水中次氯酸的强氧化性。
新制氯水起漂白作用时,是由于HClO的强氧化性将色素氧化使之褪色的结果,也是Cl2的漂白、杀菌、消毒作用必须有水存在的根本原因。
④氯水中盐酸的强酸性。
在AgNO3溶液中滴加适量的氯水,有白色沉淀生成。是氯水中的HCl与AgNO3作用的结果。
⑤氯水中盐酸的强酸性和氯气的强氧化性共同起作用。
向氯水中加镁粉、铝粉等活泼金属时,可观察到氯水颜色褪去且有气泡冒出,氯水中的Cl2和HCl与镁、铝共同作用的结果。
有关氯水问题的分析方法:
1.氯水性质的多样性
氯气溶于水形成的溶液叫氯水,新制的氯水呈浅黄绿色,有刺激性气味。氯水中存在三个平衡:
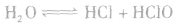 ,
,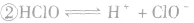 ,
,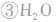
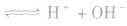 。所以,在氯水中存在三种分子:Cl2、 H2O、HClO;四种离子:H+、Cl-、ClO-及少量OH-。由于在光照条件下HClO可分解
。所以,在氯水中存在三种分子:Cl2、 H2O、HClO;四种离子:H+、Cl-、ClO-及少量OH-。由于在光照条件下HClO可分解
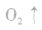 ,故久置的氯水为盐酸。
,故久置的氯水为盐酸。
(1)氯水的性质氯水在与不同物质发生反应时,表现出成分的复杂性和性质的多样性。
说明:
①氯水通常现用现制,可短时间密封保存于棕色试剂瓶中(见光或受热易分解的物质均保存在棕色试剂瓶中);
②Cl:使湿润的蓝色石蕊试纸先变红,后褪色。
(2)新制氯水、久置氯水、液氯的区别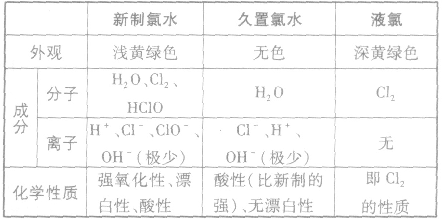
外界因素对平衡 的影响:
的影响:
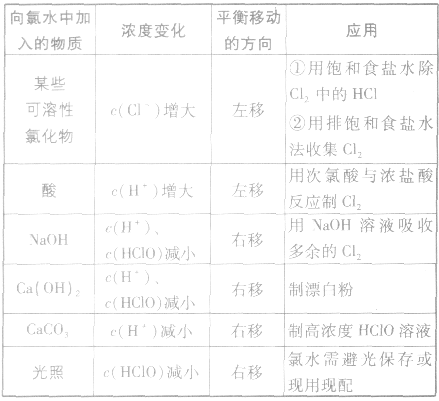
卤离子的检验方法:
1.银盐法:
特别提醒:加入稀HNO3的目的是防止CO32-、 PO43-等离子的干扰。有关反应为: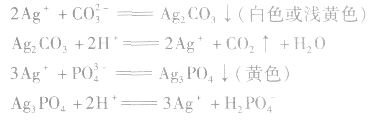
2.置换一萃取法
3.置换一淀粉法检验I-
①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:


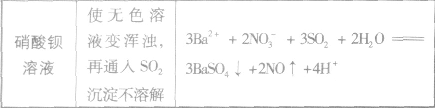
SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表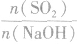 ,如下数轴所示:
,如下数轴所示: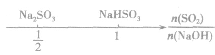
分析数轴可得:
(1)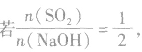 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2)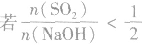 ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3)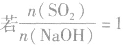 ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4)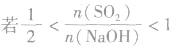 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5)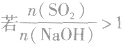 ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。
二氧化硫的制备:
工业制法:

实验室制法:
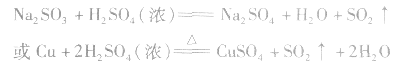
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

臭氧:
在常温常压下,臭氧是一种有特殊臭味的淡蓝色气体,它的密度比氧气的大。液态臭氧呈深蓝色,沸点为-112.4摄氏度,固态臭氧呈紫黑色,熔点为-251摄氏度。
化学:不稳定,具有极强的氧化性,可用于漂白和消毒
氧气和臭氧的性质比较:
| 名称 | 氧气 | 臭氧 |
| 化学式 | O2 | O3 |
| 相对分子质量 | 32 | 48 |
| 分子空间构型 | 直线型 | V形 |
| 物理性质 | 通常为无色、无味的气体,液态氧为淡蓝色,固态氧为雪花状、淡蓝色。不易溶于水,在常温下 1L水中只能溶解约30mL的氧气。在标准状况下的密度为1.43g/L。熔点54.6K,沸点90K | 通常为有特殊臭味的淡蓝色气体,在水中的溶解度比氧气大。在标准状况F的密度为 2.143g/L。熔点22K,沸点160。6K。液态臭氧呈深蓝色,固态臭氧呈紫黑色 |
| 相互转化 |  |
 |
| 化学性质 | 氧的电负性仅次于氟,但由于O2的分子结构稳定,O2的化学性质不太活泼。在加热或点燃等条件下,O2能氧化除稀有气体、卤素和某些贵重金属以外的金属、非金属单质,众多的还原性化合物 | O3不稳定,在常温下缓慢分解生成氧气,加热可加快O,的分解,MnO2、PbO2、铂黑、氯原子等也能促进O3的分解;O3是极强的氧化剂,煤气、松节油等在O3中能自燃,许多有机色素能被O3氧化,使发色基团遭到破坏变为无色物质。在室温时,O3可将PbS等氧化: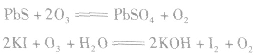 |
| 制法 | O2的工业制法是分离液态空气和电解水。分离液态空气是工业上制取O2最重要的方法。液态氧的沸点(90K)比液态氮的沸点(77K)高,因此氮气首先从液态空气中蒸发出来,剩下的主要就是液态氧了 | 一般使O2通过无声放电的O3发生器来制取O3 |
| 用途 | O2是人类赖以生存的最重要的一种物质。O2在工业上有重要用途,例如利用乙炔在O2中燃烧产生的高温能熔化金属,达到焊接或切割金属的目的;利用纯O2代替空气不但可以加快化学反应速率,还可降低能耗;用纯O2冶炼钢铁,用富氧空气生产氮肥,都取得了很好的效果。另外,O2在医疗中常用来抢救缺氧或呼吸困难的危重病人 | O3的用途主要是利用它的氧化性。近年来,O3在环境保护、漂白等方面日益显示它的作用,例如 O3能使有毒的氰化物、酚等变为无毒物质;能杀死许多细菌;用O3代替Cl2对饮用水消毒,不但杀菌效果好,而且不会带入异昧,且能避免水中产生有副作用的有机氯 |
氧族元素:

过氧化氢:
俗称,双氧水,基本结构为H-O-O-H,但并不是直线结构,因此有极性,是极性分子;O上有孤电子对,因此O-O键很弱易断。
过氧化氢和水的性质比较:


与“下列叙述正确的是[ ]A.H2O2、SO2、氯水、过氧化钠、臭氧、活...”考查相似的试题有:
- xgNa2O和ygNa2O2分别加入等质量的水中(水足量),结果得到等质量分数的溶液,则A与B关系正确的是[ ]A.x = yB.x > yC.x
- 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠...
- (10分)A-G的转化关系如图所示(部分反应物、产物和反应条件未标出)已知:①A、B为中学化学常见的金属单质;C-G均为化合物,...
- 现有碳酸钠、碳酸氢钠、氢氧化钠、氯化铁和苯酚五种物质的溶液,它们之间有如图所示转化关系,图中每条线两端的物质可以发生...
- (3分)运用比较方法是化学科学中研究物质性质的基本方法之一,请运用比较法解答下题:过氧化钠几乎可与所有的常见气态非金属...
- 与水反应生成碱并放出气体的是( )A.F2B.Na2OC.Na2O2D.K
- (10分) 硫酸的消费量是衡量一个国家化工生产水平的重要标志。(1)V2O5是SO2与O2反应的催化剂,请写出该反应的方程式:________...
- 下列叙述正确的是[ ]A.硫在过量的氧气中燃烧生成三氧化硫B.二氧化硫通入BaCl2溶液中生成BaSO3白色沉淀C.二氧化硫通入滴有...
- 下列有关二氧化硫的说法中,正确的是A.检验SO2气体中是否混有CO2的方法是通入澄清石灰水中B.SO2气体具有漂白性,能使品红溶...
- 下列有关说法中正确的是[ ]A.双氧水被称为绿色氧化剂,是因为其还原产物为O2,对环境没有污染B.王水是浓盐酸和浓硝酸按体积...