本试题 “一定条件下,在2SO2+O22SO3的化学平衡体系中,各物质的浓度分别是2.0mol/L、0.8mol/L、2.4mol/L,则氧气在反应起始时的浓度可能是( )A.0.8~2mol/LB.0~2...” 主要考查您对化学反应进行的方向
可逆反应与不可逆反应
化学平衡的有关计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应进行的方向
- 可逆反应与不可逆反应
- 化学平衡的有关计算
化学反应的方向与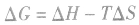 :
:
1.化学反应进行方向的判据
(1)由稳定性弱的物质向稳定性强的物质转变
如 ,稳定性
,稳定性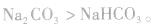
(2)离子反应总是向着使反应体系中某些离子浓度减小的方向进行
①溶解度大的物质向溶解度小的物质转变,如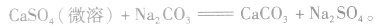
②由相对强酸(碱)向相对弱酸(碱)转变,如 ,
,  所以酸性强弱:
所以酸性强弱: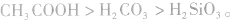
(3)由难挥发性物质向易挥发性物质转变
如 所以沸点:
所以沸点: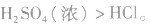
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质转变
如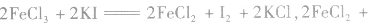
 ,则氧化性:
,则氧化性: 。
。
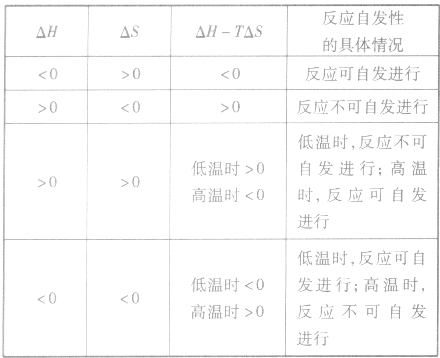
2.焓变和熵变共同判断反应的方向:
在温度、压强一定的条件下,自发反应总是向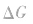
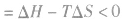 的方向进行,直至达到平衡状态;
的方向进行,直至达到平衡状态;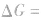
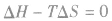 表明反应已达到平衡状态;
表明反应已达到平衡状态;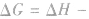
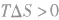 表明反应不能自发进行。
表明反应不能自发进行。
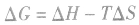 :
:1.化学反应进行方向的判据
(1)由稳定性弱的物质向稳定性强的物质转变
如
 ,稳定性
,稳定性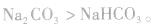
(2)离子反应总是向着使反应体系中某些离子浓度减小的方向进行
①溶解度大的物质向溶解度小的物质转变,如
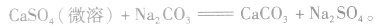
②由相对强酸(碱)向相对弱酸(碱)转变,如
 ,
,  所以酸性强弱:
所以酸性强弱: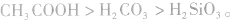
(3)由难挥发性物质向易挥发性物质转变
如
 所以沸点:
所以沸点: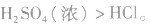
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质转变
如
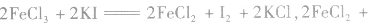
 ,则氧化性:
,则氧化性: 。
。 2.焓变和熵变共同判断反应的方向:
在温度、压强一定的条件下,自发反应总是向
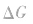
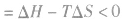 的方向进行,直至达到平衡状态;
的方向进行,直至达到平衡状态;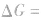
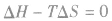 表明反应已达到平衡状态;
表明反应已达到平衡状态;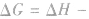
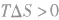 表明反应不能自发进行。
表明反应不能自发进行。
可逆反应与不可逆反应:
(1)可逆反应:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
注:①在可逆反应中,由反应物到生成物的反应叫正反应;由生成物到反应物的反应叫逆反应。
②可逆反应必须是“同一条件”。
(2)不可逆反应:在不同条件下能向两个方向进行的反应为不可逆反应。如:点燃情况下,氢气和氧气能生成水;在通电条件下,水电解能生成氢气和氧气。
可逆反应的特点:
①可逆反应必须是同一条件下既能向正反应方向又能向逆反应方向进行的反应,对于在不同条件下向正、逆反直方向进行的反应则不能认为是可逆反应。
②可逆反应是不能进行到底的,不能实现完全转化
(1)可逆反应:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
注:①在可逆反应中,由反应物到生成物的反应叫正反应;由生成物到反应物的反应叫逆反应。
②可逆反应必须是“同一条件”。
(2)不可逆反应:在不同条件下能向两个方向进行的反应为不可逆反应。如:点燃情况下,氢气和氧气能生成水;在通电条件下,水电解能生成氢气和氧气。
可逆反应的特点:
①可逆反应必须是同一条件下既能向正反应方向又能向逆反应方向进行的反应,对于在不同条件下向正、逆反直方向进行的反应则不能认为是可逆反应。
②可逆反应是不能进行到底的,不能实现完全转化
化学平衡计算的一般思路和方法:
有天化学平衡的计算一般涉及各组分的物质的量、浓度、转化率、百分含量,气体混合物的密度、平均摩尔质量、压强等。通常的思路是写出反应方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的火系,列出比例式或等式或依据平衡常数求解,这种思路和方法通常称为“三段式法”、如恒温恒压下的反应mA(g)+nB(g) pC(g)+ qD(g)
pC(g)+ qD(g)
(1)令A、B的起始物质的量分别为amol,bmol 达到平衡后,A的消耗量为m·xmol,容器容积为VL。
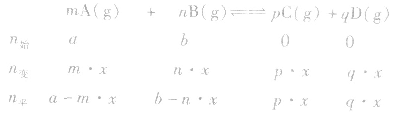
则有:

(2)对于反应物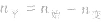 ,对于生成物
,对于生成物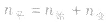
(3)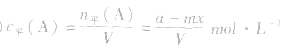
(4)A的转化率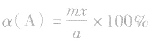
(5)平衡时A的体积(物质的量)分数
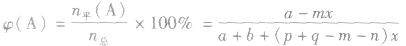
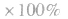
(6)
(7)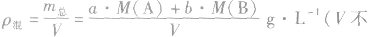
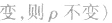
(8)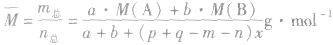
有天化学平衡的计算一般涉及各组分的物质的量、浓度、转化率、百分含量,气体混合物的密度、平均摩尔质量、压强等。通常的思路是写出反应方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的火系,列出比例式或等式或依据平衡常数求解,这种思路和方法通常称为“三段式法”、如恒温恒压下的反应mA(g)+nB(g)
 pC(g)+ qD(g)
pC(g)+ qD(g) (1)令A、B的起始物质的量分别为amol,bmol 达到平衡后,A的消耗量为m·xmol,容器容积为VL。
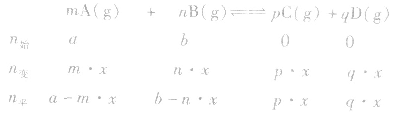
则有:

(2)对于反应物
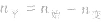 ,对于生成物
,对于生成物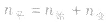
(3)
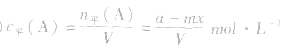
(4)A的转化率
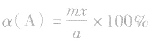
(5)平衡时A的体积(物质的量)分数
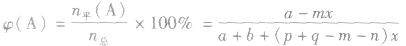
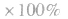
(6)

(7)
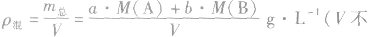
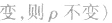
(8)
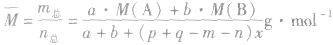
发现相似题
与“一定条件下,在2SO2+O22SO3的化学平衡体系中,各物质的浓度分...”考查相似的试题有:
- 下列说法不正确的是[ ]A.铅蓄电池在放电过程中,负极质量减小,正极质量增加B.常温下,反应不能自发进行,则该反应的C.一...
- 下列反应中属于可逆反应的是( )A.2H2+O22H2OB.6CO2+6H2OC6H12O6+6O2C.Pb+PbO2+2H2SO42PbSO4+2H2OD.C+O22CO(炼铁炉中)
- T℃时,有甲、乙两个密闭容器,甲容器的体积为1L,乙容器的体积为2L,分别向甲、乙两容器中加入6molA和3molB ,发生了如下反应:3A...
- 向5 mL 0.1 mol·L-1的KI溶液中滴加5~6滴0.1 mol·L-1的FeCl3溶液后,再进行下列实验,其中可证明FeCl3溶液和KI溶液的反应是...
- 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)2SO3(g);△H=-190kJ·mol-1(1)该热化学反应方程...
- 在一定温度下将1mol CO和9mol水蒸气放在密闭的容器中发生下列反应:CO(g)+H2O(g)CO2(g)+H2(g)达到平衡后,已知该反应平衡常数...
- 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。(1)目前工...
- 某温度下,容器为2L的密闭容器中发生反应:A(g)+2B(g)⇌2C(g)+xD(g).起始时投入1molA和2molB,2min后达到平衡,生成1...
- 在容积为2.0 L的密闭容器中充入0.60 mol X和1.60 mol Y,发生反应:aX(g)+3Y(g)2Z(g) 经过10 min反应达到平衡状态,Y的浓度为...
- 在一密闭容器中,反应aA(g)bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,达到新的平衡时,B的浓度是原平衡时的60%,...