本试题 ““保护母亲河英溪”这是在英都到仑苍路上的一条广告语,说明现在英溪里的水出现某些问题,镇政府受到重视。某学校的化学兴趣小组对其产生了兴趣,于是某同学取...” 主要考查您对过滤
蒸馏
水污染与防治
硬水和软水
水的净化
纯净物和混合物
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 过滤
- 蒸馏
- 水污染与防治
- 硬水和软水
- 水的净化
- 纯净物和混合物
过滤定义:
利用介质滤除水中杂质的方法。
通过特殊装置将流体提纯净化的过程,过滤的方式很多,使用的物系也很广泛,固-液、固-气、大颗粒、小颗粒都很常见。
在推动力或者其他外力作用下悬浮液(或含固体颗粒发热气体)中的液体(或气体)透过介质,固体颗粒及其他物质被过滤介质截留,从而使固体及其他物质与液体(或气体)分离的操作。
过滤归纳:
| 过滤的原理 | 其中一种能溶于水,另一种不能溶于水,则可以先把它们充分溶于水中,再进行过滤分离 |
| 制作过滤器 | 把一张圆形滤纸连续对折两次,得到一个四层的扇形滤纸,然后再用手捏住最外面一层滤纸展开,便得到一个一边是一层,另一边是三层的滤纸,用少量水润湿一下,把它贴在漏斗内壁上即可。 |
| 用到的仪器 | 铁架台(带铁圈)、烧杯、漏斗、玻璃棒、滤纸等 |
| 过滤装置 | 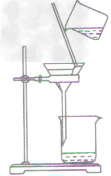 |
| 注意事项 | 操作注意事项有:一贴、二低、三靠。 一贴:滤纸紧贴漏斗内壁,以没有气泡为准,可加快过滤的速度; 二低:滤纸边缘低于漏斗边缘;漏斗内液面低于滤纸边缘,防止液体从滤纸与漏斗之间的间隙流下,使过滤不充分; 三靠:盛待过滤液体的烧杯紧靠引流的玻璃棒,防止液体溅到漏斗外丽;玻璃棒的下端紧靠在三层滤纸上,防止戳破滤纸;漏斗下端长的那侧管口紧靠烧杯内壁,防止液体溅出 |
| 过滤失败的原因 | ①滤纸破损;②过滤时液面高于滤纸边缘; ③收集滤液的烧杯不洁净 |
| 过滤操作实验口诀 | 斗架烧杯玻璃棒,滤纸漏斗角一样。 过滤之前要静置,三靠两低不要忘。 |
定义:
指利用液体混合物中各组分挥发性的差异而将组分分离的传质过程。将液体沸腾产生的蒸气导入冷凝管,使之冷却凝结成液体的一种蒸发、冷凝的过程。
蒸馏是分离沸点相差较大的混合物的一种重要的操作技术,尤其是对于液体混合物的分离有重要的实用意义。
即,蒸馏条件:1.液体是混合物。2.各组分沸点不同。
实验室制蒸馏水:
(1)原理:蒸馏是利用互相溶解的液体混合物中各组分沸点小同进行分离提纯的操作。其过程是:加热样品使其中某组分汽化,然后使蒸气冷凝为液体加以收集。
(2)仪器:铁架台、蒸馏烧瓶、冷凝管、尾接管、锥形瓶、温度计、酒精灯、石棉网等。
(3)装置:
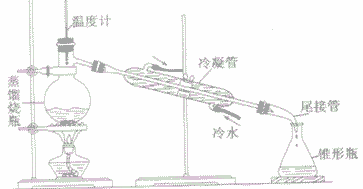
(4)操作:
①用洒精灯外焰给受热仪器先预热后加热
②对蒸馏烧瓶(烧杯、烧瓶、锥形瓶等仪器)加热时,不能直接加热,一定要垫石棉网,蒸馏烧瓶中液体体积为容器容积的1/3—2/3
③温度计不能直接插人蒸馏烧瓶的液体之中,应使温度计水银球与蒸馏烧瓶支管口位于同一水平线上
④蒸馏烧瓶的支管必须露出橡皮塞以防蒸馏出来的液体接触橡皮塞而带入杂质
⑤冷凝管中冷水的走向应是下口进、上口出,以使蒸汽充分冷却。
(5)关键:
①控制好加热温度。如果采用加热浴,加热浴的温度应当比蒸馏液体的沸点高出若干度,否则难以将被蒸馏物蒸馏出来。加热浴温度比蒸馏液体沸点高出的越多,蒸馏速度越快。但是,加热浴的温度也不能过高,否则会导致蒸馏瓶和冷凝器上部的蒸气压超过大气压,有可能产生事故,特别是在蒸馏低沸点物质时尤其需注意。一般地,加热浴的温度不能比蒸馏物质的沸点高出30℃。整个蒸馏过程要随时添加浴液,以保持浴液液面超过瓶中的液面至少一公分。
②蒸馏高沸点物质时,由于易被冷凝,往往蒸气未到达蒸馏烧瓶的侧管处即已经被冷凝而滴回蒸馏瓶中。因此,应选用短颈蒸馏瓶或者采取其它保温措施等,保证蒸馏顺利进行。
③蒸馏之前,必须了解被蒸馏的物质及其杂质的沸点和饱和蒸气压,以决定何时(即在什么温度时)收集馏分。
④蒸馏烧瓶应当采用圆底烧瓶。沸点在40-150℃的液体可采用150℃以上的液体,或沸点虽在150℃以下,对热不稳常压的简单蒸馏。对于沸点在定、易热分解的液体,可以采用减压蒸馏和水蒸汽蒸馏。
(6)简易装置
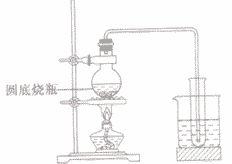
(7)应用
①水的净化
②石油的分馏
(8)蒸馏化学口诀
隔网加热冷管倾,上缘下缘两相平。
需加碎瓷防暴沸,热气冷水逆向行。
瓶中液限掌握好,先撤酒灯水再停。
指利用液体混合物中各组分挥发性的差异而将组分分离的传质过程。将液体沸腾产生的蒸气导入冷凝管,使之冷却凝结成液体的一种蒸发、冷凝的过程。
蒸馏是分离沸点相差较大的混合物的一种重要的操作技术,尤其是对于液体混合物的分离有重要的实用意义。
即,蒸馏条件:1.液体是混合物。2.各组分沸点不同。
实验室制蒸馏水:
(1)原理:蒸馏是利用互相溶解的液体混合物中各组分沸点小同进行分离提纯的操作。其过程是:加热样品使其中某组分汽化,然后使蒸气冷凝为液体加以收集。
(2)仪器:铁架台、蒸馏烧瓶、冷凝管、尾接管、锥形瓶、温度计、酒精灯、石棉网等。
(3)装置:

(4)操作:
①用洒精灯外焰给受热仪器先预热后加热
②对蒸馏烧瓶(烧杯、烧瓶、锥形瓶等仪器)加热时,不能直接加热,一定要垫石棉网,蒸馏烧瓶中液体体积为容器容积的1/3—2/3
③温度计不能直接插人蒸馏烧瓶的液体之中,应使温度计水银球与蒸馏烧瓶支管口位于同一水平线上
④蒸馏烧瓶的支管必须露出橡皮塞以防蒸馏出来的液体接触橡皮塞而带入杂质
⑤冷凝管中冷水的走向应是下口进、上口出,以使蒸汽充分冷却。
(5)关键:
①控制好加热温度。如果采用加热浴,加热浴的温度应当比蒸馏液体的沸点高出若干度,否则难以将被蒸馏物蒸馏出来。加热浴温度比蒸馏液体沸点高出的越多,蒸馏速度越快。但是,加热浴的温度也不能过高,否则会导致蒸馏瓶和冷凝器上部的蒸气压超过大气压,有可能产生事故,特别是在蒸馏低沸点物质时尤其需注意。一般地,加热浴的温度不能比蒸馏物质的沸点高出30℃。整个蒸馏过程要随时添加浴液,以保持浴液液面超过瓶中的液面至少一公分。
②蒸馏高沸点物质时,由于易被冷凝,往往蒸气未到达蒸馏烧瓶的侧管处即已经被冷凝而滴回蒸馏瓶中。因此,应选用短颈蒸馏瓶或者采取其它保温措施等,保证蒸馏顺利进行。
③蒸馏之前,必须了解被蒸馏的物质及其杂质的沸点和饱和蒸气压,以决定何时(即在什么温度时)收集馏分。
④蒸馏烧瓶应当采用圆底烧瓶。沸点在40-150℃的液体可采用150℃以上的液体,或沸点虽在150℃以下,对热不稳常压的简单蒸馏。对于沸点在定、易热分解的液体,可以采用减压蒸馏和水蒸汽蒸馏。
(6)简易装置

(7)应用
①水的净化
②石油的分馏
(8)蒸馏化学口诀
隔网加热冷管倾,上缘下缘两相平。
需加碎瓷防暴沸,热气冷水逆向行。
瓶中液限掌握好,先撤酒灯水再停。
水体污染的定义:
大量的污染物质排入水体,超过水体的自净能力使水质恶化,水体及其周围的生态平衡遭到破坏,对人类健康、生活和生产活动等造成损失和威胁的情况。
水体污染来源:
a.工业污染:座水、废渣、废气《工业“三反”》。
b.农业污染:化肥、农药的不合理使川。
c.生活污染:含磷洗涤剂的大量使用、生活污水的任意排放等。
防治措施:
a.工业上:通过应用新技术、新工艺减少污染物的产生,同时对污染的水体作处理使之符合排放标准。
b.农业上:提们使川农家肥,合理使用化肥和农药。
c.生活污水也应逐步实现欲中处理和排放。
水体的自净能力:
广义的水体自净是指在物理、化学和生物作用下.受污染的水体逐渐自然净化,水质复原的过程。,狭义的水体自净是指水体叶I微生物氧化分解有机污染物而使水体净化的过程。水体自净大致分为三类,即物理净化、化学净化和生物净化。它们同时发生,相互影响,共同作用。
(1)物理净化。物理净化是指污染物质由于稀释、扩散、混合和沉淀等过程而浓度降低。污水进入水体后,大颗粒的不溶性固体在水流较弱的地方逐渐沉入水底,形成污泥。悬浮体、胶体和可溶性污染物因混合、稀释,浓度逐渐降低。
(2)化学净化。化学净化是指污染物由于氧化还原、酸碱反应、分解、化合和吸附凝聚等化学或物理作用而浓度降低。流动的水体从水面上大气中溶人氧气,使污染物中铁、锰等重金属离子氧化,生成难溶性物质析出沉降。某些元素在一定酸性环境中,形成易溶性化合物,随水漂移而稀释;在中性或碱性条件下,某些元素形成难溶化合物而沉降。天然水中的胶体,吸附和凝聚水中悬浮物质微粒,随水流移动或逐渐沉降。
(3)生物净化,又称生物化学净化。是指生物活动尤其是微生物对有机物的氧化分解使污染物质的浓度降低。
城市污水及处理:
(1)城市污水城市污水包括生活污水、工业废水和径流污水等,由城市排水管网汇集并输送到污水处理厂进行处理。城市污水的污染,一般经历三个历史时期:病源污染期、总体污染期和新污染期。在病源污染期,城市污水主要是生活污水。由于污水中含有病菌和病毒,污水排入水体后往往会传染疾病。在总体污染期,随着工业的发展和人口的集中,城市污水量及所含的污染物种类不断增加。污水排入水体后,造成水体中悬浮物数量和生化需氧量越来越大,水体缺氧,水生生物灭绝。在新污染期,由于工业的高度发展,污水所含的污染物种类更加复杂。工业废水日益成为城市污水处理中的主要对象。
(2)城市污水处理城市污水处理分为三个级别.分别称为污水一级处理、污水二级处理、污水三级处理。一级处理应用物理处理方法,即用格栅、沉砂池、初沉池、活性污泥池、二次沉淀池等构筑物,去除污水中不溶解的污染物和寄生虫卵。二级处理应用生物处理方法,即主要通过微生物的代谢作用进行物质转化的过程,将污水巾各种复杂的有机物降解为简单的物质。生物处理对污水水质、水温、供氧量等都有一定的要求。三级处理是用生物化学(硝化一反硝化)法、碱化吹脱法或离子交换法除氮,用化学沉淀法除磷,用臭氧氧化法、活性炭法或超过滤法除去难降解有机物,用反渗透法除去盐类,用氯化法消毒等过程中的一种或几种组成的污水处理工艺。
大量的污染物质排入水体,超过水体的自净能力使水质恶化,水体及其周围的生态平衡遭到破坏,对人类健康、生活和生产活动等造成损失和威胁的情况。
水体污染来源:
a.工业污染:座水、废渣、废气《工业“三反”》。
b.农业污染:化肥、农药的不合理使川。
c.生活污染:含磷洗涤剂的大量使用、生活污水的任意排放等。
防治措施:
a.工业上:通过应用新技术、新工艺减少污染物的产生,同时对污染的水体作处理使之符合排放标准。
b.农业上:提们使川农家肥,合理使用化肥和农药。
c.生活污水也应逐步实现欲中处理和排放。
水体的自净能力:
广义的水体自净是指在物理、化学和生物作用下.受污染的水体逐渐自然净化,水质复原的过程。,狭义的水体自净是指水体叶I微生物氧化分解有机污染物而使水体净化的过程。水体自净大致分为三类,即物理净化、化学净化和生物净化。它们同时发生,相互影响,共同作用。
(1)物理净化。物理净化是指污染物质由于稀释、扩散、混合和沉淀等过程而浓度降低。污水进入水体后,大颗粒的不溶性固体在水流较弱的地方逐渐沉入水底,形成污泥。悬浮体、胶体和可溶性污染物因混合、稀释,浓度逐渐降低。
(2)化学净化。化学净化是指污染物由于氧化还原、酸碱反应、分解、化合和吸附凝聚等化学或物理作用而浓度降低。流动的水体从水面上大气中溶人氧气,使污染物中铁、锰等重金属离子氧化,生成难溶性物质析出沉降。某些元素在一定酸性环境中,形成易溶性化合物,随水漂移而稀释;在中性或碱性条件下,某些元素形成难溶化合物而沉降。天然水中的胶体,吸附和凝聚水中悬浮物质微粒,随水流移动或逐渐沉降。
(3)生物净化,又称生物化学净化。是指生物活动尤其是微生物对有机物的氧化分解使污染物质的浓度降低。
城市污水及处理:
(1)城市污水城市污水包括生活污水、工业废水和径流污水等,由城市排水管网汇集并输送到污水处理厂进行处理。城市污水的污染,一般经历三个历史时期:病源污染期、总体污染期和新污染期。在病源污染期,城市污水主要是生活污水。由于污水中含有病菌和病毒,污水排入水体后往往会传染疾病。在总体污染期,随着工业的发展和人口的集中,城市污水量及所含的污染物种类不断增加。污水排入水体后,造成水体中悬浮物数量和生化需氧量越来越大,水体缺氧,水生生物灭绝。在新污染期,由于工业的高度发展,污水所含的污染物种类更加复杂。工业废水日益成为城市污水处理中的主要对象。
(2)城市污水处理城市污水处理分为三个级别.分别称为污水一级处理、污水二级处理、污水三级处理。一级处理应用物理处理方法,即用格栅、沉砂池、初沉池、活性污泥池、二次沉淀池等构筑物,去除污水中不溶解的污染物和寄生虫卵。二级处理应用生物处理方法,即主要通过微生物的代谢作用进行物质转化的过程,将污水巾各种复杂的有机物降解为简单的物质。生物处理对污水水质、水温、供氧量等都有一定的要求。三级处理是用生物化学(硝化一反硝化)法、碱化吹脱法或离子交换法除氮,用化学沉淀法除磷,用臭氧氧化法、活性炭法或超过滤法除去难降解有机物,用反渗透法除去盐类,用氯化法消毒等过程中的一种或几种组成的污水处理工艺。
定义:
硬水是含有较多可溶性钙、镁化合物的水。
软水是不含或含较少可溶性钙、镁化合物的水。
水的硬度:
水的硬度常用一种规定的标准来衡量,这个标准是:把1L水里含10mgCaO(或相当于10mgCaO)称为1度。
硬水和软水的检验:
(1)用肥皂水来检验硬水和软水,把肥皂水滴在水里搅拌,产生泡沫多的是软水,产生泡沫少或不产生泡沫的是硬水
(2)用加热煮沸的方法检验硬水和软水。水加热煮沸时,有较多沉淀的是硬水,不产生沉淀或者产生沉淀较少的是软水。
硬水的软化:
就是设法除去硬水中的钙、镁化合物。
硬水软化的方法:生活中常用煮沸法,工业上常用离子交换法和药剂软化法,实验室常用蒸馏法,蒸馏法是净化程度较高的水,蒸馏时应注意以下几点:
①蒸馏瓶中的液体不能超过其容积的2/3.
②加热时,应在烧瓶中放几粒沸石(或碎瓷片)。
③装置气密性良好
④水银温度计的水银球应放在蒸馏烧瓶的支管口附近。
使用硬水造成的危害:
饮用水中含有微量的钙、镁成分,对人体健康是有益的。但是,水中含太多的钙、镁成分,对生活和生产都有危害。
①用硬水洗涤,不仅浪费肥皂,而且会在织物上积有肥皂跟钙、镁反应后生成的沉淀,不容易洗干净,还会使纤维变脆、易断。
②硬水有苦涩味,长期饮用硬水会使人的胃肠功能紊乱,出现不同程度的腹胀、腹泻和腹痛。
③锅炉用水硬度太大,会产生水垢,这会大大降低锅炉的导热能力,造成燃料的浪费。另外,当水垢爆裂脱落时,会造成炉壁局部受热不均,易引起锅炉爆炸。
离子交换法:
离子交换法是工业生产软化水的重要方法之一。离子交换法的原理:离子交换树脂是一种聚合物,带有相应的功能基团(一般情况下,常规的钠离子交换树脂带有大量的钠离子),当含钙、镁离子较高的硬水经过离子交换树脂时,离子交换树脂即可以释放出钠离子,其功能基团与钙、镁离子结合。这样水中的钙、镁离子含量下降,水的硬度降低,硬水即可被软化为软水。离子交换法的流程为:工作(即交换)、反洗、再生、清洗四个过程。
硬水是含有较多可溶性钙、镁化合物的水。
软水是不含或含较少可溶性钙、镁化合物的水。
水的硬度:
水的硬度常用一种规定的标准来衡量,这个标准是:把1L水里含10mgCaO(或相当于10mgCaO)称为1度。
硬水和软水的检验:
(1)用肥皂水来检验硬水和软水,把肥皂水滴在水里搅拌,产生泡沫多的是软水,产生泡沫少或不产生泡沫的是硬水
(2)用加热煮沸的方法检验硬水和软水。水加热煮沸时,有较多沉淀的是硬水,不产生沉淀或者产生沉淀较少的是软水。
硬水的软化:
就是设法除去硬水中的钙、镁化合物。
硬水软化的方法:生活中常用煮沸法,工业上常用离子交换法和药剂软化法,实验室常用蒸馏法,蒸馏法是净化程度较高的水,蒸馏时应注意以下几点:
①蒸馏瓶中的液体不能超过其容积的2/3.
②加热时,应在烧瓶中放几粒沸石(或碎瓷片)。
③装置气密性良好
④水银温度计的水银球应放在蒸馏烧瓶的支管口附近。
使用硬水造成的危害:
饮用水中含有微量的钙、镁成分,对人体健康是有益的。但是,水中含太多的钙、镁成分,对生活和生产都有危害。
①用硬水洗涤,不仅浪费肥皂,而且会在织物上积有肥皂跟钙、镁反应后生成的沉淀,不容易洗干净,还会使纤维变脆、易断。
②硬水有苦涩味,长期饮用硬水会使人的胃肠功能紊乱,出现不同程度的腹胀、腹泻和腹痛。
③锅炉用水硬度太大,会产生水垢,这会大大降低锅炉的导热能力,造成燃料的浪费。另外,当水垢爆裂脱落时,会造成炉壁局部受热不均,易引起锅炉爆炸。
离子交换法:
离子交换法是工业生产软化水的重要方法之一。离子交换法的原理:离子交换树脂是一种聚合物,带有相应的功能基团(一般情况下,常规的钠离子交换树脂带有大量的钠离子),当含钙、镁离子较高的硬水经过离子交换树脂时,离子交换树脂即可以释放出钠离子,其功能基团与钙、镁离子结合。这样水中的钙、镁离子含量下降,水的硬度降低,硬水即可被软化为软水。离子交换法的流程为:工作(即交换)、反洗、再生、清洗四个过程。
定义:
清除水中不好的或不需要的杂质,使水达到纯净的程度。
四种净化水的方法,原理,作用:
| 净化水的方法 | 原理 | 作用 |
| 沉淀 | 食难溶性的杂质沉淀下来,并与水分层 | 使难溶性大颗粒沉降或加入明矾,形成的胶状物吸附杂质沉降 |
| 过滤 | 把液体与难溶于液体的固体物质分离 | 除去难溶性杂质 |
| 吸附 | 利用物质的吸附作用,吸附水中一些难溶性杂质,臭味和色素 | 除去难溶性杂质,部分可溶性杂质,臭味和色素 |
| 蒸馏 | 通过加热的方法使水变成水蒸气后冷凝成水 | 除去可溶性杂质,使硬水软化 |
水净化的方法:
吸附,沉淀,过滤,蒸馏,杀菌
吸附:常用明矾和活性炭,明矾溶于水后形成胶状物吸附水中的悬浮物,
活性炭不仅可以吸附水中的悬浮物,还可以吸附在水中有异味的物质和色素
沉淀:水中悬浮物别吸附后形成密度大的颗粒,从而使杂质沉淀
过滤:除去水中不溶性的杂质
蒸馏:除去可溶性杂质的方法
杀菌:常用杀毒剂:漂白粉,氯气以及新型消毒剂二氧化氯等
吸附、沉淀、过滤和蒸馏中单一操作净化程度较高的是蒸馏。综合运用时,按吸附→沉淀→过滤→蒸馏的顺序操作净化效果更好
加絮凝剂(明矾)与活性炭净水的比较:
| 净化水的方法 | 原理 | 能除去的杂质 |
| 明矾净水 | 明研溶于水后形成胶状物质,对杂质进行吸附,将微小颗粒吸附在一起形成大的固体颗粒而沉阵下来 | 不溶于水的微小固体颗粒 |
| 活性炭净水 | 利用内部疏松多孔的结构来吸附水中的微小颗粒和一些可溶于水的杂质 | 不溶于水的微小固体颗粒和部分能溶于水的杂质以及气味,颜色等 |
自来水厂净化水的过程图及步骤
1、净化过程图
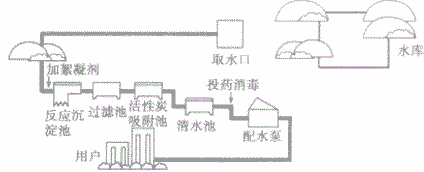
2、自来水净化步骤
①从水库中取水。
②加絮凝剂(主要是明矾),使悬浮的小颗粒状杂质被吸附凝聚。
③在反应沉淀池中沉降分离,使水澄清
④将沉淀池中流出的较澄清的水通入过滤池中,进一步除去不溶性杂质。
⑤再将水引人活性炭吸附池中,除去水中的臭味和残留的颗粒较小的不溶性杂质。
⑥细菌消毒(常用通入氯气的办法)。它是一个化学变化过程,因为除去病菌的过程.就是把病菌变成其他物质的过程。
⑦杀菌后的水就是洁净、可以饮用的自来水,通过配水泵供给用户,但水中仍然含有可以溶于水的一些杂质,所以还是混合物。
混合物:
(1)概念:由两种或多种物质混合而成的物质,没有有固定的组成,各成分保持自己原有的化学性质。
(3)常见的混合物:空气、合金、矿石、溶液等。
(4)混合物的提纯:混合物经过物理或化学的方法可以提纯。
纯净物:
(1)概念:只由一种物质组成的物质。
(3)纯净物的分类:纯净物根据物质组成的元素种类,分为两大类:单质和化合物。
纯净物和氧化物的区别:
| 纯净物 | 混合物 | |
| 概念 | 宏观:由一种物质组成的物质 微观:由同种分子构成(对于由分子构成的物质而言) |
宏观:由两种或多种物质组成的物质 微观:由不同种分子构成(对于由分子构成的物质而言) |
| 区别 | 由同种物质组成(对于由分子构成的物质,是由同种分子构成的),组成是固定的 | 由不同种物质组成(对于由分子构成的物质. 是由不同种分子构成的),组成是不固定的 |
| 特点 | ①具有固定的组成 ②具有一定的性质 ③有专门的化学符号 |
①没有固定的组成和性质 ②各成分保持各自的性质 ③没有专门的化学符号 |
| 分离方法 | 组成固定,不需分离;若需将化合物分成几种单质,则必须通过化学方法才能实现 | 物理方法: 筛选 过滤 蒸馏 |
| 实例 | 氧气,二氧化碳,高锰酸钾 | 空气,粗盐,蔗糖水 |
| 联系 | 纯净物是相对而言的,自然界中绝对纯净的物质是不存在的,通常的纯净物是指含杂质很少的具有高纯度的物质。两者间的关系为 | |
对纯净物和混合物概念的理解:
(1)混合物概念:混合物可以看作是由几种纯净物混合而成的,混合物的形成过程中发生的是物理变化。由于混合物的组成一般不固定,所以往往不能用化学式表示。
(2)纯净物概念:纯净物只由一种物质组成,有固定的组成.可以用化学式表示。
常考的纯净物与混合物:
(1)混合物:石油、煤、天然气、洁净的空气、生理盐水、矿泉水、汽水、碘酒、白酒、双氧水、盐酸、合金等都是混合物。
(2)纯净物:水银、烧碱、纯碱、胆矾、液态氧、液态氮、蒸馏水(纯水)、干冰、冰水共存物、金刚石、石墨、生石灰、熟石灰、氯化钠、氧化铁等都是纯净物:
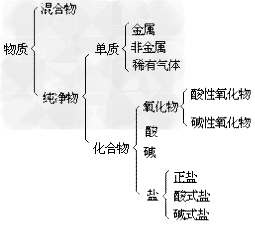
物质的分类示意图:
发现相似题
与““保护母亲河英溪”这是在英都到仑苍路上的一条广告语,说明现...”考查相似的试题有:
- 下列混合物中可用过滤法分离的是:( )A.面粉和食盐B.食盐和蔗糖C.酒精和水D.白醋和水
- 酥油茶是极具民族特色的一种饮品,也是藏族人民待客的最佳饮料.制普通酥油茶的简单过程是:将茶叶熬成红汤,滤出茶渣,将热...
- 在南京的普通百姓中,低碳生活已经成为人们所追求的目标.“低碳生活”简言之就是减低二氧化碳的排放,就是低能量、低消耗、低...
- 2010年“中国水周”的主题是:“严格水资源管理,保障可持续发展”。水与人类的生活和生产密切相关。请回答以下相关问题:(一)...
- 学习的目的是在于应用。请根据你所掌握的化学知识,解释或解决以下生活中的一些常见问题。(1)要区分硬水与软水,可以使用的...
- 下列物质中既存在离子又存在分子的是( )A.氯化钠晶体B.金刚石C.液氧D.氯化钠溶液
- 下列物质中属于酸的是 A.H2CO3B.NaHCO3C.P2O5D.Ba(OH)2
- 下列各组物质中,分类正确的是A.常见的混合物:空气、酒精 、食盐 B. 常见的合成材料:塑料、合成纤维、合成橡胶C常见的营养...
- 下列是我们日常生活中接触到的物质,属于纯净物的是( )A.可乐饮料B.洁净的空气C.潺潺的溪水D.蒸馏水
- 下列物质中属于纯净物的是[ ]A.食盐水B.冰水C.汽水D.自来水