本试题 “用NaCl固体配制溶质的质量分数为10%的溶液,下列情况会造成溶质质量数偏大的是______A.将用于搅拌的玻璃棒用蒸馏水冲洗,洗涤液并于溶液中 B.量取水的体积...” 主要考查您对溶液的配制
元素符号的意义及写法
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶液的配制
- 元素符号的意义及写法
知识梳理:
1 、固体 + 水
①实验步骤:计算—称量—量取—溶解
②实验器材:托盘天平 + 药匙(或镊子) ;合适的量筒 + 胶头滴管;烧杯 + 玻璃棒
③注意事项:计算、称量和量取都要准确,溶解时固体要溶解完全
2 、液体 + 水
①实验步骤:计算—量取—溶解
②实验器材:合适的量筒 + 胶头滴管;烧杯 + 玻璃棒
③注意事项:计算、量取都要准确,同时需要两种不同规格的量筒
配制溶液的步骤:
(1)用溶质和水配制一定溶质质量分数的溶液
①实验用品:托盘天平、烧杯、量筒、胶头滴管、玻璃棒、药匙等。
②实验步骤:
计算→称量药品→量取水→搅拌溶解
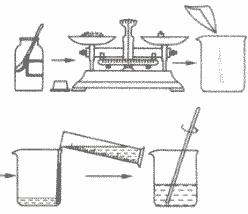
a.计算所需溶质和水的质量;
b.用托盘天平称量所需溶质,倒入烧杯中;
c.把水的密度近似看作1g/cm3,用量筒量取一定体积的水,倒入盛有溶质的烧杯里,用玻璃棒搅拌,使溶质溶解;
d.把配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签(标签中应包括药品的名称和溶液中溶质的质量分数),放到试剂柜中。
③导致溶液质量分数变化的因素
a.称量时物质和砝码的位置放错,如止确称量5.8gNaCl,应在右盘放置5g砝码,再用0.8g游码,若放错位置,将砝码放在天平的左盘,则实际称量NaCl的质量为5g-0.8g=4.2g,这样会导致配制的溶液溶质质量分数变小;
b.量筒量取水的体积时读取示数错误,读取示数时仰视读数所量取水的实际体积大于理论值,将会使配制的溶液溶质质量分数变小;读取示数时俯视读数所量取水的实际体积小于理论值,将会使配制的溶液溶质质量分数变大;
c.将量筒中的水倒入烧杯时洒落到外面或未倒净,将导致溶液溶质质最分数偏大;
d.所用固体不纯,将会导致溶液溶质质量分数偏小;
e.计算错误可能会导致溶液溶质质量分数偏大或偏小。
配制溶液时导致溶质质量分数变化的原因:
在配制一定质量和一定质量分数的溶液过程中,经常会出现所得溶液溶质质量分数偏大或偏小的情况。
1. 所配溶液溶质质量分数偏小的原因:
①从计算错误角度考虑:水的质量算多了,溶质的质量算少了;
②从用托盘大平称量的角度考虑:天平读数有问题。药品和砝码放颠倒了,左盘放纸片但右盘没有放纸片,调零时,游码未拨回“0”刻度等;
③从用量筒量取液体的角度考虑:量取溶剂时,仰视读数了;
④从转移药品角度考虑:烧杯不干燥或烧杯内有水,量筒中的液体溶质未全部倒人烧杯中;
⑤从药品的纯度角度考虑:溶质中含有杂质
2. 所配溶液溶质质量分数偏大的原因
①称量时,所用砝码已生锈或沾有油污;②量取溶剂时,俯视读数了。
综合配制溶液的计算利用:
所提供的信息可选取多种方案配制所需的溶液。如现有KCl固体、蒸馏水、5%的KCl溶液、15%的KCl溶液,配制100g10%的KCl溶液,其方案有:
| 所需药品 | 主要步骤 | |
| 一 | 10gKCl+90g蒸馏水 | 用天平称量10gKCl,用量筒量取90ml水,分别倒入烧杯,用玻璃棒搅拌至KCl固体全部消失 |
| 二 | 66.7g15%的KCl溶液33.3g蒸馏水 | 用量筒量取33.3mL水,用天平称66.7g15%的KCl溶液,混合均匀即可 |
| 三 | 5.3gKCl+94.7g 5%的KCl溶液 | 用天平称量5.3gKCl固体和94.7g 5%的KCl溶液,将5.3gKCl倒入94.7g5%的KCl溶液中,用玻璃棒搅拌至KCl固体全部消失 |
| 四 | 50g5%KCl溶液+50g15%KCl 溶液 | 用天平称量5%、15%的KCl溶液各50g,混合均匀即可 |
表示方法:
为了书写和学术交流的方便,采用国际统一的符号来表示各种元素,如:氢元素用“H”来表示,铁元素用“Fe”来表示等。
元素符号的写法:
①由一个字母表示的元素符号要大写,如:H、C、 S、P,K。
②由两个字母表示的元素符号,第一个字母要大写,第二个字母要小写(即“一大二小”)。如:Na、Mg、 Ca、Zn、Si。
为了书写和学术交流的方便,采用国际统一的符号来表示各种元素,如:氢元素用“H”来表示,铁元素用“Fe”来表示等。
元素符号的写法:
①由一个字母表示的元素符号要大写,如:H、C、 S、P,K。
②由两个字母表示的元素符号,第一个字母要大写,第二个字母要小写(即“一大二小”)。如:Na、Mg、 Ca、Zn、Si。
元素符号和化学式的关系:
| 化学用语 | 元素符号 | 化学式 | |
| 意义 | 宏观 | 表示一种元素 表示一种物质(由原子构成的物质) |
表示这种物质 表示这种物质由几种元素组成 |
| 微观 | 表示该元素的一个原子 | 表示这种物质的一个分子〔由分子构成的物质) 表示一个分子含有各原子的个数(由分子构成的物质) | |
| 量的意义 | —— | 表示这种物质的相对分子质量 表示这种物质中各元素的原子个数比和质量之比 表示物质中各组成元素的质量分数 | |
| 举例 | H 表示氢元素 表示一个氢原子 |
H2O 表示水 表示水是由氢元素和氧元素组成的 表示1个水分子 表示1个水分子中含有2个氢原子和1个氧原子 | |
| 注意事项 | 单独的化学式和元素符号,既有宏观意义,又有微观意义化学式和元素符号前加上数字,则只表示微观意义,即只表示相应的粒子个数,如“2H”表示两个氢原子,"3H2O"表示三个水分子化学式中元素符号右下角的数字表示每个分子中所含该元素原子的个数,如“CO2”中的”2”表示一个二氧化碳分子中含有两个氧原子 | ||
发现相似题
与“用NaCl固体配制溶质的质量分数为10%的溶液,下列情况会造成溶...”考查相似的试题有:
- 下列物质放入足量水中,能形成溶液的是A.牛奶B.植物油C.食盐D.面粉
- 实验室要配制60g 10%的NaOH溶液,现提供30g 20%的NaOH溶液、40g 5%的NaOH溶液以及足够的NaOH固体和水,请选用上述的药品,设...
- 用固体氯化钠配制溶质质量分数一定的氯化钠溶液,必不可少的一组仪器是A.托盘天平、烧杯、药匙、玻璃棒、量筒B.量筒、玻璃...
- 稀释浓溶液时使用的仪器中通常不包括( )A.酒精灯B.量筒C.烧杯D.玻璃棒
- 化学实验室取用16 g硫酸铜粉末,可配制8%的硫酸铜溶液___________g;若用20%的硫酸铜溶液100 g加水稀释,可得8%的硫酸铜溶液_...
- 现有下列仪器:①试管;②酒精灯;③量筒;④烧杯;⑤滴管;⑥约匙;⑦托盘天平;⑧玻璃棒等.实验室用食盐和水配制50g 10%的氯化钠溶...
- 以下是省水环境监测中心2006年4月发布的全省地表水资源质量状况中的一部分编号河段水质类别主要污染指标质量状况A长江芜湖戈...
- 请用元素或化学式表示:(1)2个氮原子_____________;(2)3个氧分子_____________;(3)五氧化二磷_____________;(4)天然气或沼...
- 请用正确的化学用语填空:
- 用元素符号或化学式填空:钾______;氦______;氯化钙______;氢氧化镁______;碳酸钠______.