本试题 “张明同学在学习“硫酸及其盐的某些性质与用途“中,进行如下实验探究.[实验一]探究浓硫酸的氧化性将实验室常用的药品放入如图所示的实验装置后,加热装置甲....” 主要考查您对(浓)硫酸
硫酸盐
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- (浓)硫酸
- 硫酸盐
硫酸:
硫酸的分子式:H2SO4;结构式: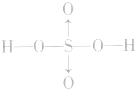 ,H2SO4中硫元素为+6价,处于最 0 高价,具有氧化性,但只有浓H2SO4表现出强氧化性,而稀硫酸、硫酸盐巾的硫元素通常不表现氧化性。
,H2SO4中硫元素为+6价,处于最 0 高价,具有氧化性,但只有浓H2SO4表现出强氧化性,而稀硫酸、硫酸盐巾的硫元素通常不表现氧化性。
硫酸的物理性质和化学性质:
1.硫酸的物理性质
纯硫酸是无色、黏稠的油状液体,密度大,沸点高,是一种难挥发的强酸,易溶于水,能以任意比与水互溶.浓硫酸溶于水时放出大量的热。常见浓硫酸的质量分数为98.3%,其密度为 1.84g·cm-3,沸点为338℃,物质的量浓度为18.4mol·L-1.H2SO4的浓度越大,密度越大,若将30%的H2SO4溶液与10%的H2SO4溶液等体积混合,所得溶液的质量分数大于20%。
2.稀硫酸的化学性质
稀硫酸具有酸的通性。
(1)与指示剂作用:能使紫色石蕊试液变红。
(2)与碱发生中和反应
(3)与碱性氧化物或碱性气体反应 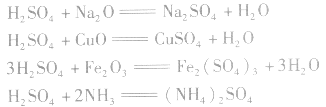
(4)与活泼金属发生置换反应 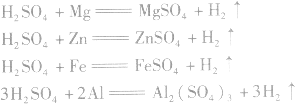
(5)与某些盐溶液反应 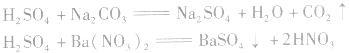
4.浓硫酸的特性
(1)吸水性将一瓶浓硫酸敞口放置在空气中,其质量将增加,密度将减小,浓度降低,体积变大。这是因为浓硫酸具有吸水性,实验室里常利用浓硫酸作干燥剂。
浓硫酸不仅可以吸收空气中的水,还可吸收混在气体中的水蒸气、混在固体中的湿存水、结晶水合物中的部分结晶水。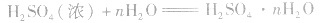 。
。
浓H2SO4中的H2SO4分子可强烈地吸收游离的水分子形成一系列的硫酸水合物: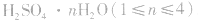 。这些水合物很稳定,所以浓H2SO4可作某些不与其反应的气体、固体的干燥剂,同时不能暴露在空气中。能够用浓H2SO4干燥的气体有
。这些水合物很稳定,所以浓H2SO4可作某些不与其反应的气体、固体的干燥剂,同时不能暴露在空气中。能够用浓H2SO4干燥的气体有 、
、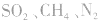 等酸性或中性气体,而具有还原性的气体
等酸性或中性气体,而具有还原性的气体 和碱性气体NH3则不能用浓H2SO4干燥。另外在酯化反应中,如
和碱性气体NH3则不能用浓H2SO4干燥。另外在酯化反应中,如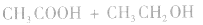
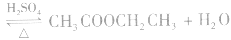 中,浓H2SO4作催化剂和吸水剂。
中,浓H2SO4作催化剂和吸水剂。
(2)脱水性指浓H2SO4将有机物里的氧、氧元素按原子个数比2:1脱去生成水的性质。浓H2SO4从有机物中脱下来的是氢、氧元素的原子,不是水,脱下来的氢、氧元素的原子按2:1的比例结合成H2O;对于分子中所含氢、氧原子个数比为2:l的有机物(如蔗糖、纤维素等),浓H2SO4可使其炭化变黑,如: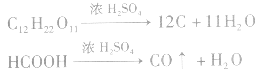
(3)强氧化性常温下,Fe、Al遇浓H2SO4会发生钝化。但热的浓 H2SO4能氧化大多数金属(除金、铂外)、某些非金属单质及一些还原性化合物。如: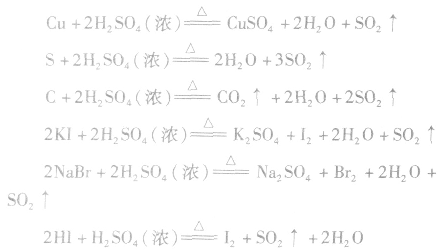
在这些氧化还原反应中,浓硫酸的还原产物一般为SO2。
浓、稀硫酸的比较与鉴别:
1.比较
稀硫酸—弱氧化性—可与活泼金属反应,生成H2—氧化性由H+体现。
浓硫酸——强氧化性——加热时可与绝大多数金属和某些非金属反应,通常生成SO2——氧化性由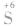 体现。
体现。
2.鉴别
从浓H2SO4和稀H2SO4性质的差异人手,可知鉴别浓H2SO4和稀H2SO4的方法有多种。
方法一:取少量蒸馏水,向其中加入少量试样硫酸,如能放出大量热则为浓H2SO4,反之则为稀H2SO4。
方法二:观察状态,浓H2SO4呈黏稠状,而稀H2SO4为黏稠度较小的溶液。
方法三:用手掂掂分量,因为浓H2SO4的密度较大 (1.84g·cm-3,相同体积的浓H2SO4和稀H2SO4,浓H2SO4的质量比稀H2SO4大很多。
方法四:取少量试样,向其中投入铁片,若产生气体,则为稀H2SO4, ;若无明显现象(钝化),则为浓H2SO4。
;若无明显现象(钝化),则为浓H2SO4。
方法五:用玻璃棒蘸取试样在纸上写字,立即变黑 (浓H2SO4的脱水性)者为浓H2SO4,另一种为稀H2SO4。
方法六:取少量试样,分别投入一小块铜片,稍加热发生反应的(有气泡产生)为浓H2SO4。(浓H2SO4的强氧化性),无现象的是稀H2SO4.
硫酸的用途及使用:
(1)用途硫酸是化学工业最黄要的产品之一,它的用途极广(如下图)。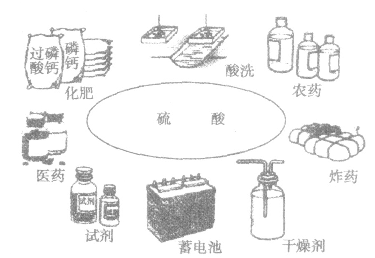
①利用其酸性可制磷肥、氮肥,可除锈,可制实用价值较高的硫酸盐等。
②利用其吸水性,在实验室浓H2SO4常用作干燥剂。
③利用其脱水性,浓H2SO4常作精炼石油的脱水剂、有机反应的脱水剂等。
④利用浓H2SO4的高沸点和难挥发性,常用于制取各种挥发性酸。
⑤浓H2SO4常作有机反应的催化剂。
(2)浓硫酸的安全使用
①浓H2SO4的稀释稀释浓硫酸时应特别注意:将浓硫酸沿器壁慢慢地注入水中,并不断搅拌,使产生的热量迅速地扩散出去。切不可把水倒人浓硫酸里。两种液体混合时,要把密度大的加到密度小的液体中,如浓H2SO4、浓HNO3-混合酸的配制方法是把浓H2SO4沿器壁慢慢地注入浓HNO3中。
②万一不小心将浓硫酸溅到皮肤上、衣服上或桌面上,应分别怎样处理?
皮肤上:用干布迅速拭去,再用大量水冲洗,最后涂上3%~5%的碳酸氢钠溶液。
衣服上:用大量水冲洗。
桌面上:大量时,用适量。NaHCO3,溶液冲洗,后用水冲洗,再用抹布擦干;少量时用抹布擦即可。
几种重要的硫酸盐:

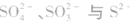 的检验:
的检验:
1.SO42-的检验
(1)原理:利用 ,
,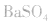 具有不溶于盐酸、硝酸的特性。
具有不溶于盐酸、硝酸的特性。
(2)试剂:可溶性钡盐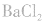 溶液或
溶液或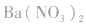 溶液,盐酸和稀硝酸。
溶液,盐酸和稀硝酸。
(3)易出现的错误:
①只加可溶性钡盐,不酸化。误将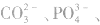 、
、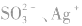 等判成SO42-,此时上述离子会分别产生
等判成SO42-,此时上述离子会分别产生 等白色沉淀.
等白色沉淀.
②先加可溶性盐,后酸化。误将 等判成SO42-,如向待测液中先滴加
等判成SO42-,如向待测液中先滴加 溶液,再加盐酸有白色沉淀生成便断定含SO42-。其错误之处是未注意溶液中不含SO42-而含Ag+或
溶液,再加盐酸有白色沉淀生成便断定含SO42-。其错误之处是未注意溶液中不含SO42-而含Ag+或 也会有同样现象,因为
也会有同样现象,因为
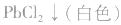
③试剂选择错误。误将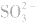 判成
判成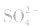 ,如向待测液中滴加盐酸酸化的
,如向待测液中滴加盐酸酸化的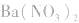 溶液,或滴加硝酸酸化的
溶液,或滴加硝酸酸化的 溶液,生成白色沉淀,使误以为有
溶液,生成白色沉淀,使误以为有 ,错在未注意
,错在未注意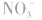 在酸性条件下具有强氧化性,可将
在酸性条件下具有强氧化性,可将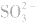 氧化成
氧化成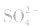 。
。
(4)检验的关键:既要注意试刹的选择,义耍注意操作顺序的优化,全面考虑,综合分析,正确推导,方能排除干扰离子。
(5)最佳检验方法:
2.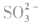 的检验常用气体法:
的检验常用气体法: (不能用硝酸等强氧化性酸),生成能使品红溶液褪色的无色有刺激性气味的气体。
(不能用硝酸等强氧化性酸),生成能使品红溶液褪色的无色有刺激性气味的气体。
3. 的检验
的检验
(1)气体法: ,所用酸必须是非强氧化性酸,可用稀盐酸或稀硫酸,生成能使湿润的醋酸铅试纸变黑的气体。
,所用酸必须是非强氧化性酸,可用稀盐酸或稀硫酸,生成能使湿润的醋酸铅试纸变黑的气体。
(2)沉淀法: ,生成黑色沉淀;或
,生成黑色沉淀;或 ,生成乳白色或黄色沉淀(溶液中)。
,生成乳白色或黄色沉淀(溶液中)。
亚硫酸及亚硫酸盐:
1.亚硫酸溶液中的微粒
SO2与水反应生成亚硫酸,亚硫酸不稳定,易分储成SO2和H2O,因此SO2与H2O的反应是一个可逆反应,用“ ”表示。
”表示。 
在亚硫酸溶液中存在的微粒有(三分子、四离子):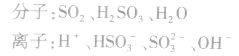
2.亚硫酸的性质
(1)亚硫酸的热稳定性
H2SO3极其不稳定,只能存在于稀的水溶液中。 H2SO3易分解生成SO2和H2O。 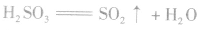
(2)亚硫酸的氧化性和还原性
H2SO3遇到比它更强的氧化剂时,表现还原性。如:
H2SO3遇到比它更强的还原剂时,表现氧化性。如:
(3)亚硫酸的酸性
H2SO3是中强酸,在水溶液中分两步电离: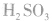
 。
。
由亚硫酸的组成和电离可知,亚硫酸对应的盐有正盐和酸式盐两种,如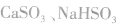 。
。
3.亚硫酸盐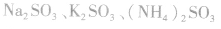 等亚硫酸盐易溶于水、易电离。
等亚硫酸盐易溶于水、易电离。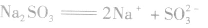

与“张明同学在学习“硫酸及其盐的某些性质与用途“中,进行如下实...”考查相似的试题有:
- 6.4g铜与100mL98%的浓H2SO4溶液(密度为ρg•cm-3)共热,铜没有剩余,求:(1)浓H2SO4的物质的量浓度是多少mol•L-1?(2)产...
- 常温下金属Al、Fe遇下列物质钝化的是( )A.盐酸B.稀硝酸C.稀硫酸D.浓硫酸
- 实验证明铜在低温下不能和O2发生反应,也不能和稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来...
- 如图.在一支试管中放入一小块铜片,再加入少量浓硫酸,然后把试管固定在铁架台上.把一小条蘸有品红溶液的滤纸放入带有单孔...
- 酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是( )。A.酯化反应的产物只有酯B.酯化反应可看成取代反...
- 某化学兴趣小组在学习“硫酸及其盐的某些性质和用途”中,进行了如下实验探究:【实验一】探究浓硫酸的氧化性(1)写出烧瓶中反应...
- 某化学课外兴趣小组探究铜与浓硫酸的反应情况.甲.乙.丙三位同学进行了下列实验:取12.8g铜片和20ml.18mol/L的浓硫酸放在...
- 已知二氧化硫可使高锰酸钾溶液褪色,反应的化学方程式为:5SO2+2KMnO4+2H2O═K2SO4+2MnSO4+2H2SO4用如图装置来验证浓硫酸与木...
- 下列画有横线的物质,在反应中不能被完全消耗的是( )①将含有少量H2O(g)的H2通过盛有足量Na2O2的容器中并不断用电火花点燃...
- (1)下列事实反映了硫酸的什么性质:①实验室制取氢气______;②干燥氢气______;③浓硫酸溶解金属铜______;④浓硫酸可用钢瓶贮...