本试题 “下列化学用语的使用及说法中正确的是[ ]A.K+与Ar的结构示意图相同B.Na2O的电子式是:C.通常状况下,1.5 mol氧气与0.5 mol氮气的混合气体的体积为44.8 LD....” 主要考查您对气体摩尔体积
原子结构示意图
离子结构示意图
电子式的书写
结构简式
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 气体摩尔体积
- 原子结构示意图
- 离子结构示意图
- 电子式的书写
- 结构简式
气体摩尔体积:
单位物质的量的气体所占的体积。
符号:Vm
单位:L/mol(L·mol-1)、m/mol(m·mol-1)
计算公式: 气体摩尔体积(Vm)=气体体积(V)/物质的量(n)
标况下(0℃ 101kPa)气体摩尔体积约为22.4L/mol,在25℃和101kPa条件下,气体摩尔体积约为24.5L/mol。
气体摩尔体积的使用方法:
- 在非标准状况下,不能用气体摩尔体积22.4mol/L进行计算。
- 标准状况下,非气体(即固、液体)不能用气体摩尔体积22.4mol/L进行计算。
- 气体可以是纯净气体,也可以是混合气体。
决定物质体积大小的因素:
- 粒子数目的多少
- 粒子本身的大小
- 粒子之间的平均距离
决定固体、液体物质的体积大小的因素主要是粒子数目的多少和粒子本身的大小;而气体的体积大小的决定因素是粒子数目的多少和分子间的平均距离。
标准状况下,气体摩尔体积的5个“关键”:
- 关键字——气体:研究对象是气体,非气体不研究摩尔体积。
- 关键字——任何:任何气体,只要是气体,不管纯净物还是混合物,只要状态相同,物质的量相同,体积就相同。
- 关键字——标况:标况下气体摩尔体积一定是Vm=22.4L/mol,非标准状况下的气体不一定等于22.4L/mol。
- 关键字——约为:22.4只是个约数,不是准确值,因为对于气体,忽略了粒子的大小对体积的影响,所以在相同的条件下。气体的摩尔体积近似相等。
- 关键字——1mol:气体在标况下的体积约为22.4L所对应的物质的量为1mol。
标准状况:
在0℃和101kPa的条件下,1mol任何气体的体积都约为22.4L。温度为0℃、压强为101kPa时的状况,我们通常称为“标准状况”。
在标准状况下,气体的摩尔体积约为22.4L/mol。
问题探究:
标准状况下,1mol气体的体积是22.4L,如果当1mol气体的体积是22.4L时,一定是标准状况吗?
答:不一定,因为影响气体体积的因素是温度、压强两个条件,非标准状况下1mol气体的体积也可能是22.4L。
定义:
圆圈和圆圈内的数字分别表示原子核和核内的质子数,弧线表示电子层,弧线上的数字表示该层的电子数。
表示原子结构的常用图示:
1.原子符号:
2.核外电子分层排布示意图:
3.原子结构示意图:
相对原子质量及近似相对原子质量:
1.几个概念的辨析
| 原子的真实质量 | 原子的真实质量也称绝对质量,是通过精密的实验测得的,原子的真实质量很小,使用极不方便,所以科学上,一般不直接使用原子的真实质量,而使用原子的相对质量—— 相对原子质量 |
| 核素的相对原子质量 | 核素的相对原子质量是指一个核素原子的质量与一个碳-12原子质量的l/12的比值 |
| 元素的相对原子质量 | 元素的相对原子质量是指某元素各种核素的相对原子质量与各核素原子所占的原子个数百分比(丰度)的乘积之和,也就是元素周期表中所给的相对原子质量的数值。一般情况下元素的相对原子质量不为整数 |
| 原子的质量数 | 原子的质量数是指某元素的一种核素原子的核中所含质子数和中子数之和,在实际使用中常代替相对原子质量,所以也叫做近似相对原子质量。需要注意的是元素无质量数 |
2.近似相对原子质量
1.核素的近似相对原子质量,就是核素的质量数。
2.元素的近似相对原子质量,就是按照该元素各种核素的质量数和各种核素原子所占的原子个数百分比算出的平均值。例如,氯元素的近似相对原子质量为:
正离子的离子结构示意图中核内质子数大于核外电子数;
负离子的离子结构示意图中核内质子数小于核外电子数。
原子是否满足最外层8电子结构的判断方法:
1.离子化合物
(1)阳离子:看“主族元素原子的次外层电子数+ 原子的最外层电子数一化合价数”是否等于8,若为8,则该原子满足最外层8电子结构,否则不满足。
(2)阴离子:看“其原子的最外层电子数+化合价的绝对值”是否等于8,若为8,则该原子满足最外层8 电子结构,否则不满足。
2.共价化合物计算“各原子的最外层电子数+化合价的绝对值” 是否等于8,若为8,则该原子满足最外层8电子结构,否则不满足。另外,还有一些不满足8电子结构的特殊粒子,请大家记住:
(1)主族元素形成的化合物中:
a.H、Li、Be、B元素原子不满足最外层8电子结构.
b.非最高价离子(如 Pb2+、Bi3+等)也不满足最外层8电子结构。
(2)过渡金属元素形成的离子最外层电子数一般大于8.
定义:
在化学反应中,一般是原子的最外层电子数目发生变化。为了简便起见,化学中常在元素符号周围用小黑点“· ”或小叉“×”来表示元素原子的最外层电子,相应的式子叫做电子式。
(1)原子的电子式:H· 、Na· 、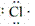
(2)阳离子的电子式:不画出离子最外层电子数,元素右上角标出“n+”电荷字样:Na+、Al3+、Mg2+
(3)阴离子的电子式:要画出最外层电子数,用 “[ ]”括起来,右上角标出“n-”: 、
、 、
、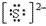
(4)离子化合物的电子式:由阴、阳离子的电子式组成,相同离子不能合并: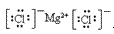 、
、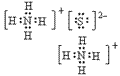
(5)共价化合物的电子式:画出离子最外层电子数: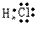 、
、
(6)用电子式表示物质形成的过程:
氯化氢的形成过程: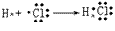
氯化镁的形成过程: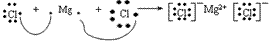
结构式:
共价键中的每一对共用电子用一根短线表示,未成键电子不写出,物质的电子式就变成了结构式。
例如: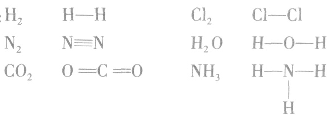
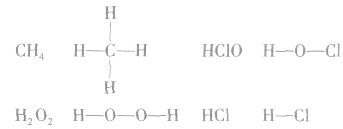
书写电子式的常见错误:
1.漏写未参与成键的电子,如: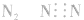
2.化合物类型不清,漏写或多写“[]”及错写电荷数,如: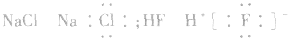
3.书写不规范,错写共用电子对如:N2的电子式为: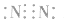 ,不能写成:
,不能写成: ,更不能写成:
,更不能写成: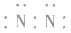 或
或 。
。
4.不考虑原子间的结合顺序如:HClO的电子式为 ,而非
,而非 。因氧原子需形成2对共用电子才能达到稳定结构,而H、 Cl各需形成1对共用电子就能达到稳定结构。
。因氧原子需形成2对共用电子才能达到稳定结构,而H、 Cl各需形成1对共用电子就能达到稳定结构。
5.不考虑原子最外层有几个电子均写成8电子结构如: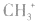 的电子式为
的电子式为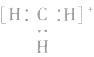 ,而非
,而非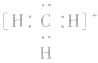 , 因
, 因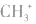 中碳原子最外层应有6个电子(包括共用电子),而非8个电子。
中碳原子最外层应有6个电子(包括共用电子),而非8个电子。
6.不清楚A如型离子化合物中两个B是分开写还是写一块如: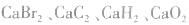 中
中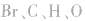 均为-l 价,Br-、H-已达到稳定结构,应分开写;C原子得一个电子,最外层有5个电子,需形成三对共用电子才能达到稳定结构,不能分开写;氧原子得一个电子,最外层有7个电子,需形成一对共用电子才能达到稳定结构,也不能分开写。它们的电子式分别为:
均为-l 价,Br-、H-已达到稳定结构,应分开写;C原子得一个电子,最外层有5个电子,需形成三对共用电子才能达到稳定结构,不能分开写;氧原子得一个电子,最外层有7个电子,需形成一对共用电子才能达到稳定结构,也不能分开写。它们的电子式分别为: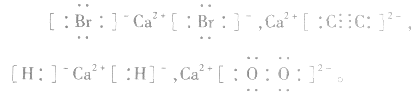
结构式的简便写法,着重突出结构特点(官能团),如CH3-CH3,CH2=CH2
与“下列化学用语的使用及说法中正确的是[ ]A.K+与Ar的结构示意...”考查相似的试题有:
- 下列物质的体积约为22.4L的是[ ]A.标准状况下1mol H2OB.20℃、101 kPa时36.5g HClC.标准状况下80g CuOD.标准状况下0.4 mol...
- (1)5molCO2的质量是______;在标准状况下所占的体积约为______;所含的分子数目约为______;所含氧原子的数目约为______....
- 下列粒子的结构表示正确的是[ ]A.18O的结构示意图B.O2-的结构示意图C.Ca2+的电子式D.Mg2+的电子式:Mg2+
- (1)下面列出了几组物质,请将物质的合适组号填写在空格上。互为同位素的是____________;互为同分异构体的是_____________...
- 下列关于中学化学中的“水”对应正确的是( )A.蒸馏水--H2OB.氯水--Cl2、H2O、HClO、H+、Cl-、ClO-、OH-(少量)C.王水--浓...
- 丁子香酚可用于配制康乃馨型香精及制作杀虫剂和防腐剂,结构简式如图。下列物质在一定条件下不能跟丁子香酚反应的是A.NaOH溶...
- 有多种同分异构体,其中符合属于酯类并含含苯环的同分异构体有多少种(不考虑立异构)A.6B.5C.4D.3
- 完全燃烧0.1mol某烃,燃烧产物依次通过如图所示的装置,实验结束后,称得甲装置增重9.0g,乙装置增重17.6g.求(1)该烃的化...
- 萘分子的结构可以表示为 或,两者是等同的。苯并[α]芘是强致癌物质(存在于烟囱灰、煤焦油、燃烧的烟雾和内燃机的尾气中)。...
- (12分) 格氏试剂(RMgX)是有机反应中的一种重要试剂,它的制法为:(R为烃基,X为卤素)格氏试剂能与醛反应生成醇,反应历程为...