本试题 “绿色化学是20世纪90年代出现的一个多学科交叉的研究领域。它可以诠释为环境友好化学,其核心内涵是反应过程和化工生产中,尽量减少或彻底消除使用和生产有害...” 主要考查您对绿色化学
大气污染、改善大气质量
水体污染、爱护水资源
工业生产纯碱
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 绿色化学
- 大气污染、改善大气质量
- 水体污染、爱护水资源
- 工业生产纯碱
绿色化学:
1.定义绿色化学是一门研究运用现代科学技术的原理和方法来减少或消除化学产品的设计、生产和应用中有害物质的使用与产生,使所研究开发的化学产品和过程对环境更加友好的学科。
2.绿色化学的基本原则
(1)防治污染的产生优于治理产生的污染;
(2)原子经济性(设计的合成方法应将反应过程中所用的材料,尽可能全部转化到最终产品中)即原子的利用率达到100%。
(3)应考虑到能源消耗对环境和经济的影响,并应尽量少地使用能源(在常温、常压下进行)。
1.定义绿色化学是一门研究运用现代科学技术的原理和方法来减少或消除化学产品的设计、生产和应用中有害物质的使用与产生,使所研究开发的化学产品和过程对环境更加友好的学科。
2.绿色化学的基本原则
(1)防治污染的产生优于治理产生的污染;
(2)原子经济性(设计的合成方法应将反应过程中所用的材料,尽可能全部转化到最终产品中)即原子的利用率达到100%。
(3)应考虑到能源消耗对环境和经济的影响,并应尽量少地使用能源(在常温、常压下进行)。
大气污染:
(1)大气污染源:颗粒物、硫的氧化物、氮的氧化物、CO 碳氢化合物、氟氯代烷
(2)大气污染危害:危害人体健康、影响动植物的生长、严重时会影响地球的气候
(3)全球性三大环境问题:酸雨、臭氧层受损、温室效应
①酸雨:正常雨水:PH约为5.6 酸雨:PH小于5.6 我国为硫酸型酸雨,烧煤炭造成
硫酸型:硫的氧化物转化 SO2+H2O=H2SO3 2H2SO3+O2=2H2SO4 大气中烟尘和O3作催化剂
硝酸型:氮的氧化物转化 3NO2+H2O=2HNO3+NO↑
②臭氧层:自然界的臭氧90%集中在距地面15-50km的大气平流层中 吸收自太阳的大部分紫外线
引起臭氧层受损物质 氟氯代烷(致冷剂)、哈龙(含溴的灭火剂)、CCl4、N2O、NO、核弹爆炸产物
保护臭氧层公约:《保护臭氧层维也纳公约》 《关于消耗臭氧层物质的蒙特利尔议定书公约》
③温室效应:太阳短波辐射可以透过大气射入地面,而地面增暖后放出的长短辐射却被大气中的二氧化碳等物质所吸收,从而产生大气变暖的效应
温室效应后果:荒漠将扩大,土地侵蚀加重,森林退向极地,旱涝灾害严重,雨量将增加7-11%;温带冬天更湿,夏天更旱;热带也将变得更湿,干热的副热带变得更干旱,两极冰块将熔化,使海平面上升1米多,引起厄尔尼诺现象
引起温室效应的物质:CO2、CH4、N2O、氟氯代烷
改善大气质量:
①减少煤等化石燃料燃烧产生污染:改善燃煤质量、改进燃烧装置、技术和排烟设备、发展洁净煤技术和综合利用、调整和优化能源结构
煤的综合利用: 煤的的干馏、煤的气化、煤的液化
煤的气化 C+H2O(g)=CO+H2
煤的液化 CO+2H2→CH3OH
煤的脱硫 2CaCO3+O2+2SO2=2CaSO4+2CO2
②减少汽车等机动车尾气污染
尾气污染(占大气污染排出总量的40-50%):CO、NO2、NO、碳氢化合物
使用无铅汽油:四乙基铅作抗爆震剂,铅对神经系统损害大
尾气系统加催化转化器:前半部 2CO+2NO2 CO2+N2 后半部 2CO+O2
CO2+N2 后半部 2CO+O2 2CO2 C7H16+11O2
2CO2 C7H16+11O2 7CO2+8H2O
7CO2+8H2O
(1)大气污染源:颗粒物、硫的氧化物、氮的氧化物、CO 碳氢化合物、氟氯代烷
(2)大气污染危害:危害人体健康、影响动植物的生长、严重时会影响地球的气候
(3)全球性三大环境问题:酸雨、臭氧层受损、温室效应
①酸雨:正常雨水:PH约为5.6 酸雨:PH小于5.6 我国为硫酸型酸雨,烧煤炭造成
硫酸型:硫的氧化物转化 SO2+H2O=H2SO3 2H2SO3+O2=2H2SO4 大气中烟尘和O3作催化剂
硝酸型:氮的氧化物转化 3NO2+H2O=2HNO3+NO↑
②臭氧层:自然界的臭氧90%集中在距地面15-50km的大气平流层中 吸收自太阳的大部分紫外线
引起臭氧层受损物质 氟氯代烷(致冷剂)、哈龙(含溴的灭火剂)、CCl4、N2O、NO、核弹爆炸产物
保护臭氧层公约:《保护臭氧层维也纳公约》 《关于消耗臭氧层物质的蒙特利尔议定书公约》
③温室效应:太阳短波辐射可以透过大气射入地面,而地面增暖后放出的长短辐射却被大气中的二氧化碳等物质所吸收,从而产生大气变暖的效应
温室效应后果:荒漠将扩大,土地侵蚀加重,森林退向极地,旱涝灾害严重,雨量将增加7-11%;温带冬天更湿,夏天更旱;热带也将变得更湿,干热的副热带变得更干旱,两极冰块将熔化,使海平面上升1米多,引起厄尔尼诺现象
引起温室效应的物质:CO2、CH4、N2O、氟氯代烷
改善大气质量:
①减少煤等化石燃料燃烧产生污染:改善燃煤质量、改进燃烧装置、技术和排烟设备、发展洁净煤技术和综合利用、调整和优化能源结构
煤的综合利用: 煤的的干馏、煤的气化、煤的液化
煤的气化 C+H2O(g)=CO+H2
煤的液化 CO+2H2→CH3OH
煤的脱硫 2CaCO3+O2+2SO2=2CaSO4+2CO2
②减少汽车等机动车尾气污染
尾气污染(占大气污染排出总量的40-50%):CO、NO2、NO、碳氢化合物
使用无铅汽油:四乙基铅作抗爆震剂,铅对神经系统损害大
尾气系统加催化转化器:前半部 2CO+2NO2
 CO2+N2 后半部 2CO+O2
CO2+N2 后半部 2CO+O2 2CO2 C7H16+11O2
2CO2 C7H16+11O2 7CO2+8H2O
7CO2+8H2O水体污染:
(1)重金属:使人体的蛋白质变性,可通过食物链被富集,人通过饮水和食物摄入而中毒
汞Hg:水俣病 镉Cd:痛痛病
还有铬、铅等
(2)植物营养物质污染:生活废水和工业废水蛋白质含N、洗涤剂和化肥中含P等植物营养素
在分解时大量消耗水中的溶解氧,释放养分,使藻类和浮游生物大量繁殖
颜色:蓝、红、棕
在江河湖泊在出现叫水华;在海湾在出现叫赤潮。
海水淡化:
(1)海水淡化又称脱盐,利用物理、化学、生物方法将海水中溶解的盐脱除。海水淡化的方法有蒸馏法、膜法(电渗析、反渗透)、冷冻法、离子交换法等。其中蒸馏法、膜法是主要方法。
(2)常用方法
①蒸馏法能耗大,成本高;但设备相对简单,技术比较成熟改进方法:采用降低容器内压强的方法,并安装热交换器。原理:压强越大,液体的沸点越高。
②电渗析法耗能最少,成本较低,海水淡化大多采用这种方法。
③反渗透法效率最高。
④冷冻法需要大量的能源。
(1)重金属:使人体的蛋白质变性,可通过食物链被富集,人通过饮水和食物摄入而中毒
汞Hg:水俣病 镉Cd:痛痛病
还有铬、铅等
(2)植物营养物质污染:生活废水和工业废水蛋白质含N、洗涤剂和化肥中含P等植物营养素
在分解时大量消耗水中的溶解氧,释放养分,使藻类和浮游生物大量繁殖
颜色:蓝、红、棕
在江河湖泊在出现叫水华;在海湾在出现叫赤潮。
海水淡化:
(1)海水淡化又称脱盐,利用物理、化学、生物方法将海水中溶解的盐脱除。海水淡化的方法有蒸馏法、膜法(电渗析、反渗透)、冷冻法、离子交换法等。其中蒸馏法、膜法是主要方法。
(2)常用方法
①蒸馏法能耗大,成本高;但设备相对简单,技术比较成熟改进方法:采用降低容器内压强的方法,并安装热交换器。原理:压强越大,液体的沸点越高。
②电渗析法耗能最少,成本较低,海水淡化大多采用这种方法。
③反渗透法效率最高。
④冷冻法需要大量的能源。
工业生产纯碱:
纯碱(学名碳酸钠)实际上是盐,由于它在水中发生水解作用而使溶液呈碱性。纯碱易溶于水,呈强碱性,能提供
Na+离子。这些性质使它们被广泛地用于制玻璃、肥皂、纺织、印染、漂白、造纸、精制石油、冶金及其他化学工业等各部门中。
碳酸钠在自然界中存在相当广泛。一些生长在盐碱地和海岸附近的植物中含有碳酸钠,可以从植物的灰烬中提取;当冬季来临时,碱湖中所含的碳酸钠结晶析出,经过简单的加工就可以使用。
世界上最早是通过路布兰法实现了碳酸钠的工业生产。其生产原理是:
用硫酸将食盐转变成硫酸钠
NaCl+H2SO4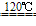 NaHSO4+HCl↑NaCl+NaHSO4
NaHSO4+HCl↑NaCl+NaHSO4 Na2SO4+HCl↑
Na2SO4+HCl↑
将硫酸钠与木炭、石灰石一起加热,反应生成碳酸钠和硫化钙
Na2SO4+2C Na2S+2CO2↑ Na2S+CaCO3
Na2S+2CO2↑ Na2S+CaCO3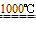 Na2CO3+CaS
Na2CO3+CaS
存在原料利用不充分、成本较高、设备腐蚀严重等
氨碱法生产硫酸:
氨碱法是由比利时人索尔维发明的,所以,氨碱法也称为索尔维制碱法。氨碱法的原料也是氯化钠和碳酸钙,不同的是它还使用了炼焦的副产品氨。
原料:CaCO3、NaCl、NH3
1.生成碳酸氢钠和氯气铵
将CO2通入含NH3的饱和NaCl溶液中
NH3+CO2+H2O==NH4HCO3 NaCl+NH4HCO3==NaHCO3↓+NH4Cl
2.抽取碳酸钠2NaHCO3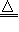 Na2CO3+CO2↑+H2O↑
Na2CO3+CO2↑+H2O↑
氨碱法生产原理:
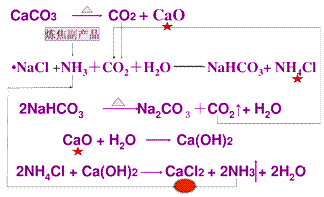
氨碱法的优点:原料便宜易得,氨和部分二氧化碳可循环利用,产品纯度高,步骤简单。氨碱法的缺点:副产物氯化钙的处理问题,氯化钠的利用率低。
联合制碱法:
我国化学侯德榜(下图)改革国外的纯碱生产工艺,生产流程可简要表示如下:

(1)上述生产纯碱的方法称联合制碱法或侯德榜制碱法,副产品的一种用途为化肥或电解液或焊药等。
(2)沉淀池中发生的化学反应方程式是NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓或NH3+CO2+H2O=NH4HCO3 NH4HCO3+NaCl=NaHCO3↓+NH4Cl。
(3)写出上述流程中X物质的分子式CO2。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了I 的循环。从沉淀池中取出沉淀的操作是过滤
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加稀硝酸和硝酸银溶液
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用是:
①增大NH4+的浓度,使NH4Cl更多地析出②使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
联合法综合利用了合成氨的原料,提高了氯化钠的利用率,减少了环境污染。
NH3、CO2都来自于合成氨工艺;这样NH4Cl就成为另一产品化肥。综合利用原料、降低成本、减少环境污染,NaCl利用率达96%。
纯碱(学名碳酸钠)实际上是盐,由于它在水中发生水解作用而使溶液呈碱性。纯碱易溶于水,呈强碱性,能提供
Na+离子。这些性质使它们被广泛地用于制玻璃、肥皂、纺织、印染、漂白、造纸、精制石油、冶金及其他化学工业等各部门中。
碳酸钠在自然界中存在相当广泛。一些生长在盐碱地和海岸附近的植物中含有碳酸钠,可以从植物的灰烬中提取;当冬季来临时,碱湖中所含的碳酸钠结晶析出,经过简单的加工就可以使用。
世界上最早是通过路布兰法实现了碳酸钠的工业生产。其生产原理是:
用硫酸将食盐转变成硫酸钠
NaCl+H2SO4
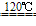 NaHSO4+HCl↑NaCl+NaHSO4
NaHSO4+HCl↑NaCl+NaHSO4 Na2SO4+HCl↑
Na2SO4+HCl↑ 将硫酸钠与木炭、石灰石一起加热,反应生成碳酸钠和硫化钙
Na2SO4+2C
 Na2S+2CO2↑ Na2S+CaCO3
Na2S+2CO2↑ Na2S+CaCO3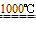 Na2CO3+CaS
Na2CO3+CaS 存在原料利用不充分、成本较高、设备腐蚀严重等
氨碱法生产硫酸:
氨碱法是由比利时人索尔维发明的,所以,氨碱法也称为索尔维制碱法。氨碱法的原料也是氯化钠和碳酸钙,不同的是它还使用了炼焦的副产品氨。
原料:CaCO3、NaCl、NH3
1.生成碳酸氢钠和氯气铵
将CO2通入含NH3的饱和NaCl溶液中
NH3+CO2+H2O==NH4HCO3 NaCl+NH4HCO3==NaHCO3↓+NH4Cl
2.抽取碳酸钠2NaHCO3
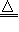 Na2CO3+CO2↑+H2O↑
Na2CO3+CO2↑+H2O↑ 氨碱法生产原理:

氨碱法的优点:原料便宜易得,氨和部分二氧化碳可循环利用,产品纯度高,步骤简单。氨碱法的缺点:副产物氯化钙的处理问题,氯化钠的利用率低。
联合制碱法:
我国化学侯德榜(下图)改革国外的纯碱生产工艺,生产流程可简要表示如下:

(1)上述生产纯碱的方法称联合制碱法或侯德榜制碱法,副产品的一种用途为化肥或电解液或焊药等。
(2)沉淀池中发生的化学反应方程式是NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓或NH3+CO2+H2O=NH4HCO3 NH4HCO3+NaCl=NaHCO3↓+NH4Cl。
(3)写出上述流程中X物质的分子式CO2。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了I 的循环。从沉淀池中取出沉淀的操作是过滤
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加稀硝酸和硝酸银溶液
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用是:
①增大NH4+的浓度,使NH4Cl更多地析出②使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
联合法综合利用了合成氨的原料,提高了氯化钠的利用率,减少了环境污染。
NH3、CO2都来自于合成氨工艺;这样NH4Cl就成为另一产品化肥。综合利用原料、降低成本、减少环境污染,NaCl利用率达96%。
发现相似题
与“绿色化学是20世纪90年代出现的一个多学科交叉的研究领域。它...”考查相似的试题有:
- “绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是 ①实验室收集氨气采用图所示装置 ②实验室中做氯气与钠的反应实验时采...
- 2011年7月16日14时25分,中国石油大连石化公司厂区内1000万吨常减压蒸馏装置换热器发生泄漏,引发大火,所幸的是无人员伤亡。...
- 下列药物类型中由于过度使用导致人类面临无药可用的危机的是( )A.中成药B.抗生素C.维生素等保健药D.抗酸药
- 近年来,北京等大城市的公共汽车开始采用天然气作为汽车的燃料,其主要目的是A.防止石油短缺B.减低成本C.减少对大气的污染...
- (14分)小伶同学某日的食谱为:早餐——鸡蛋1个,包子2个,牛奶1瓶;午餐——米饭100g,炸鸡腿70g,炒五花肉50g,煎蛋50g;晚餐—...
- 导致下列现象的主要原因与排放CO2有关的是( )。A.酸雨B.光化学烟雾C.臭氧层空洞D.温室效应
- 下列叙述正确的是[ ]①CO2的大量排放会加剧温室效应 ②酸雨的pH为5.6,主要是因为溶解了SO2 ③利用太阳能、风能和氢能替代化石能...
- 下列措施符合“绿色化学”思想的是A.直接排放含磷生活污水B.大量使用氟里昂作为冰箱制冷剂C.使用可降解塑料代替不可降解塑料...
- 下列说法中不正确的是 ( )。A.空气中的臭氧对人体健康有益无害B.光化学烟雾的产生与汽车排放的尾气有关C.倡导人们在购物时...
- 为实现扼制温室效应,使用下列燃料可实现二氧化碳零排放的是 ( )A.氢气B.天然气C.汽油D.乙醇汽油