本试题 “下列说法中,不正确的是( )A.过量的红磷在充满空气的密闭容器中燃烧,可除去容器内的氧气B.“曾青得铁则化为铜”是指将铁片放入氯化铜、硝酸铜等溶液中都可...” 主要考查您对硬水和软水
氧气的性质
金属活动性
碳的性质
酸碱指示剂
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 硬水和软水
- 氧气的性质
- 金属活动性
- 碳的性质
- 酸碱指示剂
定义:
硬水是含有较多可溶性钙、镁化合物的水。
软水是不含或含较少可溶性钙、镁化合物的水。
水的硬度:
水的硬度常用一种规定的标准来衡量,这个标准是:把1L水里含10mgCaO(或相当于10mgCaO)称为1度。
硬水和软水的检验:
(1)用肥皂水来检验硬水和软水,把肥皂水滴在水里搅拌,产生泡沫多的是软水,产生泡沫少或不产生泡沫的是硬水
(2)用加热煮沸的方法检验硬水和软水。水加热煮沸时,有较多沉淀的是硬水,不产生沉淀或者产生沉淀较少的是软水。
硬水的软化:
就是设法除去硬水中的钙、镁化合物。
硬水软化的方法:生活中常用煮沸法,工业上常用离子交换法和药剂软化法,实验室常用蒸馏法,蒸馏法是净化程度较高的水,蒸馏时应注意以下几点:
①蒸馏瓶中的液体不能超过其容积的2/3.
②加热时,应在烧瓶中放几粒沸石(或碎瓷片)。
③装置气密性良好
④水银温度计的水银球应放在蒸馏烧瓶的支管口附近。
使用硬水造成的危害:
饮用水中含有微量的钙、镁成分,对人体健康是有益的。但是,水中含太多的钙、镁成分,对生活和生产都有危害。
①用硬水洗涤,不仅浪费肥皂,而且会在织物上积有肥皂跟钙、镁反应后生成的沉淀,不容易洗干净,还会使纤维变脆、易断。
②硬水有苦涩味,长期饮用硬水会使人的胃肠功能紊乱,出现不同程度的腹胀、腹泻和腹痛。
③锅炉用水硬度太大,会产生水垢,这会大大降低锅炉的导热能力,造成燃料的浪费。另外,当水垢爆裂脱落时,会造成炉壁局部受热不均,易引起锅炉爆炸。
离子交换法:
离子交换法是工业生产软化水的重要方法之一。离子交换法的原理:离子交换树脂是一种聚合物,带有相应的功能基团(一般情况下,常规的钠离子交换树脂带有大量的钠离子),当含钙、镁离子较高的硬水经过离子交换树脂时,离子交换树脂即可以释放出钠离子,其功能基团与钙、镁离子结合。这样水中的钙、镁离子含量下降,水的硬度降低,硬水即可被软化为软水。离子交换法的流程为:工作(即交换)、反洗、再生、清洗四个过程。
硬水是含有较多可溶性钙、镁化合物的水。
软水是不含或含较少可溶性钙、镁化合物的水。
水的硬度:
水的硬度常用一种规定的标准来衡量,这个标准是:把1L水里含10mgCaO(或相当于10mgCaO)称为1度。
硬水和软水的检验:
(1)用肥皂水来检验硬水和软水,把肥皂水滴在水里搅拌,产生泡沫多的是软水,产生泡沫少或不产生泡沫的是硬水
(2)用加热煮沸的方法检验硬水和软水。水加热煮沸时,有较多沉淀的是硬水,不产生沉淀或者产生沉淀较少的是软水。
硬水的软化:
就是设法除去硬水中的钙、镁化合物。
硬水软化的方法:生活中常用煮沸法,工业上常用离子交换法和药剂软化法,实验室常用蒸馏法,蒸馏法是净化程度较高的水,蒸馏时应注意以下几点:
①蒸馏瓶中的液体不能超过其容积的2/3.
②加热时,应在烧瓶中放几粒沸石(或碎瓷片)。
③装置气密性良好
④水银温度计的水银球应放在蒸馏烧瓶的支管口附近。
使用硬水造成的危害:
饮用水中含有微量的钙、镁成分,对人体健康是有益的。但是,水中含太多的钙、镁成分,对生活和生产都有危害。
①用硬水洗涤,不仅浪费肥皂,而且会在织物上积有肥皂跟钙、镁反应后生成的沉淀,不容易洗干净,还会使纤维变脆、易断。
②硬水有苦涩味,长期饮用硬水会使人的胃肠功能紊乱,出现不同程度的腹胀、腹泻和腹痛。
③锅炉用水硬度太大,会产生水垢,这会大大降低锅炉的导热能力,造成燃料的浪费。另外,当水垢爆裂脱落时,会造成炉壁局部受热不均,易引起锅炉爆炸。
离子交换法:
离子交换法是工业生产软化水的重要方法之一。离子交换法的原理:离子交换树脂是一种聚合物,带有相应的功能基团(一般情况下,常规的钠离子交换树脂带有大量的钠离子),当含钙、镁离子较高的硬水经过离子交换树脂时,离子交换树脂即可以释放出钠离子,其功能基团与钙、镁离子结合。这样水中的钙、镁离子含量下降,水的硬度降低,硬水即可被软化为软水。离子交换法的流程为:工作(即交换)、反洗、再生、清洗四个过程。
定义:
氧气,空气主要组分之一,比空气重,标准状况(0℃和大气压强101325帕)下密度为1.429克/升。无色、无臭、无味。在水中溶解度很小。压强为101kPa时,氧气在约-183摄氏度时变为淡蓝色液体,在约-218摄氏度时变成雪花状的淡蓝色固体。
氧气的性质:
1.氧气的物理性质:
(1)无色无味,标况下,氧气的密度为1.429g/L,密度比空气大,难溶于水,1L水中只能溶解约30ml的氧气。
(2)三态变化:氧气(无色气体) 液氮(淡蓝色液体)
液氮(淡蓝色液体)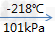 固态氮(淡蓝色雪花状)
固态氮(淡蓝色雪花状)
(3)工业产生的氧气,一般加压贮存在蓝色的钢瓶中。
2.氧气的化学性质:
(1)化学性质较活泼,在一定条件下,可以和多种物质发生化学反应,同时放出热量;具有助燃性和氧化性,在化学反应中提供氧,是一种常用的氧化剂。
(2)助燃性,氧化性
①与金属的反应:
2Mg+O2 2MgO
2MgO
3Fe+2O2 Fe3O4
Fe3O4
②与非金属的反应:
C+O2 CO2(O2充分)
CO2(O2充分)
2C+O2 2CO(O2不充分)
2CO(O2不充分)
③与化合物的反应:
2CO+O2 2CO2
2CO2
CH4+2O2 CO2+2H2O
CO2+2H2O
C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
易错点:
(1)误认为氧气具有可燃性,可以做燃料
氧气可以帮助可燃物燃烧,具有助燃性,它本身不能燃烧,不能做可燃物。
(2)误认为氧气的化学性质非常活泼,能与所有物质发生反应
氧气是一种化学性质非常活泼的气体,在一定条件下能与许多物质发生化学反应,但不是与所有物质都能发生化学反应。
(3)误认为燃烧都需要氧气
燃烧有广义和狭义之分,通常所说的燃烧是指可燃物与氧气发生的一种发光,放热的剧烈的氧化反应。燃烧的条件之一是需要氧气。但有一些燃烧不需要氧气,如镁在二氧化碳中也能燃烧。
(4)误认为物质与氧气的反应叫氧化反应
氧化反应是物质与氧发生的反应,其中包括物质与氧气中的氧元素发生的反应,也包括物质与其他含氧物质中的氧元素发生的反应。如氢气与氧气反应生成水是氧化反应,氢气与氧化铜反应生成铜和水也是氧化反应。
(5)误认为氧气与液氧性质不行
物质的性质包括物理性质和化学性质,氧气与液氧物理性质不同,但化学性质是相同的,因为它们二者的分子构成相同,都是由氧分子构成的。
(6)误认为含氧的物质都能制取氧气。
制取氧气需要含氧的物质,但不是所有的含氧物质都能用来制取氧气。
氧气,空气主要组分之一,比空气重,标准状况(0℃和大气压强101325帕)下密度为1.429克/升。无色、无臭、无味。在水中溶解度很小。压强为101kPa时,氧气在约-183摄氏度时变为淡蓝色液体,在约-218摄氏度时变成雪花状的淡蓝色固体。
氧气的性质:
1.氧气的物理性质:
(1)无色无味,标况下,氧气的密度为1.429g/L,密度比空气大,难溶于水,1L水中只能溶解约30ml的氧气。
(2)三态变化:氧气(无色气体)
 液氮(淡蓝色液体)
液氮(淡蓝色液体) 固态氮(淡蓝色雪花状)
固态氮(淡蓝色雪花状)(3)工业产生的氧气,一般加压贮存在蓝色的钢瓶中。
2.氧气的化学性质:
(1)化学性质较活泼,在一定条件下,可以和多种物质发生化学反应,同时放出热量;具有助燃性和氧化性,在化学反应中提供氧,是一种常用的氧化剂。
(2)助燃性,氧化性
①与金属的反应:
2Mg+O2
 2MgO
2MgO3Fe+2O2
 Fe3O4
Fe3O4②与非金属的反应:
C+O2
 CO2(O2充分)
CO2(O2充分)2C+O2
 2CO(O2不充分)
2CO(O2不充分)③与化合物的反应:
2CO+O2
 2CO2
2CO2CH4+2O2
 CO2+2H2O
CO2+2H2OC2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O易错点:
(1)误认为氧气具有可燃性,可以做燃料
氧气可以帮助可燃物燃烧,具有助燃性,它本身不能燃烧,不能做可燃物。
(2)误认为氧气的化学性质非常活泼,能与所有物质发生反应
氧气是一种化学性质非常活泼的气体,在一定条件下能与许多物质发生化学反应,但不是与所有物质都能发生化学反应。
(3)误认为燃烧都需要氧气
燃烧有广义和狭义之分,通常所说的燃烧是指可燃物与氧气发生的一种发光,放热的剧烈的氧化反应。燃烧的条件之一是需要氧气。但有一些燃烧不需要氧气,如镁在二氧化碳中也能燃烧。
(4)误认为物质与氧气的反应叫氧化反应
氧化反应是物质与氧发生的反应,其中包括物质与氧气中的氧元素发生的反应,也包括物质与其他含氧物质中的氧元素发生的反应。如氢气与氧气反应生成水是氧化反应,氢气与氧化铜反应生成铜和水也是氧化反应。
(5)误认为氧气与液氧性质不行
物质的性质包括物理性质和化学性质,氧气与液氧物理性质不同,但化学性质是相同的,因为它们二者的分子构成相同,都是由氧分子构成的。
(6)误认为含氧的物质都能制取氧气。
制取氧气需要含氧的物质,但不是所有的含氧物质都能用来制取氧气。
定义:
金属活动性指金属单质在水溶液中失去电子生成金属阳离子的性质。
常见金属活动性顺序:
K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au
金属活动性顺序表的意义
(1)金属的位置越靠前,它的活动性越强
(2)位于氢前面的金属能置换出酸中的氢(强氧化酸除外)。
(3)位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来(K,Ca,Na除外)。
(4)很活泼的金属,如K、Ca、Na与盐溶液反应,先与溶液中的水反应生成碱,碱再与盐溶液反应,没有金属单质生成。如:
2Na+CuSO4+2H2O==Cu(OH)2↓+Na2SO4+H2↑
(5)不能用金属活动性顺序去说明非水溶液中的置换反应,如氢气在加热条件下置换氧化铁中的铁:
Fe2O3+3H2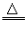 2Fe+3H2O
2Fe+3H2O
金属原子与金属离子得失电子能力的比较

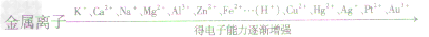
金属活动性顺序表的应用
(1)判断某些置换反应能否发生
a.判断金属与酸能否反应:
条件:
①金属必须排在氢前面
②酸一般指盐酸或稀硫酸
b.判断金属与盐溶液能否反应:
条件:
①单质必须排在盐中金属的前面
②盐必须可溶于水
③金属不包含K、Ca、Na
(2)根据金属与盐溶液的反应判断滤液、滤渣的成分。如向CuSO4,AgNO3混合液中加铁粉,反应后过滤,判断滤液和滤渣成分。铁与CuSO4和AgNO3溶液反应有先后顺序,如果铁足量,先将AgNO3中的Ag完全置换后再置换CuSO4中的Cu,那么溶液中只有FeSO4;如果铁的量不足,应按照“先后原则”分别讨论滤液和滤渣的成分。
(3)根据金属活动性顺序表判断金属与酸反应的速率或根据反应速率判断金属的活动性顺序。如镁、锌、铁三种金属与同浓度的稀H2SO4反应产生氢气的速率:Mg>Zn>Fe,则可判断金属活动性Mg>Zn>Fe,
(4)利用金属活动性顺序表研究金属冶炼的历史。金属活动性越弱,从其矿物中还原出金属单质越容易; 金属活动性越强,从其矿物中还原出金属单质越难。所以越活泼的金属越不易冶炼,难于冶炼的金属开发利用的时间就越迟。
(5)应用举例
a.湿法炼铜我国劳动人民在宋代就掌握了湿法炼铜技术,即将铁放入硫酸铜溶液中置换出铜: Fe+CuSO4=FeSO4+Cu。
b.从洗相废液中回收银洗相废掖中含有大量的硝酸银,可用铁置换回收: Fe+2AgNO3==Fe(NO3)2+2Ag。
c.处理工业废水中的铜、汞离子工业废水中常含铜、汞等金属离子,这些离子对生物有很大的危害,在排放前必须进行处理,可用铁置换回收:Fe+CuSO4==FeSO4+Cu
d.实验室选择金属与酸反应制取氢气在金属活动性顺序表中,H之前的金属都能跟稀 H2SO4、稀HCl反应产生氢气,但Zn之前的金属与酸反应太快。不便操作;Zn之后的金属与酸反应太慢,花费时间太长,从经济效益和反应速率多方而考虑,Zn是最合适的金属。
金属与混合溶液的反应
(1)将一种金属单质放入几种金属的盐溶液的混合液中时,其中排在金属活动性顺序表巾最靠后的金属最先被置换出来,然后再依次置换出稍靠后的金属。简记为“在金属活动性顺序中,距离远,先反应”。如将金属Zn。放入FeSO4和CuSO4的混合溶液中,Zn先与CuSO4发生置换反应,与CuSO4反应完后再与FeSO4 发生置换反应。根据金属锌的最不同可分为以下几种情况:
(2)将几种不同的金属放入同一种盐溶液中,发生反应的情况与将一种金属放入几种金属的盐溶液中相似,也是在金属活动性顺序表中,距离越远的先反应,然后是距离较远的反应。
金属与酸反应生成氢气图像问题的分析方法:
(1)等质氢图:两种金属反应产生的氢气质量相同,此图反映两种情况:

①酸不足,金属过虽,产生的氢气质量由酸的质量决定。
②酸足量,投放的两种金属与酸反应产生氢气的质量恰好相同,如6.5g锌和5.6g铁分别投入足量的盐酸中反应产生的氢气质量相同。
(2)等质等价金属图:如等质量的镁、铁、锌与足量的酸反应生成的金属离子都是+2价,产生氢气的速率和质量不同。此图反映出:

①金属越活泼,图示反应物的线越陡,如Mg线比Zn线陡,Zn线比Fe线陡,说明活泼性Mg>Zn>Fe
②金属的相对原子质量越小。等质量时,与酸反应产生的氢气越多,曲线的拐点越高,因此,相对原子质量Zn >Fe>Mg。
可简单概括为:越陡越活,越高越小。
(3)等质不等价金属图:铝、镁、锌与酸反应生成金属离子的化合价分别为+3、+2、+2,此图反映出等质不等价金属与酸反应不仅速率不同而且生成的氢气的质量与金属化合价有关。
可用下面式子计算氢气质量:

金属与酸或盐溶液反应前后溶液密度变化的判断方法:
金属与酸的反应和金属与盐溶液的反应均为置换反应,反应后溶液的溶质发生了改变,导致溶液的溶质质量分数、溶液的密度也随之改变。反应前后溶液的密度的变化取决于反应前后溶液中溶质的相对分子质量的相对大小。
(1)反应后溶液密度变小:如Fe+CuSO4== FeSO4+Cu,在该反应中,反应前溶液中的溶质为CuSO4,其相对分子质量为160;反应后溶液中的溶质为FeSO4,其相对分子质量为152,由于152<160,故该反应后溶液密度变小。
(2)反应后溶液密度变大:如Zn+H2SO4== ZnSO4+H2↑,在该反应中,反应前溶液中的溶质为H2SO4,相对分子质量为98;反应后溶液中溶质为ZnSO4,相对分子质童为161,由于161>98。故该反应后溶液密度变大。
真假黄金的鉴别:
黄金是一种具有金黄色光泽的金属、化学性质极不活泼。黄铜的外形与黄金非常相似,所以不法分子常用黄铜(Zn,Cu合金)来冒充黄金。但二者之间的性质有很大差异,可用多种方法鉴别。
方法一:取少量金黄色金属块于试管中,加入少量稀盐酸或稀硫酸,若有气泡产生(Zn+2HCl==ZnCl2 +H2),则原试样为黄铜;若没有气泡产生,则原试样为黄金。
方法二:取少量金黄色金属块,用天平称其质量,用量筒和水测出其体积,计算出金属块的密度与黄金的密度对照,若密度相等,则为黄金;若有较大的差异,则为黄铜。
方法三:取少员金黄色金属块在火焰上加热,若金属块表面变黑(2Cu+O2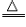 2CuO,则原试样为黄铜;若无变化,则为黄金。
2CuO,则原试样为黄铜;若无变化,则为黄金。
方法四:取少讨金黄色金属块于试管中,向试管中加人适量的硫酸铜溶液,若金属块表而出现红色物质且溶液颜色变浅(Zn+CuSO4==ZnSO4+Cu),则原试样为黄铜;若无变化,则原试样为黄金。
金属活动性指金属单质在水溶液中失去电子生成金属阳离子的性质。
常见金属活动性顺序:
K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au
金属活动性顺序表的意义
(1)金属的位置越靠前,它的活动性越强
(2)位于氢前面的金属能置换出酸中的氢(强氧化酸除外)。
(3)位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来(K,Ca,Na除外)。
(4)很活泼的金属,如K、Ca、Na与盐溶液反应,先与溶液中的水反应生成碱,碱再与盐溶液反应,没有金属单质生成。如:
2Na+CuSO4+2H2O==Cu(OH)2↓+Na2SO4+H2↑
(5)不能用金属活动性顺序去说明非水溶液中的置换反应,如氢气在加热条件下置换氧化铁中的铁:
Fe2O3+3H2
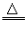 2Fe+3H2O
2Fe+3H2O金属原子与金属离子得失电子能力的比较

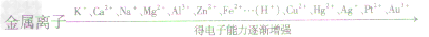
金属活动性顺序表的应用
(1)判断某些置换反应能否发生
a.判断金属与酸能否反应:
条件:
①金属必须排在氢前面
②酸一般指盐酸或稀硫酸
b.判断金属与盐溶液能否反应:
条件:
①单质必须排在盐中金属的前面
②盐必须可溶于水
③金属不包含K、Ca、Na
(2)根据金属与盐溶液的反应判断滤液、滤渣的成分。如向CuSO4,AgNO3混合液中加铁粉,反应后过滤,判断滤液和滤渣成分。铁与CuSO4和AgNO3溶液反应有先后顺序,如果铁足量,先将AgNO3中的Ag完全置换后再置换CuSO4中的Cu,那么溶液中只有FeSO4;如果铁的量不足,应按照“先后原则”分别讨论滤液和滤渣的成分。
(3)根据金属活动性顺序表判断金属与酸反应的速率或根据反应速率判断金属的活动性顺序。如镁、锌、铁三种金属与同浓度的稀H2SO4反应产生氢气的速率:Mg>Zn>Fe,则可判断金属活动性Mg>Zn>Fe,
(4)利用金属活动性顺序表研究金属冶炼的历史。金属活动性越弱,从其矿物中还原出金属单质越容易; 金属活动性越强,从其矿物中还原出金属单质越难。所以越活泼的金属越不易冶炼,难于冶炼的金属开发利用的时间就越迟。
(5)应用举例
a.湿法炼铜我国劳动人民在宋代就掌握了湿法炼铜技术,即将铁放入硫酸铜溶液中置换出铜: Fe+CuSO4=FeSO4+Cu。
b.从洗相废液中回收银洗相废掖中含有大量的硝酸银,可用铁置换回收: Fe+2AgNO3==Fe(NO3)2+2Ag。
c.处理工业废水中的铜、汞离子工业废水中常含铜、汞等金属离子,这些离子对生物有很大的危害,在排放前必须进行处理,可用铁置换回收:Fe+CuSO4==FeSO4+Cu
d.实验室选择金属与酸反应制取氢气在金属活动性顺序表中,H之前的金属都能跟稀 H2SO4、稀HCl反应产生氢气,但Zn之前的金属与酸反应太快。不便操作;Zn之后的金属与酸反应太慢,花费时间太长,从经济效益和反应速率多方而考虑,Zn是最合适的金属。
金属与混合溶液的反应
(1)将一种金属单质放入几种金属的盐溶液的混合液中时,其中排在金属活动性顺序表巾最靠后的金属最先被置换出来,然后再依次置换出稍靠后的金属。简记为“在金属活动性顺序中,距离远,先反应”。如将金属Zn。放入FeSO4和CuSO4的混合溶液中,Zn先与CuSO4发生置换反应,与CuSO4反应完后再与FeSO4 发生置换反应。根据金属锌的最不同可分为以下几种情况:
| 金属锌的量 | 析出金属 | 滤液的成分 |
| 锌不足(不能与CuSO4溶液完全反应) | Cu | ZnSO4、FeSO4、CuSO4 |
| 锌不足(恰好与CuSO4溶液完全反应) | Cu | ZnSO4、FeSO4 |
| 锌不足(不能与FeSO4溶液完全反应) | Fe、Cu | ZnSO4、FeSO4 |
| 锌适量(恰好与FeSO4溶液完全反应) | Fe、Cu | ZnSO4 |
| 锌足量 | Zn、Fe、Cu | ZnSO4 |
金属与酸反应生成氢气图像问题的分析方法:
(1)等质氢图:两种金属反应产生的氢气质量相同,此图反映两种情况:

①酸不足,金属过虽,产生的氢气质量由酸的质量决定。
②酸足量,投放的两种金属与酸反应产生氢气的质量恰好相同,如6.5g锌和5.6g铁分别投入足量的盐酸中反应产生的氢气质量相同。
(2)等质等价金属图:如等质量的镁、铁、锌与足量的酸反应生成的金属离子都是+2价,产生氢气的速率和质量不同。此图反映出:

①金属越活泼,图示反应物的线越陡,如Mg线比Zn线陡,Zn线比Fe线陡,说明活泼性Mg>Zn>Fe
②金属的相对原子质量越小。等质量时,与酸反应产生的氢气越多,曲线的拐点越高,因此,相对原子质量Zn >Fe>Mg。
可简单概括为:越陡越活,越高越小。
(3)等质不等价金属图:铝、镁、锌与酸反应生成金属离子的化合价分别为+3、+2、+2,此图反映出等质不等价金属与酸反应不仅速率不同而且生成的氢气的质量与金属化合价有关。
可用下面式子计算氢气质量:


金属与酸或盐溶液反应前后溶液密度变化的判断方法:
金属与酸的反应和金属与盐溶液的反应均为置换反应,反应后溶液的溶质发生了改变,导致溶液的溶质质量分数、溶液的密度也随之改变。反应前后溶液的密度的变化取决于反应前后溶液中溶质的相对分子质量的相对大小。
(1)反应后溶液密度变小:如Fe+CuSO4== FeSO4+Cu,在该反应中,反应前溶液中的溶质为CuSO4,其相对分子质量为160;反应后溶液中的溶质为FeSO4,其相对分子质量为152,由于152<160,故该反应后溶液密度变小。
(2)反应后溶液密度变大:如Zn+H2SO4== ZnSO4+H2↑,在该反应中,反应前溶液中的溶质为H2SO4,相对分子质量为98;反应后溶液中溶质为ZnSO4,相对分子质童为161,由于161>98。故该反应后溶液密度变大。
真假黄金的鉴别:
黄金是一种具有金黄色光泽的金属、化学性质极不活泼。黄铜的外形与黄金非常相似,所以不法分子常用黄铜(Zn,Cu合金)来冒充黄金。但二者之间的性质有很大差异,可用多种方法鉴别。
方法一:取少量金黄色金属块于试管中,加入少量稀盐酸或稀硫酸,若有气泡产生(Zn+2HCl==ZnCl2 +H2),则原试样为黄铜;若没有气泡产生,则原试样为黄金。
方法二:取少量金黄色金属块,用天平称其质量,用量筒和水测出其体积,计算出金属块的密度与黄金的密度对照,若密度相等,则为黄金;若有较大的差异,则为黄铜。
方法三:取少员金黄色金属块在火焰上加热,若金属块表面变黑(2Cu+O2
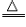 2CuO,则原试样为黄铜;若无变化,则为黄金。
2CuO,则原试样为黄铜;若无变化,则为黄金。方法四:取少讨金黄色金属块于试管中,向试管中加人适量的硫酸铜溶液,若金属块表而出现红色物质且溶液颜色变浅(Zn+CuSO4==ZnSO4+Cu),则原试样为黄铜;若无变化,则原试样为黄金。
概述:
碳是一种非金属元素,位于元素周期表的第二周期IVA族。拉丁语为Carbonium,意为“煤,木炭”。汉字“碳”字由木炭的“炭”字加石字旁构成,从“炭”字音。碳是一种很常见的元素,它以多种形式广泛存在于大气和地壳之中。碳单质很早就被人认识和利用,碳的一系列化合物——有机物更是生命的根本。碳是生铁、熟铁和钢的成分之一。碳能在化学上自我结合而形成大量化合物,在生物上和商业上是重要的分子。生物体内大多数分子都含有碳元素。
碳的存在形式:
碳的存在形式是多种多样的,有晶态单质碳如金刚石、石墨;有无定形碳如煤;有复杂的有机化合物如动植物等;碳酸盐如大理石等。单质碳的物理和化学性质取决于它的晶体结构。高硬度的金刚石和柔软滑腻的石墨晶体结构不同,各有各的外观、密度、熔点等。
碳的化学性质:
1.稳定性:在常温下碳的化学性质稳定,点燃或高温的条件下能发生化学反应
2.可燃性:
氧气充足的条件下:C+O2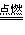 CO2
CO2
氧气不充分的条件下:2C+O2 2CO
2CO
3.还原性:
木炭还原氧化铜:C+2CuO 2Cu+CO2↑
2Cu+CO2↑
焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑
4Fe+3CO2↑
焦炭还原四氧化三铁:2C+Fe3O4 3Fe+2CO2↑
3Fe+2CO2↑
木炭与二氧化碳的反应:C+CO2 CO
CO
碳”与“炭”的区别:
“碳”是一种核电荷数为6的非金属元素,而“炭” 一般是指由石墨的微小晶体和少量杂质组成的混合物,如木炭、焦炭、活性炭、炭黑等。在说明碳元素时,用“碳”表示,如碳单质、二氧化碳、碳酸等;在说明含石墨的无定形碳时,用“炭”表示,如木炭、焦炭等。
碳燃烧生成物的判断:
氧气量充足时,碳充分燃烧:C+O2 CO2
CO2
氧气量不充足时,碳不充分燃烧:2C+O2 2CO
2CO
mg碳与ng氧气反应:
①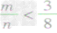 时,生成物只有CO,且O2有剩余;
时,生成物只有CO,且O2有剩余;
②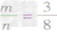 时,恰好完全反应生成CO2;
时,恰好完全反应生成CO2;
③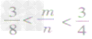 时,生成物既有CO2,也有CO;
时,生成物既有CO2,也有CO;
④ 时,恰好完全反应生成CO;
时,恰好完全反应生成CO;
⑤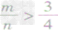 时,生成物只有CO,且C有剩余。
时,生成物只有CO,且C有剩余。
碳单质及其化合物间的转化:
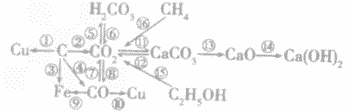
(1)C+2CuO 2Cu+CO2↑
2Cu+CO2↑
(2)C+O2 CO2
CO2
(3)3C+2Fe2O3 4Fe+3CO2↑
4Fe+3CO2↑
(4)2C+O2 2CO
2CO
(5)CO2 + H2O===H2CO3
(6)H2CO3==CO2 + H2O
(7)2CO + O2 2CO2
2CO2
(8)C+CO2 2CO
2CO
(9)3CO + Fe2O3 2Fe + 3CO2
2Fe + 3CO2
(10)CO+ 2CuO 2Cu + CO2
2Cu + CO2
(11)Ca(OH)2 + CO2====CaCO3↓+ H2O
(12)CaCO3+2HCl==CaCl2+CO2↑+H2O
(13)CaCO3 CaO+CO2
CaO+CO2
(14)CaO+H2O==Ca(OH)2
(15)C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
(16)CH4+O2 CO2+2H2O
CO2+2H2O
碳是一种非金属元素,位于元素周期表的第二周期IVA族。拉丁语为Carbonium,意为“煤,木炭”。汉字“碳”字由木炭的“炭”字加石字旁构成,从“炭”字音。碳是一种很常见的元素,它以多种形式广泛存在于大气和地壳之中。碳单质很早就被人认识和利用,碳的一系列化合物——有机物更是生命的根本。碳是生铁、熟铁和钢的成分之一。碳能在化学上自我结合而形成大量化合物,在生物上和商业上是重要的分子。生物体内大多数分子都含有碳元素。
碳的存在形式:
碳的存在形式是多种多样的,有晶态单质碳如金刚石、石墨;有无定形碳如煤;有复杂的有机化合物如动植物等;碳酸盐如大理石等。单质碳的物理和化学性质取决于它的晶体结构。高硬度的金刚石和柔软滑腻的石墨晶体结构不同,各有各的外观、密度、熔点等。
碳的化学性质:
1.稳定性:在常温下碳的化学性质稳定,点燃或高温的条件下能发生化学反应
2.可燃性:
氧气充足的条件下:C+O2
 CO2
CO2 氧气不充分的条件下:2C+O2
 2CO
2CO 3.还原性:
木炭还原氧化铜:C+2CuO
 2Cu+CO2↑
2Cu+CO2↑ 焦炭还原氧化铁:3C+2Fe2O3
 4Fe+3CO2↑
4Fe+3CO2↑ 焦炭还原四氧化三铁:2C+Fe3O4
 3Fe+2CO2↑
3Fe+2CO2↑ 木炭与二氧化碳的反应:C+CO2
 CO
CO 碳”与“炭”的区别:
“碳”是一种核电荷数为6的非金属元素,而“炭” 一般是指由石墨的微小晶体和少量杂质组成的混合物,如木炭、焦炭、活性炭、炭黑等。在说明碳元素时,用“碳”表示,如碳单质、二氧化碳、碳酸等;在说明含石墨的无定形碳时,用“炭”表示,如木炭、焦炭等。
碳燃烧生成物的判断:
氧气量充足时,碳充分燃烧:C+O2
 CO2
CO2 氧气量不充足时,碳不充分燃烧:2C+O2
 2CO
2CO mg碳与ng氧气反应:
①
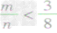 时,生成物只有CO,且O2有剩余;
时,生成物只有CO,且O2有剩余;②
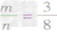 时,恰好完全反应生成CO2;
时,恰好完全反应生成CO2; ③
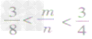 时,生成物既有CO2,也有CO;
时,生成物既有CO2,也有CO;④
 时,恰好完全反应生成CO;
时,恰好完全反应生成CO; ⑤
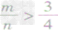 时,生成物只有CO,且C有剩余。
时,生成物只有CO,且C有剩余。 碳单质及其化合物间的转化:

(1)C+2CuO
 2Cu+CO2↑
2Cu+CO2↑ (2)C+O2
 CO2
CO2(3)3C+2Fe2O3
 4Fe+3CO2↑
4Fe+3CO2↑ (4)2C+O2
 2CO
2CO (5)CO2 + H2O===H2CO3
(6)H2CO3==CO2 + H2O
(7)2CO + O2
 2CO2
2CO2 (8)C+CO2
 2CO
2CO(9)3CO + Fe2O3
 2Fe + 3CO2
2Fe + 3CO2 (10)CO+ 2CuO
 2Cu + CO2
2Cu + CO2 (11)Ca(OH)2 + CO2====CaCO3↓+ H2O
(12)CaCO3+2HCl==CaCl2+CO2↑+H2O
(13)CaCO3
 CaO+CO2
CaO+CO2 (14)CaO+H2O==Ca(OH)2
(15)C2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O(16)CH4+O2
 CO2+2H2O
CO2+2H2O酸碱指示剂:
跟酸或碱的溶液起作用而显示不同颜色的物质,叫酸碱指示剂,通常也简称指示剂。
紫色石蕊试液和无色酚酞试液的显色:
紫色石蕊试液和无色酚酞试液是两种常用的酸碱指示剂,它们与酸性、碱性溶液作用时显示的颜色见下表:
易错点:
①变色的是指示剂,而不是酸或碱的溶液。如盐酸使紫色石蕊试液变红,不能说成紫色石蕊试液使盐酸变红,但可以说紫色石蕊试液遇盐酸变红。
②酸或碱的溶液能使紫色石蕊试液或酚酞试液变色,但能使紫色石蕊试液或酚酞试液变色的不一定是酸或碱的溶液,还可能是酸性盐溶掖或碱性盐溶液。如碳酸钠溶液能使紫色石蕊试液变蓝,但碳酸钠不是碱,而是盐。
酸碱指示剂的代用品:
在自然界里,有许多植物色素在不同的酸碱性溶液中.都会发生特定的颜色变化。这些植物色素可以用作石蕊和酚酞等指示剂的代用品。一些植物的色素及其在酸碱性溶液中的颜色变化如下:
跟酸或碱的溶液起作用而显示不同颜色的物质,叫酸碱指示剂,通常也简称指示剂。
紫色石蕊试液和无色酚酞试液的显色:
紫色石蕊试液和无色酚酞试液是两种常用的酸碱指示剂,它们与酸性、碱性溶液作用时显示的颜色见下表:
| 酸性溶液 | 碱性溶液 | 中性溶液 | |
| 石蕊试液 | 红 | 蓝 | 紫 |
| 酚酞试液 | 无 | 红 | 无 |
易错点:
①变色的是指示剂,而不是酸或碱的溶液。如盐酸使紫色石蕊试液变红,不能说成紫色石蕊试液使盐酸变红,但可以说紫色石蕊试液遇盐酸变红。
②酸或碱的溶液能使紫色石蕊试液或酚酞试液变色,但能使紫色石蕊试液或酚酞试液变色的不一定是酸或碱的溶液,还可能是酸性盐溶掖或碱性盐溶液。如碳酸钠溶液能使紫色石蕊试液变蓝,但碳酸钠不是碱,而是盐。
酸碱指示剂的代用品:
在自然界里,有许多植物色素在不同的酸碱性溶液中.都会发生特定的颜色变化。这些植物色素可以用作石蕊和酚酞等指示剂的代用品。一些植物的色素及其在酸碱性溶液中的颜色变化如下:
| 代用指示剂的颜色 | |||
| 在酸性溶液中 | 在中性溶液中 | 在碱性溶液中 | |
| 牵牛花 | 红色 | 紫色 | 蓝色 |
| 苏木 | 黄色 | 红棕色 | 玫瑰红色 |
| 紫萝卜皮 | 红色 | 紫色 | 黄绿色 |
| 月季花 | 浅红色 | 红色 | 黄色 |
| 美人蕉 | 淡红色 | 红色 | 绿色 |
发现相似题
与“下列说法中,不正确的是( )A.过量的红磷在充满空气的密闭...”考查相似的试题有:
- “金属明星”钛的获取方法之一为:TiCl4+2Mg2MgCl2+Ti,该反应属于A.分解反应B.化合反应C.置换反应D.复分解反应
- 现有X、Y、Z三种金属,已知:①X和稀硫酸不反应;②Z+H2SO4(稀)=ZSO4+H2↑;③X+2YNO3=2Y+X(NO3)2,这三种金属的活动性顺序正...
- 学过金属的活动性顺序以后,东东对其一系列知识进行了研究.(1)据下图中的实验现象判断,稀硫酸里a、b、c、d四种金属中,位...
- 下列叙述正确的是( )A.酸跟活泼金属反应一定生成盐和氢气B.金属活动顺序中,排在前面的金属一定能置换后面的金属C.单质...
- 科学家发现碳家族非常庞大,其中金刚石、石墨等是常见的碳单质.(1)金刚石和石墨物理性质存在着差异,是因为______;(2)...
- 我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和足量木炭粉加热至800℃,即可得到金光闪闪的“药金”.请回答...
- 下列关于碳单质用途的叙述中,错误的是A.用铅可制成铅笔芯B.用石墨可做干电池的电极C.用活性炭做冰箱除臭剂D.用刀头镶有...
- 下列说法正确的是( )A.紫色石蕊试液能使盐酸变红色B.氢氧化铁能使无色酚酞试液变红色C.浓硫酸沾在皮肤上用布擦去即可D....
- 某学生的化学实验报告中,有以下实验数据,其中不合理的是( )A.用托盘天平称取11.7g氧化铜粉末B.用10mL量筒量取5.26mL盐...
- 下列对于化学实验操作的叙述中,正确的是( )A.用胶头滴管滴加液体时,滴管下端紧贴试管内B.将pH试纸浸入溶液中,测定溶液...