本试题 “(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利原理____________,哪些违反了洪特规则_______________。(2)某元素的激发...” 主要考查您对电子排布式
电子云和原子轨道
泡利原理
洪特规则
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电子排布式
- 电子云和原子轨道
- 泡利原理
- 洪特规则
电子排布式:
①简化电子排布式
为了避免电子排布式书写过于繁琐,把内层电子达到稀有气体元素原子结构的部分以相应稀有气体的冗素符号外加方括号表示,即为简化电子排布式,如K 的简化电子排布式为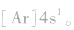
②特殊电子排布式
有个别元素的基态原子的电子排布对于构造原理有1个电子的反常。因为能量相同的原子轨道在全充满( )、半充满(
)、半充满(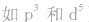 )和全空(
)和全空(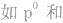
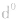 )状态时,体系的能量较低,原子较稳定。
)状态时,体系的能量较低,原子较稳定。 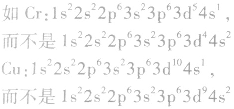
(2)电子排布图:用方框表示一个原子轨道,用箭头“↑”或“↓”来区别自旋状态不同的电子。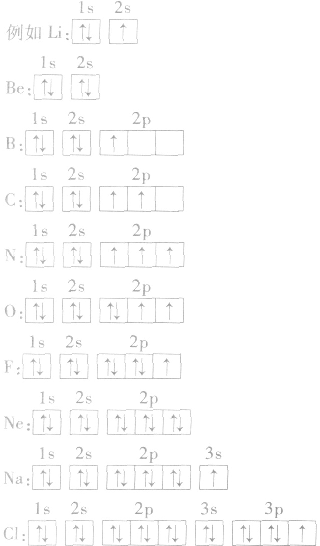
构造原理:
多电子原子的核外电子排布总是按照能量最低原理,由低能级逐步填充到高能级。绝大多数元素的原子核外电子的排布遵循下图所示的排布顺序,这种排布顺序被称为构造原理。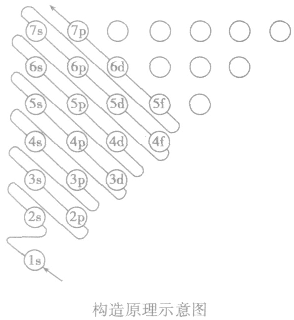
点拨:构造原理中的排布顺序,其实质是各能级的能量高低顺序,可由下列公式得出ns<(n一2)f< (n一1)d<np(n表示能层序数)。常用的重要的能级交错顺序有: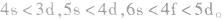
核外电子排布式一构造原理的应用:
根据构造原理,按照能级顺序,用能级符号右上角的数字表示该能级上电子数的式子,叫做电子排布式。例如,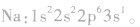
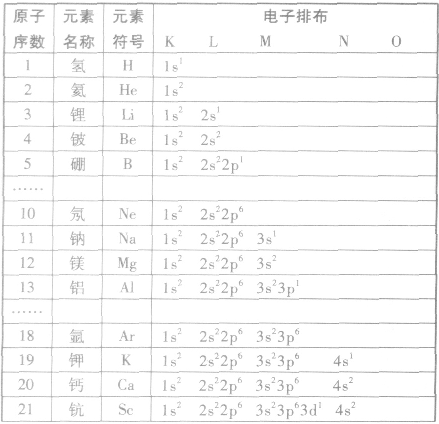
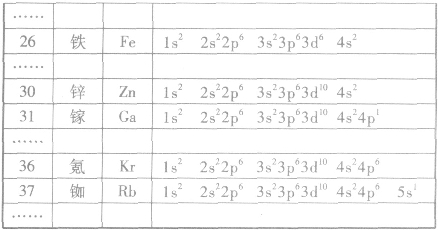
核外电子运动状态:
核外电子的运动特征核外电子的质量很小,运动空间小,但运动速度却很大,接近光速。
由于电子的绕核运转是高速的、无规律的,因此我们无法预测电子在某一时刻的位置,只能预测电子在某一区域内出现几率的大小。
现代量子力学指出,核外电子的运动不能像经典力学中确定宏观物体的运动状态那样,同时用位置和速度的物理量来准确描述它的运动状态,而只能确定它在原子核外各处出现的概率。
电子云:
由于核外电子的概率密度分布看起来像一片云雾,因而被形象地称作电子云。换句话说,电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述。
电子云密度大的地方,表明电子在核外空间单位体积内出现的机会多;电子云密度小的地方,表明电子在核外空间单位体积内出现的机会少。
原子轨道:
(1)定义:量子力学把电子在原子核外的一个空间运动状态称为一个原子轨道。
(2)原子轨道的形状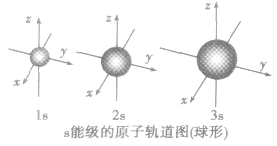
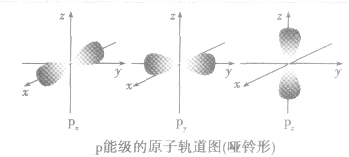
在原子中不能容纳运动状态完全相同的电子。又称泡利原理、不相容原理引。
一个原子中不可能有电子层、电子亚层、电子云伸展方向和自旋方向完全相同的两个电子。如氦原子的两个电子,都在第一层(K层),电子云形状是球形对称、只有一种完全相同伸展的方向,自旋方向必然相反。每一轨道中只能容纳自旋相反的两个电子,每个电子层中可能容纳轨道数是n2个、每层最多容纳电子数是2n2个。
在相同能量的原子轨道上,电子的排布将尽可能占据不同的轨道,而且自旋方向相同,即为洪特规则,又称为最多轨道原理。
一般:电子总是尽先自旋平行地分占不同轨道。如:
碳原子的轨道表示是:
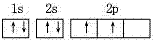 ,而不是
,而不是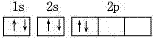
特别提醒:等价轨道全空(p0、d0、f0)和全满时(p6、d10、f14)的结构,也具有较低能量和较大的稳定性。像铁离子Fe3+(3d5)和亚铁离子Fe2+(3d6)对比看,从3d6→3d5才稳定,这和亚铁离子不稳定易被氧化的事实相符合。根据洪特规则铬的电子排布式应为 1s22s22p63s23p63d54s1。
与“(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。...”考查相似的试题有:
- 基态原子电子排布为1s22s22p63s23p1的元素最可能的价态是( )A.+1B.+2C.+3D.-1
- 有Xn-、Yn+、Z三种粒子,其核外电子层结构相同,则下列分析中不正确的是( )A.粒子半径大小的关系是Xn->Yn+、X<YB.Z是稀...
- 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B...
- 某元素原子的最外层电子数为次外层电子数的3倍,则该元素原子核内质子数为( )A.3B.7C.8D.10
- 下列属于离子化合物且阴阳离子核外电子排布相同的是( )A.K2SB.NaClC.MgBr2D.SCl2
- 下列叙述正确的是( )A.在原子核外电子排布中,当M层是最外层时,该层最多只能排布8个电子B.电子的能量越低,运动区域离核...
- 有E、Q、T、X、Z五种前四周期元素,原子序数E2+与ET2互为等电子体。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。...
- 下列关于价电子构型为3s23p4的粒子描述正确的是[ ]A.它的元素符号为OB.它的核外电子排布式为1s22s22p63s23p4C.它可与H2生...
- 已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电...
- 设X、Y、Z代表三种元素。已知:①X+和Y-两种离子具有相同的电子层结构;②Z元素原子核内质子数比Y元素原子核内质子数少9个;③Y...