本试题 “(6分)某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞(B)...” 主要考查您对水的离子积常数
水电离的影响因素
水的电离平衡
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 水的离子积常数
- 水电离的影响因素
- 水的电离平衡
水的电离:
水是一种极弱的电解质,它能微弱地电离:
实验测得:25℃时,1L纯水中只有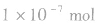 的水分子发生电离,故25℃时纯水中
的水分子发生电离,故25℃时纯水中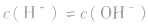

水的离子积:
在一定温度下,水电离出的c(H+)与c(OH-)的乘积是一个常数,称为水的离子积常数,简称水的离子积,用符号 表示,即
表示,即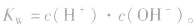
(1)在一定温度下,水的离子积都是一个常数,在25℃时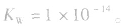
(2)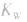 随温度的变化而变化,温度升高,
随温度的变化而变化,温度升高,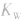 增大。
增大。
(3)水的离子积常数揭示了在任何水溶液中均存在水的电离平衡,都有 存在。在酸性或碱性的稀溶液中,当温度为25℃时,
存在。在酸性或碱性的稀溶液中,当温度为25℃时,
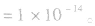
(4)在酸或碱的稀溶液中,由水电离出的c(H+)和c(OH-)总相等.即 如25℃时
如25℃时 或NaOH溶液中,
或NaOH溶液中,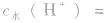
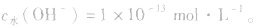
溶液中c(H+)或c(OH-)的计算:
常温下,稀溶液中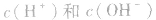 的乘积总是
的乘积总是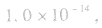 知道
知道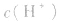 就可以计算出
就可以计算出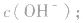 反之亦然
反之亦然
1.酸溶液
当在水中加入酸后,将使水的电离平衡向左移动 (抑制水的电离)。在酸的水溶液中,H+主要由酸电离产生,即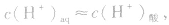 而OH-是由水电离产生的:
而OH-是由水电离产生的: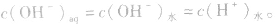
2.碱溶液
同理,在碱的水溶液中,OH-主要由碱电离产生,即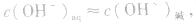 而H+是由水电离产生的:
而H+是由水电离产生的: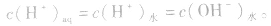
3.盐溶液
在盐的水溶液中,H+和OH-全部来自水的电离,且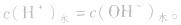
(1)若单一水解的盐的水溶液呈酸性,c(H+)> c(OH-),即弱碱阳离子水解


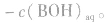
(2)若单一水解的盐的水溶液呈碱性,c(OH一)> c(H+),即弱酸阴离子水解
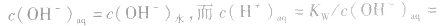
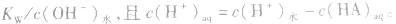
说明:由以上分析可以看出,在常温下(25℃):
酸(或碱)的溶液中,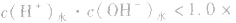
 发生水解的盐溶液中
发生水解的盐溶液中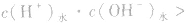
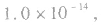 但
但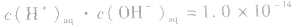 总成立。
总成立。
影响水电离平衡的因素:
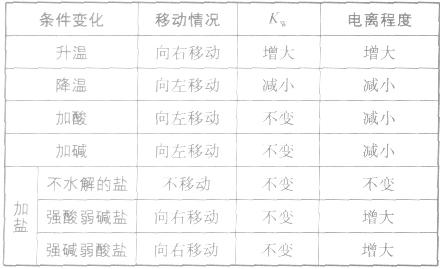
水的电离:
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O
 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L 注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
发现相似题
与“(6分)某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其...”考查相似的试题有:
- 以酚酞试液为指示剂,对某新制的NaOH溶液进行中和滴定实验,数据记录如下表:该新制NaOH溶液的浓度c计算最合理的是A.c=0.10...
- 能使水的电离平衡右移,且水溶液显碱性的离子是( )A.H+B.OH-C.Al3+D.HCO3-
- 能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是[ ]①将水加热②向水中投入一小块金属钠③向水中通CO2④向水中加入明矾晶体⑤向...
- 根据所学化学反应原理填空:(1)升高温度时,水的pH______(填“增大”“减小”或“不变”)(2)体积、pH均相同的盐酸和醋酸溶液...
- 在①、②、③、④四条曲线中,能正确表示将一定浓度的NaOH溶液加水稀释,其pH与加水的体积(V)的关系的是A.①B.②C.③D.④
- (7分) t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:(1)该温度下,水的离子积常数kw= 。(2...
- 某Na2CO3溶液的pH可能是A.5B.6 C.7D.8
- 在水中加入下列物质,可以促进水电离的是( )A.H2SO4B.NaOHC.Na2CO3D.KNO3
- 有关水的电离平衡的说法正确的是[ ]A.水的离子积通常用 来表示,随温度变化而变化,只适用于纯水,在稀盐酸中数值会变大B....
- 下列叙述正确的是( )A.90℃纯水的pH<7,说明加热可导致水呈酸性B.将稀氨水逐滴加入稀盐酸中,当溶液的pH=7时,c(Cl-)>...