本试题 “于下列各装置图的叙述中,正确的是[ ]A.实验室用装置①制取氨气B.装置②可用于制备氢氧化亚铁并观察其颜色C.装置③中X若为四氯化碳,可用于吸收氨气,并防止...” 主要考查您对原电池原理
氨气的制取
尾气的吸收
氢氧化亚铁的制备
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原电池原理
- 氨气的制取
- 尾气的吸收
- 氢氧化亚铁的制备
原电池:
1.定义:将化学能转化为电能的装置。
2.工作原理:
以铜-锌原电池为例
(1)装置图:
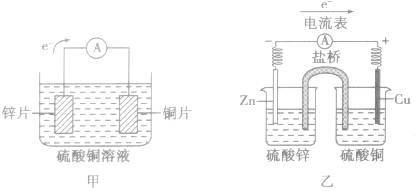
(2)原理图:
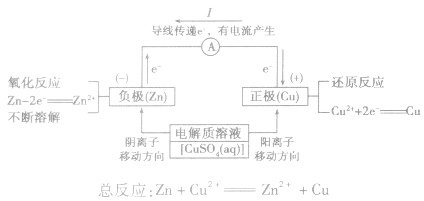
3.实质:化学能转化为电能。
4.构成前提:能自发地发生氧化还原反应。
5.电极反应:
负极:失去电子;氧化反应;流出电子
正极:得到电子;氧化反应;流入电子
6.原电池正负极判断的方法:
①由组成原电池的两级材料判断,一般是活泼金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②根据电流方向或电子流动方向判断,电流是由正极流向负极,电子流动方向是由负极流向正极。
③根据原电池里电解质溶液内离子的定向移动方向,在原电池的电解质溶液中,阳离子移向正极,阴离子移向负极。
④根据原电池两级发生的变化来判断,原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
⑤X极增重或减重:X极质量增加,说明溶液中的阳离子在X极(正极)放电,反之,X极质量减少,说明X极金属溶解,X极为负极。
⑥X极有气泡冒出:发生可析出氢气的反应,说明X极为正极。
⑦X极负极pH变化:析氢或吸氧的电极发生反应后,均能使该电极附近电解质溶液的pH增大,X极附近的pH增大,说明X极为正极。
1.定义:将化学能转化为电能的装置。
2.工作原理:
以铜-锌原电池为例

(1)装置图:

(2)原理图:

3.实质:化学能转化为电能。
4.构成前提:能自发地发生氧化还原反应。
5.电极反应:
负极:失去电子;氧化反应;流出电子
正极:得到电子;氧化反应;流入电子
6.原电池正负极判断的方法:
①由组成原电池的两级材料判断,一般是活泼金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②根据电流方向或电子流动方向判断,电流是由正极流向负极,电子流动方向是由负极流向正极。
③根据原电池里电解质溶液内离子的定向移动方向,在原电池的电解质溶液中,阳离子移向正极,阴离子移向负极。
④根据原电池两级发生的变化来判断,原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
⑤X极增重或减重:X极质量增加,说明溶液中的阳离子在X极(正极)放电,反之,X极质量减少,说明X极金属溶解,X极为负极。
⑥X极有气泡冒出:发生可析出氢气的反应,说明X极为正极。
⑦X极负极pH变化:析氢或吸氧的电极发生反应后,均能使该电极附近电解质溶液的pH增大,X极附近的pH增大,说明X极为正极。
原电池中的电荷流动:
在外电路(电解质溶液以外),电子(负电荷)由负极经导线(包括电流表和其他用电器)流向正极,使负极呈正电性趋势、正极呈负电性趋势。在内电路(电解质溶液中),阳离子(带正电荷)向正极移动,阴离子 (带负电荷)向负极移动。这样形成了电荷持续定向流动,电性趋向平衡的闭合电路。
(1)实验室用氢氧化钙和氯化铵制取氨气
2NH4Cl+Ca(OH)2 CaCl2+2NH3+2H2O
CaCl2+2NH3+2H2O
(2)仪器:铁架台,铁夹,酒精灯,两个大试管,棉花;氯化铵固体,氢氧化钙固体。
(3)装置图: 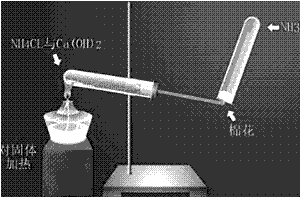
(4)注意:
a. 一般用Ca(OH)2,而不用NaOH,因NaOH碱性太强,对大试管腐蚀比Ca(OH)2强。
b. 选用Ca(OH)2时要检验消石灰是否变质, 因经过长期存放后消石灰部分变成碳酸钙,最好用新制的消石灰。
c. NH4CL与Ca(OH)2质量比5:8为宜,如用(NH4)2SO4代替NH4CL,则质量比为1:1,消石灰过量,以防止生成氨合物。
d. 试管口(盛固体药品的试管)要略向下倾斜;
e. 固体药品要平铺试管底部;
f.导出氨气的导管要短,收集氨气的导管要长,伸入试管底部;
g.为使氨气收集更多,防止空气中的水蒸汽进入收集氨气的试管,在试管口防一块,但不能堵死
h.酒精灯加热用外焰,先均匀加热,后对固体加热。
(5)收集方法: 用向下排气法取气法收集。因氨气极易溶于水,比空气轻。
干燥氨气: 用碱石灰,不能用浓硫酸和氯化钙干燥氨气。
检验氨气:用湿润的红色石蕊试纸,氨气能使湿润的红色石蕊试纸变蓝。
尾气的处理方法:
1.对于极易溶于水的尾气,如NH3、HCl、HBr等,可采用防倒吸装置(如在导气管的出气口处连接一倒置的漏斗与吸收剂液面接触)吸收.
2.对于溶解度不大的尾气,如Cl2、CO2等,可直接将出气管插入吸收剂液面下吸收。
3.对于有毒且易燃的气体,如(CO等,可在尾气出口处放置一点燃的酒精灯,使CO燃烧转变为无毒的CO2气体。
尾气处理装置:
(1)直接吸收
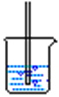
(2)燃烧处理或袋装

1.对于极易溶于水的尾气,如NH3、HCl、HBr等,可采用防倒吸装置(如在导气管的出气口处连接一倒置的漏斗与吸收剂液面接触)吸收.
2.对于溶解度不大的尾气,如Cl2、CO2等,可直接将出气管插入吸收剂液面下吸收。
3.对于有毒且易燃的气体,如(CO等,可在尾气出口处放置一点燃的酒精灯,使CO燃烧转变为无毒的CO2气体。
尾气处理装置:
(1)直接吸收

(2)燃烧处理或袋装

氢氧化亚铁的制备:
在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等制备。
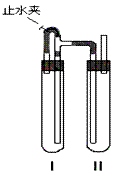
(1)在试管I里加入稀H2SO4和铁屑;
(2)II中的试剂加入前应煮沸;
(3)为了制得白色Fe(OH)2沉淀,在试管I和II中加入试剂,打开止水夹,塞紧塞子后稍等片刻后关闭止水夹;
(4)试管Ⅰ中反应生成的H2充满了试管Ⅰ和试管Ⅱ,且外界空气不易进入,这样生成的Fe(OH)2沉淀能较长时间保持白。
在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等制备。

(1)在试管I里加入稀H2SO4和铁屑;
(2)II中的试剂加入前应煮沸;
(3)为了制得白色Fe(OH)2沉淀,在试管I和II中加入试剂,打开止水夹,塞紧塞子后稍等片刻后关闭止水夹;
(4)试管Ⅰ中反应生成的H2充满了试管Ⅰ和试管Ⅱ,且外界空气不易进入,这样生成的Fe(OH)2沉淀能较长时间保持白。
发现相似题
与“于下列各装置图的叙述中,正确的是[ ]A.实验室用装置①制取氨...”考查相似的试题有:
- 根据下图,下列判断中正确的是( )A.烧杯a中的溶液pH升高B.烧杯b中发生氧化反应C.烧杯a中发生的反应为2H++2e-=H2D.烧杯...
- 图中,两电极上发生的电极反应分别为:a极:2Ag++2e-=2Ag b极:Fe-2e-=Fe2+下列说法不正确的是( )A.该装置一定是电解池B....
- 关于原电池和电解池的叙述正确的是[ ]A.原电池中失去电子的电极为阴极B.原电池的负极、电解池的阳极都发生氧化反应C.原电...
- 观察下图装置,其中a、b是两根石墨棒,有关电极反应式错误的是A.a电极:2Cl-—2e—=Cl2↑B.b电极:2H++2e—=H2↑C.铜电极:2H++...
- 在用Zn、Cu片和CuSO4溶液组成的原电池装置中,经过一段时间工作后,下列说法中正确的是 A.锌片是正极,铜片质量不变B.电流...
- 下图是用来说明金属的吸氧腐蚀的简易装置,有关此装置的叙述中错误的是( )A.铁片为负极,碳棒为正极B.铁被腐蚀,碳棒上有...
- 下列事实不能用原电池理论解释的是[ ]A、铝片不用特殊方法保存B、生铁比纯铁易生锈C、制氢气时用粗锌而不用纯锌D、工程施工队...
- [I]下列有关仪器的名称、图形、用途及使用操作的叙述均正确的是______:ABCD名称250ml容量瓶分液漏斗酸式滴定管温度计(量程1...
- 氯气和氨气在常温下混合即可发生反应。某兴趣小组同学为探究纯净、干燥的氯气与氨气的反应,设计了如下装置请回答:(1)装置F...
- 下列实验操作正确的是( )A.制氨气B.收集CO2或NOC.配制稀硫酸D.氨气的吸收