本试题 “化学能和电能的相互转化,是能量转化的重要方式之一,下图两个实验装置是实现化学能和电能相互转化的装置。(1)把化学能转化为电能的装置是_______(填“甲”...” 主要考查您对原电池电极反应式的书写
原电池原理
电解池电极反应式的书写
电解饱和氯化钠溶液
气体的检验
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原电池电极反应式的书写
- 原电池原理
- 电解池电极反应式的书写
- 电解饱和氯化钠溶液
- 气体的检验
(1)以铜锌原电池为例:
负极(Zn):Zn-2e-=Zn2+
正极(Cu):2H++2e-=H2↑
(2)正负极反应式的书写技巧:
①先确定原电池的正负极,在两极的反应物上标出相同数目的电子得失。
②根据物质放电后生成物的组成和电解质溶液中存在的离子,找到电极反应中还需要的其它离子。此时要注意溶液的酸碱性,从而判断应该是H+、OH-还是H2O参与了反应。因Zn反应后生成了Zn(OH)2,而KOH为电解质,可知负极上OH-参与了反应。MnO2生成了MnO(OH),即增加了氢元素,可知正极上有水参与了反应。
③根据电子守恒和电荷守恒写出电极反应式,即要注意配平和物质的正确书写形式,应按照离子方程式的书写要求进行。②中反应的电极反应式为:
负极:Zn+2OH--2e-=Zn(OH)2 正极:2MnO2+2H2O+2e-=2MnO(OH)+2OH-
(若只要求写正极的反应式,也可以写成MnO2+H2O+e-=MnO(OH)+OH-)
原电池总反应式的书写:将正负电极反应相加,即为原电池总反应式。
原电池正、负极的判断方法:
原电池有两个电极,一个是正极,一个是负极,判断正极和负极的方法有以下几种。
1.由组成原电池的两极材料判断一般相对较活泼的金属为负极,相对不活泼的金属或能导电的非金属为正极。
2.根据电流方向或电子流动方向判断在外电路,电流由正檄流向负极;电子由负极流向正极
3.根据原电池里电解质溶液中离子的定向移动方向判断在原电池的电解质溶液内,阳离子移向正极,阴离子移向负极。
4.根据原电池两极发生的变化来判断原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
5.X极增重或减轻工作后,X极质量增加,说明X极有物质析出,X 极为正极:反之,X极质量减少,说明X极金属溶解,X 极为负极
6.X极有气泡冒出工作后,x极上有气泡冒出,一般是发生了析出H,的电极反应,说明x极为正极。
7.X极附近pH的变化析氢或吸氧的电极反应发生后,均能使该电极附近电解质溶液的pH增大,因而工作后,X极附近pH增大了,说明X极为正极。
8.特例在判断金属活泼性的规律中,有一条为“当两种金属构成原电池时,活泼金属作负极,不活泼金属作正极”,但这条规律也有例外情况,如Mg和Al为原电池的两极,KOH为电解质溶液时,虽然Mg比Al活泼,但因Mg不和KOH反应,所以Mg作原电池的正极等。
1.定义:将化学能转化为电能的装置。
2.工作原理:
以铜-锌原电池为例

(1)装置图:
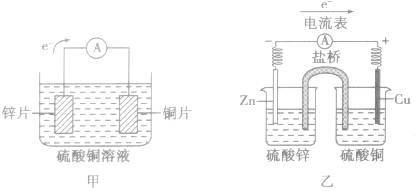
(2)原理图:
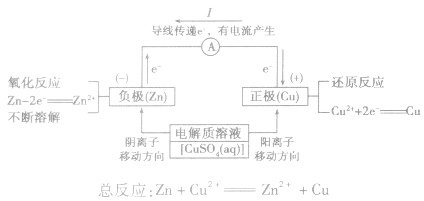
3.实质:化学能转化为电能。
4.构成前提:能自发地发生氧化还原反应。
5.电极反应:
负极:失去电子;氧化反应;流出电子
正极:得到电子;氧化反应;流入电子
6.原电池正负极判断的方法:
①由组成原电池的两级材料判断,一般是活泼金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②根据电流方向或电子流动方向判断,电流是由正极流向负极,电子流动方向是由负极流向正极。
③根据原电池里电解质溶液内离子的定向移动方向,在原电池的电解质溶液中,阳离子移向正极,阴离子移向负极。
④根据原电池两级发生的变化来判断,原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
⑤X极增重或减重:X极质量增加,说明溶液中的阳离子在X极(正极)放电,反之,X极质量减少,说明X极金属溶解,X极为负极。
⑥X极有气泡冒出:发生可析出氢气的反应,说明X极为正极。
⑦X极负极pH变化:析氢或吸氧的电极发生反应后,均能使该电极附近电解质溶液的pH增大,X极附近的pH增大,说明X极为正极。
原电池中的电荷流动:
在外电路(电解质溶液以外),电子(负电荷)由负极经导线(包括电流表和其他用电器)流向正极,使负极呈正电性趋势、正极呈负电性趋势。在内电路(电解质溶液中),阳离子(带正电荷)向正极移动,阴离子 (带负电荷)向负极移动。这样形成了电荷持续定向流动,电性趋向平衡的闭合电路。
1.根据装置书写电极反应式
(1)根据电源确定阴、阳两极→确定阳极是否是活性电极→据电极类型及电解质溶液中阴、阳离子的放电顺序写出电极反应式。
(2)在确保阴、阳两极转移电子数目相同的条件下,将两极电极反应式合并即得总反应式。
2.由氧化还原反应方程式书写电极反应式
(1)找出发生氧化反应和还原反应的物质→确定两极名称和生成物→利用电子守恒分别写出两极反应式。
(2)若写出一极反应式,而另一极反应式不好写,可用总反应式减去已写出的电极反应式,即得另一电极反应式。
在小烧杯(或U型管)里装入饱和食盐水,滴入几滴酚酞试液。用导线把碳棒、电池、电流表和铁钉相连(如图)。接通直流电源后,注意观察电流表的指针是否偏转,以及小烧杯内发生的现象,并用湿润的碘化钾淀粉试纸检验阳极放出的气体。
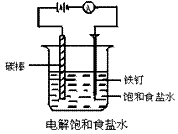
注:粗铁钉要与直流电源的阴极相连,碳棒与阳极相连。
用玻璃棒沾湿润的KI淀粉试纸检验阳极气体。
(1)饱和食盐水电解时,电流表指针发生偏转,阴、阳极均有气体放出,阳极气体有刺激性气味,并能使湿润的KI淀粉试纸变蓝,且阴极区溶液变红。
(2) 阳极:2Cl--2e-==Cl2↑
阴极:2H++2e-==H2↑(或2H2O+2e-==2OH-+H2↑)
总反应式:2NaCl+2H2O
 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑ (3)阴极区溶液变红的原因:这是由于饱和食盐水中,水所电离出的H+在阴极放电,破坏了水的电离平衡
(H2O
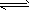 H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。
H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。 (4)例用电解饱和食盐水溶液可制取氢气、氯气和烧碱。
(1)观察法:对于特殊颜色的气体如Cl2(黄绿色)、NO2(红棕色)、碘蒸气(紫红)可据此辨之。
(2)溶解法:根据溶于水的现象不同区分,如NO2和溴蒸气均为红棕色,但溶于水后NO2形成无色溶液;溴形成橙色溶液。
(3)褪色法:SO2和CO2可用品红溶液区分。
(4)氧化法:被空气氧化看变化,如NO的检验。
(5)试纸法:如石蕊试纸、醋酸铅试纸。
(6)星火发:适用于有助燃性或可燃性的气体检验,如O2使带火星木条复燃;CH4和C2H2的检验可点燃看现象;CH4、CO、H2则可根据其燃烧产物来判断。
常见气体的检验:
(1)H2:无色、无味、可燃;①不纯点燃发出爆鸣声;②点燃纯H2,火焰呈淡色,火焰上方罩一干燥烧杯,烧杯壁上有水珠生成:2H2+O2
 2H2O
2H2O (2)O2:无色无味、能使余烬木条复燃;
(3)Cl2:黄绿色刺激性气体有毒;①使湿润淀粉碘化钾试纸变蓝:Cl2+2KI=2KCl+I2 I2遇淀粉变蓝;②使湿润蓝色石蕊试纸先变红后变白:Cl2+H2O=HCl+HClO HClO强氧化性漂白作用;
(4)CO2:无色无味无毒;①使燃着木条熄灭;②通入澄清石灰水变浑浊:CO2+Ca(OH)2=CaCO3↓+H2O
(5)CO:无色、无味、剧毒;点燃火焰呈蓝色,火焰上方罩一沾有石灰水液滴的烧杯,液滴变浑浊:
2CO+O2
 2CO2 CO2+Ca(OH)2=CaCO3↓+H2O
2CO2 CO2+Ca(OH)2=CaCO3↓+H2O (6)NO2: 红棕色气体有刺激性气味、有毒,溶于水、水溶液呈酸性,能使紫色石蕊试液变红:3NO2+H2O=2HNO3+NO
(7)NO:无色气体有毒;在空气中立即变为红棕色:2NO+O2=2NO2
(8)N2: 无色无味无毒;能使燃着木条熄灭。
(9)SO2:无色有刺激性气味、有毒;①通入品红溶液,品红褪色加热又恢复颜色;②使澄清石灰水变浑浊:
SO2+Ca(OH)2=CaSO3+H2O;
③使酸性高锰酸钾溶液褪色:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+
(10)HCl:无色刺激性气味;①能使湿润蓝色石蕊试纸变红:HCl=H++Cl-; ②用蘸浓氨水玻璃棒靠近冒白烟:NH3+HCl=NH4Cl;③气体通入HNO3酸化的AgNO3溶液,有白色沉淀生成:HCl+AgNO3=AgCl↓+HNO3 (AgCl不溶于HNO3)
(11)H2S:无色臭鸡蛋气味有毒;遇Pb(NO3)2 、(CH3COO)2Pb、CuSO4溶液均产生黑色沉淀:Pb2++H2S=PbS↓+2H+;2CH3COO-+Pb2++H2S=PbS↓+2CH3COOH;Cu2++H2S=CuS↓+2H+
(12)NH3:无色刺激性气味;①遇湿润红色石蕊试纸变蓝:NH3+H2O
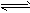 NH3?H2O
NH3?H2O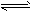 NH4++OH-;②用蘸浓盐酸玻璃棒靠近冒白烟:NH3+HCl==NH4Cl
NH4++OH-;②用蘸浓盐酸玻璃棒靠近冒白烟:NH3+HCl==NH4Cl (13)CH4:无色无味、可燃;点燃后火焰呈浅蓝色,火焰上方罩一干燥烧杯,烧杯壁上有水珠罩生成;罩一沾有石灰水液滴的烧杯,液滴变浑浊:CH4+2O2
 CO2+2H2O CO2+Ca(OH)2==CaCO3↓+H2O
CO2+2H2O CO2+Ca(OH)2==CaCO3↓+H2O (14)C2H4: 无色稍有气味;①点燃,火焰明亮(少量黑烟):C2H4+3O2
 2CO2+2H2O ;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH2=CH2+Br2→CH2Br-CH2Br
2CO2+2H2O ;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH2=CH2+Br2→CH2Br-CH2Br (15)C2H2:无色无味;①点燃火焰明亮并伴有大量黑烟:2C2H2+5O2
 4CO2+2H2O;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH≡CH+2Br2→CHBr2-CHBr2
4CO2+2H2O;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH≡CH+2Br2→CHBr2-CHBr2 物质检验的基本原则:
物质检验的“三个原则”,即一看(颜色、状态)、二嗅(气味)、三实验(加试剂)。根据实验时生成物所表现的现象不同,检验离子的方法可归纳为四类:
(1)生成气体,如 的检验;
的检验;
(2)生成沉淀,如 的检验;
的检验;
(3)显现特殊颜色,如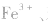 苯酚的检验。
苯酚的检验。
(4)焰色反应:检验金属或金属离子。
与“化学能和电能的相互转化,是能量转化的重要方式之一,下图两...”考查相似的试题有:
- 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池...
- 依据氧化还原反应:2Ag+(aq)+ Cu(s)===Cu2+(aq) +2Ag(s)设计的原电池如图所示。请回答下列问题:(1)电极X的材料是____;电...
- 如下图由浓硫酸、Cu、Al组成一个原电池,试写出正、负极电极反应式,并指出反应类型。负极:_______________;____________;正...
- 甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如下图。下列有关叙述正确的是A.H+从正极区通过交换...
- 如图为一原电池装置,下列叙述中正确的是( )A.铜是阳极,铜片上有气泡产生B.盐桥中的K+移向ZnSO4溶液C.电流从锌片经导线...
- 原电池产生电流的本质原因是[ ]A.原电池中溶液能电离出自由移动的离子B.有导线将两个活泼性不同的电极连接C.正极发生了氧...
- 如图,将纯Fe棒和石墨棒插入1L 1.0mol/L的NaCl溶液中.下列说法正确的是( )A.去掉电源,a与b直接连接,则Fe棒上产生气泡B...
- 如图电解池中装有硫酸铜溶液,选用不同材料的电极进行电解。下列说法正确的是( )
- 以石墨做阳极,铁网做阴极,用离子隔膜法电解饱和食盐水。请回答下列问题:(1)写出在电解过程中,与电源正极相连的电极上的...
- 现有五种短周期元素的性质、用途或原子结构信息如下表请根据表中信息回答下列问题:(1)Q气态氢化物分子的空间构型为_________...