本试题 “化学上常用燃烧法确定有机物的组成。下图装置是用燃烧法确定有机物化学式常用的装置,这种方法是在电炉加热时用纯氧氧化管内样品。根据产物的质量确定有机物...” 主要考查您对有机物燃烧确定其组成
测定物质组成、成分含量
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 有机物燃烧确定其组成
- 测定物质组成、成分含量
有机物燃烧确定其组成:
有机物完全燃烧后,各元素对应产物为:C→CO2,H→H2O,Cl→HCl。因此,我们可以根据有机物燃烧的产物分析判断该有机物的组成。
(1)某有机物完全燃烧后:若产物只有CO2和H2O,则其组成元素可能为C、H或C、H、O。欲判定该有机物中是否含氧元素,首先求出CO2中碳元素的质量及H2O中氢元素的质量,然后将碳、氢元素的质量之和与原来有机物质量相比较,若两者相等,则原有机物的组成中不含氧,否则,原有机物的组成中含氧。生成的CO2和H2O的关系有:
①生成的CO2和H2O的体积比为1∶1的有:若为烃,则属于环烷烃或烯烃;若为烃的衍生物,则为醛、酮、羧酸、酯、葡萄糖、果糖等。
②生成的CO2和H2O的体积比为1∶2的有:甲烷、甲醇和尿素等含一个碳原子和四个氢原子的物质。
③生成的CO2和H2O的体积比为2∶1的有:分子中碳、氢原子数相同的物质,如:乙炔、苯、苯乙烯、苯酚等。
④当不同的有机物的物质的量相同时,此时有机物可写成:CxHy(H2O)n或CxOy(H2O)n的形式,耗氧只能由前一部分CxHy或CxOy完成,后面部分在燃烧过程中不耗氧。则组成为CxHy(H2O)n,每摩尔耗氧(x+y/4)mol;组成为CxOy(H2O)n的物质,每摩尔耗氧(x-y/2)mol;
特例:组成符合CxHy(H2O)n的物质中CH2O耗氧最少;组成符合CxOy(H2O)n的物质中,乙二醛耗氧最少。
(2)质量之和不变的两种有机物的燃烧规律:A、B两种有机物,不论以何种质量比进行混合,只要总质量保持一定,则完全燃烧时耗氧量与生成的CO2和H2O的量之间的关系说明:
①若生成的CO2量不变,则分二种情况:A、B的相对分子质量相同时,两者必为同分异构体;另一种情况是:A、B的相对分子质量不同时,则两者中的碳元素的质量分数必然相等,如:HCHO与CH3COOH;C16H34与C16H18O等
②若生成的H2O的量不变,也分二种情况:A、B的相对分子质量相同时,两者必为同分异构体;第二种情况是:A、B的相对分子质量不同时,则两者中的氢元素的质量分数必然相等,如:C2H2与C6H6、C8H8;C10H8与C6H8O3等
③若生成的CO2和H2O的量不变,也分二种情况:A、B的相对分子质量相同时,两者必为同分异构体;第二种情况是:A、B的相对分子质量不同时,则两者中的碳、氢元素的质量分数必然相等,即两者具有相同的最简式如:CH2O与C2H4O2、C3H6O3、C6H12O6等
(3)物质的量之和不变的两种有机物完全燃烧规律:A、B两种有机物,不论以何种比例进行混合,只要总物质的量保持一定,则完全燃烧时耗氧量与生成的CO2和H2O的量之间的关系说明:
①若A、B两者互为同分异构体时,相对分子质量相同,此时无论怎样混合,完全燃烧后消耗的氧气和生成的CO2和H2O的量都保持不变,这一点我们就不再考虑
②若生成的CO2的物质的量不变:A、B的相对分子质量不同时,则两者中的碳原子数必然相等,如:C2H4与C2H4O、C2H4O2等
③若生成的H2O的物质的量不变:A、B的相对分子质量不同时,则两者中的氢原子数必然相等,如:CH4、CH4O、C2H4O、C2H4O2等
④若生成的CO2和H2O的量不变:A、B的相对分子质量不同时,则两者中的碳、氢原子数都相等,如:CH4、CH4O;C2H4、C2H4O、C2H4O2等
⑤若消耗的氧气和生成的CO2的量保持不变:A、B的相对分子质量不同时,两者含碳原子数必相等,分子中必相差n个H2O,如:C2H4与C2H6O。
(6)若消耗的氧气和生成的H2O的量保持不变:A、B的相对分子质量不同时,则两者含氢原子数必相等,分子中必相差n个CO2,如:CH4与C2H4O2。
⑦若在反应过程中消耗氧的物质的量保持不变:A、B的相对分子质量不同时,若两者含碳原子数相等,则分子中必相差n个H2O,如:C2H4与C2H6O。而当两者的氢原子数相等时,则分子中必相差n个CO2,如:CH4与C2H4O2。
定量实验介绍:

燃烧法测定氨基酸的组成:
实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现按下图所示装置进行实验。

①实验开始时,首先要通入一段时间的氧气,目的是排除体系中的N2。
②D装置的作用是吸收未反应的O2,保证最终收集的气体是N2。
③读取N2体积时,应注意:量筒内液面与广口瓶中的液面相持平视线与凹液面最低处相切。
④实验中测得N2的体积为VmL(已折算为标准状况)。为确定此氨基酸的分子式,还需要的有关数据为生成二氧化碳气体的质量、生成水的质量、氨基酸的相对分子质量
用氨气还原氧化铜的方法测定铜的近似相对原子质量:
实验室用氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为:2NH3+3CuO
 N2+3Cu+3H2O
N2+3Cu+3H2O(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。
装置图:
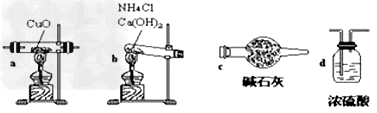
①连接顺序为:bcacd
②d中浓硫酸的作用是吸收未反应的氨、防止空气中水分进入;实验完毕时观察到a中的现象是固体由黑色转变为红色;
③Cu的相对原子质量的表达式
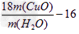
与“化学上常用燃烧法确定有机物的组成。下图装置是用燃烧法确定...”考查相似的试题有:
- 下列说法正确的是[ ]A.某烃燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物组成为CnH2nB.一种烃在足量的氧气中燃烧并...
- 某课外小组欲通过实验证明方铅矿分解所得白色粉末中含有氧元素,设计以下的实验装置:在实验或改进实验中,可能发生的化学反...
- 为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g,用下图所示装置进行实验(铁架台、铁夹等仪器未在图中画出)(1)将...
- 某有机物在氧气中充分燃烧,生成等物质的量的水和二氧化碳,则该有机物必须满足的条件是( )A.分子中的C、H、O的个数比为1...
- 某校化学兴趣小组的同学欲测定某种品牌味精中食盐的含量.下面是该小组所做的有关实验步骤:①称取某品牌袋装味精样品10.0g放...
- 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.(1)写出试管B中的实验现象______.(2)写出A中反应的化学方程式_...
- 某固体混合物可能含有CuCl2、KCl、NaOH、(NH4)2SO4中的两种,通过实验确定其组成:取少量固体溶于水,得到蓝色溶液;向该溶...
- 某化学课外活动小组,从化学手册上查得硫酸铜在500 ℃以上按下式分解:CuSO4CuO+SO2↑+SO3↑+O2↑,便决定设计一验证性实验探索测...
- 有由Na2O、Na2O2、Na2CO3、NaHCO3、NaCl中的几种物质组成的混合物.向混合物中加入足量的盐酸,有气体放出.将放出的气体通过...
- 某实验小组利用如下装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式.(1)按图连接好实验装置.检查装置的气密...