本试题 “中国科学院兰州近代物理研究所曾研制出首批重氧气(18O2),其价格远远超过黄金。下面对由18O构成的过重氧化氢(1H218O2)的叙述中正确的是(用NA表示阿伏加...” 主要考查您对摩尔质量
阿伏加德罗常数
氢键
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 摩尔质量
- 阿伏加德罗常数
- 氢键
摩尔质量:
定义:单位物质的量的物质所具有的质量
符号:M
单位:g/mol(g·mol-1)
计算公式:摩尔质量(M)=质量(m)/物质的量(n)
摩尔质量、相对分子质量、1mol物质的质量三者的区别和联系:
1mol物质的质量在数值上和摩尔质量相同,二者的区别在于单位不一样,质量的单位是千克(kg),而摩尔质量的单位是g/mol。相对分子质量与摩尔质量单位不同,但在数值上二者相等。
平均摩尔质量的计算方法:
- 已知混合物质的总质量m(混)和总物质的量n(混):M =m(混)/n(混)
- 已知同温同压下混合气体的密度ρ(混)是一种简单气体A的密度ρ(A)的倍数d(也叫相对密度)d= ρ(混)/ ρ(A),则M混= ρ混M混/ ρ(A)
- 在溶液中,M=1000ρw%/c(ρ指溶液的密度,w%指溶液中溶质的质量分数,c表示溶液的浓度)
- 已知某状况下的混合气体的密度M=ρVm(ρ表示气体的密度,Vm表示在该状况下的气体的摩尔体积)
- 已知混合物各成分的摩尔质量和其在混合体系内的物质的量分数或体积分数M=M1×n1%+M2×n2% =M1×V1%+M2×V2%
阿佛加德罗常数:
1mol粒子集体所含离子数与0.012kg碳12中所含的碳原子数相同,约为6.02×1023。
把1mol任何粒子的粒子数叫阿伏加德罗常数。
符号:NA,通常用6.02×1023mol-1表示
阿佛加德罗常数的单位:
阿佛加德罗常数是有单位的量,其单位是:mol-1,需特别注意。
阿佛加德罗常数的正误判断:
关于阿伏加德罗常数(NA)的考查,涉及的知识面广,灵活性强,是高考命题的热点。解答该类题目时要细心审题,特别注意题目中的关键性字词,留心“陷阱”。主要考查点如下:
1.考查“标准状况”、“常温常压”等外界条件的应用
(1)在标准状况下非气态物质:如H2O、SO3、戊烷、CHCl3、CCl4、苯、乙醇等,体积为22.4L时,其分子数不等于NA。
(2)注意给出气体体积是否在标准状况下:如11.2LH2的分子数未必是0.5NA。
(3)物质的质量、摩尔质量、微粒个数不受外界条件的影响。
2.考查物质的组成
(1)特殊物质中所含微粒(分子、原子、电子、质子、中子等)的数目:如Ne、D2O、18O2、H37Cl、—OH等。
(2)某些物质的阴阳离子个数比:如NaHSO4晶体中阴、阳离子个数比为1∶1,Na2CO3晶体中阴、阳离子个数比为1∶2。
(3)物质中所含化学键的数目:如H2O2、CnH2n+2中化学键的数目分别为3、3n+1。
(4)最简式相同的物质中的微粒数目:如NO2和N2O4,乙烯和丙烯等。
3.考察氧化还原反应中电子转移的数目
如:Na2O2、NO2与H2O的反应;Cl2与H2O、NaOH溶液、Cu或Fe的反应;电解AgNO3溶液、NaCl溶液等。
4.考查弱电解质的电离及盐的水解
如1L0.1mol/L的乙酸溶液和1L0.1mol/L的乙酸钠溶液中的CH3COO-的数目不相等且都小于0.1NA;1L0.1mol/L的NH4NO3溶液中c(NH4+)<0.1mol/L,但含氮原子总数仍为0.2NA;1molFeCl3水解生成Fe(OH)3胶粒的数目远远小于NA。
5.考查一些特殊的反应
如, 1molN2与3H2反应实际生产中得不到2molNH3,因是可逆反应;标准状况下2.24LO2和2.24LNO混合后,由于发生:2NO+O2==2NO2和
1molN2与3H2反应实际生产中得不到2molNH3,因是可逆反应;标准状况下2.24LO2和2.24LNO混合后,由于发生:2NO+O2==2NO2和![]() 两个反应,使2.24L<V<3.36L。
两个反应,使2.24L<V<3.36L。
有关NA的问题中常见的几种特殊情况:
有关NA的问题分析中易忽视如下问题而导致错误:
(1)碳原子超过4个的烃类物质、标准状况下的SO3等均不是气体,不能使用“22.4L/mol”来讨论问题。
(2)Na2O2由Na+和O22-构成,而不是由Na+和O2-构成,阴阳离子个数比为1:2而不是1:1.
(3)SiO2结构中只有原子无分子,1molSiO2中含有共价键数为4NA
氢键:
(1)概念:已经与电负性很大的原子(如N、O、F) 形成共价键的氢原子与另一个电负性很大的原子(如 N、O、F)之问的作用力。如水分子问的氢键如下图所示。 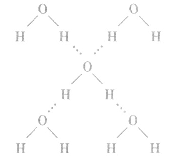
(2)表示方法:A—H…B一(A、B为N、O、F“一” 表示共价键,“…”表示形成的氢键)。
(3)分类
(4)属性:氢键不属于化学键,它属于一一种较强的分子间作用力,其作用能大小介于范德华力和化学键之间。
(5)对物质性质的影响
①氢键对物质熔、沸点的影响。分子问存在氧键时,破坏分子问的氢键,需要消耗更多的能量,所以存在氢键的物质具有较高的熔点和沸点。
例如:氮族、氧族、卤素中的N、O、F的氧化物的熔、沸点的反常现象。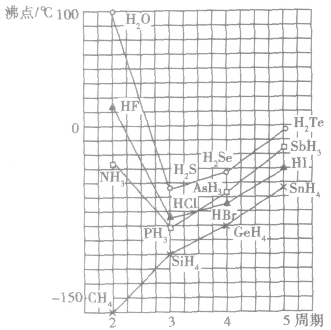
②氢键对物质溶解度的影响:氢键的存在使物质的溶解性增大。例如:NH3极易溶解于水,主要是由于氨分子和水分子之问形成了氢键,彼此互相缔合,因而加大了溶解。再如乙醇、低级醛易溶于水,也是因为它们能与水分子形成氢键。
③氢键的存在会引起密度的变化。水结冰时体积膨胀、密度减小的反常现象也可用氢键解释:在水蒸气中水以单个的水分子形式存在;在液态水中,通常是几个水分子通过氢键结合,形成(H2O)n小集团;在固态水(冰)中,水分子大范围地以氢键互相连接,成为疏松的晶体,因此在冰的结构中有许多空隙,造成体积膨胀,密度减小。
④分子内氢键与分子间氢键对物质性质的不同影响:氢键既可以存在于分子内部的原子之间,也可以存在于分子间的原子之间,只不过这两种情况对物质性质的影响程度是不一样的。例如,邻羟基苯甲醛存在分子内氢键: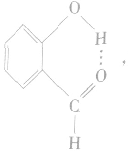 熔点为2℃,沸点为196. 5℃;对羟基苯甲醛存在分子间氢键:
熔点为2℃,沸点为196. 5℃;对羟基苯甲醛存在分子间氢键: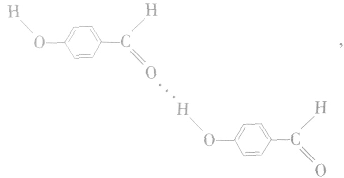 熔点为 115℃,沸点为250℃。由此可见,分子间氢键使物质的熔、沸点更高。
熔点为 115℃,沸点为250℃。由此可见,分子间氢键使物质的熔、沸点更高。
6)存在:水、醇、羧酸、酰胺、氨基酸、蛋白质、结晶水合物等物质中都能存在;生命体中许多大分子内也存在氢键,如氢键是蛋白质具有生物活性的高级结构的重要原因,DNA双螺旋的两个螺旋链也是以氢键相互结合的。
与“中国科学院兰州近代物理研究所曾研制出首批重氧气(18O2),...”考查相似的试题有:
- 下列叙述完全正确的一组是( )①一定条件,气体的摩尔体积为11.2L②由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极放出0.2g H2,...
- 下列叙述中正确的是[ ]A.1mol任何物质都含有约6.02×1023个原子B.硫酸的摩尔质量是98gC.1mol N2的质量是28gD.摩尔是国际单...
- 阿伏加德罗常数约为6.02×1023mol-1,下列说法正确的是[ ]A.标准状况下22.4 L NO与11.2 L O2混合后所得气体分子数为6.02×1023...
- 下列关于磷酸(H3PO4)的说法中正确的是[ ]A.1molH3PO4的质量为98g/molB.H3PO4的摩尔质量为98gC.9.8g H3PO4含有NA个H3PO4分...
- 下列说法中,正确的是( ) A.2g氢气所含的原子数为NA B.1mol氢气所占的体积约为22.4L C.1mol氢气的质量是2g/mol D.H2的...
- 若NA表示阿伏加德罗常数的值,下列说法不正确的是[ ]①C2H6分子中既含极性键又含非极性键②若R2-和M+的电子层结构相同,则原子...
- 设NA表示阿伏加德罗常数的值。下列说法正确的是[ ]A.1mol乙醛中含C-H键的数目为3NAB.1 L浓度为1 mol/L的醋酸钠溶液中含有NA...
- 设NA为阿伏加德罗常数的值.下列关于0.2mol/LBa(NO3)2溶液不正确的说法是( )A.2L溶液中有阴、阳离子总数为0.8NAB.500mL...
- 光健康、太阳能、绿色节能、零排放等高科技点亮2010上海世博。(1)世博园区外围设置生态化停车场,有害尾气被纳米光触媒涂料分...
- (1)金属钛(22Ti)将是继铜、铁、铝之后被人类广泛使用的第四种金属,请写出钛的基态原子的电子排布式:____ 。(2)二氧化钛可作...