本试题 “关于苯分子结构的研究经历了很长一段时间。著名科学家凯库勒最先提出了凯库勒结构式,并较好地解释了苯的一些性质。但随着理论研究的不断深入,杂化轨道理论...” 主要考查您对杂化轨道理论(中心原子杂化方式)
σ键、π键
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 杂化轨道理论(中心原子杂化方式)
- σ键、π键
杂化轨道理论:
是鲍林为了解释分子的立体结构提出的。中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见杂化方式:
(1)sp杂化:直线型 如:CO2、CS2
(2)sp2杂化:平面三角形(等性杂化为平面正三角形) 如:BCl3 C2H4
不等性杂化为V字型 如:H2O H2S OF2
(3)sp3杂化:空间四面体(等性杂化为正四面体) 如:CH4、CCl4
不等性杂化为三角锥 如:NH3 PCl3 H3O+
sp3d杂化:三角双锥
sp3d2杂化:八面体(等性杂化为正八面体)
是鲍林为了解释分子的立体结构提出的。中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见杂化方式:
(1)sp杂化:直线型 如:CO2、CS2
(2)sp2杂化:平面三角形(等性杂化为平面正三角形) 如:BCl3 C2H4
不等性杂化为V字型 如:H2O H2S OF2
(3)sp3杂化:空间四面体(等性杂化为正四面体) 如:CH4、CCl4
不等性杂化为三角锥 如:NH3 PCl3 H3O+
sp3d杂化:三角双锥
sp3d2杂化:八面体(等性杂化为正八面体)
分子的构型与杂化类型的关系:
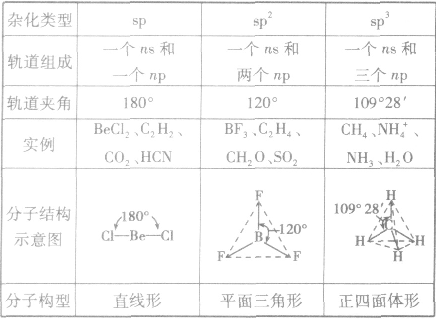
σ键:
成键原子的电子云以“头碰头”方式重叠形成的共价键,其特征是轴对称,即以形成化学键的两原子核的连线为轴作旋转,共价键的电子云图形不变。
π键:
成键原子的电子云以“肩并肩”方式形成的共价键,其特征是镜像对称,即:电子云由两块组成,若以包含原子核的平面为镜面,两块电子云互为镜像。
成键原子的电子云以“头碰头”方式重叠形成的共价键,其特征是轴对称,即以形成化学键的两原子核的连线为轴作旋转,共价键的电子云图形不变。
π键:
成键原子的电子云以“肩并肩”方式形成的共价键,其特征是镜像对称,即:电子云由两块组成,若以包含原子核的平面为镜面,两块电子云互为镜像。
共价键的分类:
(1)按成键原子是否相同或共用电子对是否偏移分 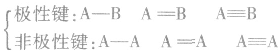
(2)按成键方式分

(3)按共用电子对数分
发现相似题
与“关于苯分子结构的研究经历了很长一段时间。著名科学家凯库勒...”考查相似的试题有:
- 按要求填写表格。
- 下列分子的中心原子发生sp2杂化的是( ) A.CH4 B.NH3 C.H2O D.BF3
- (1)由A、B两元素组成的离子晶体结构(甲)如图所示,则该晶体的化学式是:___________。(2)C原子的最外层电子排布为nsnnpm,...
- (1)金属钛(22Ti)将是继铜、铁、铝之后被人类广泛使用的第四种金属,请写出钛的基态原子的电子排布式:____ 。(2)二氧化钛可作...
- 下表为长式周期表的一部分,其中的编号代表对应的元素.① ② ③ ④ ⑤ ⑥⑦ ⑧ ⑨⑩ 请回答下列问题:(1)表中属于d区的元素是______...
- 硫酸铜晶体溶解后溶液呈天蓝色,再滴加氨水,首先生成沉淀,继续滴加氨水,沉淀溶解,得到深蓝色透明溶液,再加入无水乙醇,...
- 2008年的秋天,毒奶粉事件震惊全国,这主要是奶粉中含有有毒的三聚氰胺(分子结构如图所示).下列关于三聚氰胺分子的说法中...
- 下图物质结构图中,.代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成...
- 下列有关分子中的化学键描述不正确的是[ ]A.苯分子中每个碳原子的sp2杂化轨道形成σ键,未参加杂化的2p轨道形成大π键B.乙炔...
- (二选一)黄血盐(亚铁氰化钾,K4[Fe(CN)6] )易溶于水,广泛用做食盐添加剂(抗结剂),食盐中黄血盐的最大使用量为10 mg·kg...