本试题 “已知在含氧酸中只有H原子与O原子相连时,才能在水溶液中电离出H+。次磷酸与足量的氢氧化钠溶液 反应的产物为NaH2PO2,又知浓度均为0.1mol/L的次磷酸(H3PO2)与...” 主要考查您对电离方程式
弱电解质的电离
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电离方程式
- 弱电解质的电离
定义:
表示电解质电离的式子。强电解质电离用“=”,弱电解质电离用“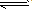 ” 。
” 。
.
表示电解质电离的式子。强电解质电离用“=”,弱电解质电离用“
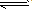 ” 。
” 。.
电离方程式的书写:
1.强电解质的电离用“ ”,弱电解质的电离用 “
”,弱电解质的电离用 “ ”。
”。
2.多元弱酸分步电离,分步持写电离方程式,一般只写第一步;多元弱碱也是分步电离的,但可按一步完全电离写出。例如:
氧硫酸: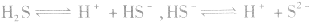
氢氧化铁:
3.强酸的酸式盐完全电离,弱酸的酸式盐中酸式酸根不完全电离。例如: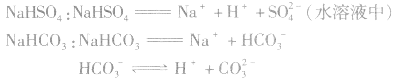
说明:在熔融状态时,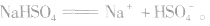
4.某些复盐能完全电离。例如:
定义:
在一定温度、浓度的条件下,弱电解质在溶液中电离成离子的速率与离子结合成分子的速率相等时,电离过程就到了电离平衡状态,叫弱电解质的电离平衡。

电离平衡的特征:
(1)等:
(2)动: 的动态平衡
的动态平衡
(3)定:条件一定,分子与离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。
在一定温度、浓度的条件下,弱电解质在溶液中电离成离子的速率与离子结合成分子的速率相等时,电离过程就到了电离平衡状态,叫弱电解质的电离平衡。

电离平衡的特征:
(1)等:

(2)动:
 的动态平衡
的动态平衡(3)定:条件一定,分子与离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。
发现相似题
与“已知在含氧酸中只有H原子与O原子相连时,才能在水溶液中电离...”考查相似的试题有:
- 下列电离方程式中,正确的是( ) A.H2SO4=H2++SO42- B.NaClO=Na++Cl-+O2- C.NaNO3=Na++NO3- D.MgSO4=Mg+2+SO42-
- 下列叙述中一定正确的是[ ]A.0.1mol/L的CH3COOH溶液中,由水电离的c(H+)为10-13mol/LB.pH=2与pH=1的CH3COOH溶液中c(H+)之...
- 下列比值为2∶1的是[ ]A.pH=2与pH=1的硝酸中c(H+)之比B.Na2CO3溶液中c(Na+)与c(CO32-)之比C.0.2mol/L与0.1mol/L醋酸中c(H...
- (1)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ.则表示甲烷燃烧热的热化学方程式为______.(2)下表中的数...
- 某温度下,相同体积、相同pH的氨水和氢氧化钠溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是A.a点导电能力比b点强B...
- 某二元弱酸(简写成H2A)溶液,按下式发生一级和二级电离:H2A⇌H++HA-,HA-⇌H++A2-,已知同浓度时电离程度H2A远大于HA-.设有...
- 向0.1 mol/L的氨水溶液中加水稀释或加入少量NH4Cl固体时均会引起变化的是( )A.溶液的导电能力减弱B.溶液的pH变小C.NH3·H...
- (14分)某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。实验一 配制并标定醋酸溶液的浓度取冰醋酸配制250 mL 0.4 m...
- (1)某温度下,纯水的c(H+)=2×10-7mol-L-1,则此时c(OH-)为______;若温度不变,滴入稀盐酸使c(H+)=5×10-4mol-L-1则溶...
- 醋酸溶液中存在电离平衡CH3COOH⇌H++CH3COO-,下列叙述不正确的是( )A.0.10mol/L醋酸溶液中粒子浓度的关系满足:c(CH3COOH...