本试题 “分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题(1)以下叙述中,正确的是________________。A....” 主要考查您对能量的相互转化
原电池原理
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 能量的相互转化
- 原电池原理
能量的相互转化:
化学反应中的能力变化表现为热量的变化。常见能量转化有:化学能和电能的相互转化、化学能和热能的相互转化、化学能和光能、风能的相互转化等。
如:燃料燃烧产生能量最终带动发电机发电,将化学能转化为电能;铜、锌形成原电池,将化学能转化为电能。
原电池:
1.定义:将化学能转化为电能的装置。
2.工作原理:
以铜-锌原电池为例
(1)装置图:
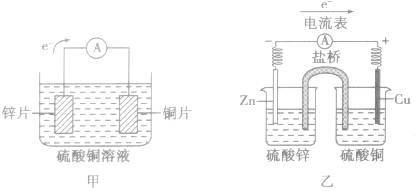
(2)原理图:
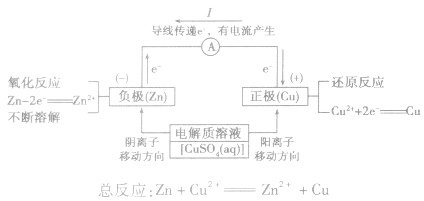
3.实质:化学能转化为电能。
4.构成前提:能自发地发生氧化还原反应。
5.电极反应:
负极:失去电子;氧化反应;流出电子
正极:得到电子;氧化反应;流入电子
6.原电池正负极判断的方法:
①由组成原电池的两级材料判断,一般是活泼金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②根据电流方向或电子流动方向判断,电流是由正极流向负极,电子流动方向是由负极流向正极。
③根据原电池里电解质溶液内离子的定向移动方向,在原电池的电解质溶液中,阳离子移向正极,阴离子移向负极。
④根据原电池两级发生的变化来判断,原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
⑤X极增重或减重:X极质量增加,说明溶液中的阳离子在X极(正极)放电,反之,X极质量减少,说明X极金属溶解,X极为负极。
⑥X极有气泡冒出:发生可析出氢气的反应,说明X极为正极。
⑦X极负极pH变化:析氢或吸氧的电极发生反应后,均能使该电极附近电解质溶液的pH增大,X极附近的pH增大,说明X极为正极。
1.定义:将化学能转化为电能的装置。
2.工作原理:
以铜-锌原电池为例

(1)装置图:

(2)原理图:

3.实质:化学能转化为电能。
4.构成前提:能自发地发生氧化还原反应。
5.电极反应:
负极:失去电子;氧化反应;流出电子
正极:得到电子;氧化反应;流入电子
6.原电池正负极判断的方法:
①由组成原电池的两级材料判断,一般是活泼金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②根据电流方向或电子流动方向判断,电流是由正极流向负极,电子流动方向是由负极流向正极。
③根据原电池里电解质溶液内离子的定向移动方向,在原电池的电解质溶液中,阳离子移向正极,阴离子移向负极。
④根据原电池两级发生的变化来判断,原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
⑤X极增重或减重:X极质量增加,说明溶液中的阳离子在X极(正极)放电,反之,X极质量减少,说明X极金属溶解,X极为负极。
⑥X极有气泡冒出:发生可析出氢气的反应,说明X极为正极。
⑦X极负极pH变化:析氢或吸氧的电极发生反应后,均能使该电极附近电解质溶液的pH增大,X极附近的pH增大,说明X极为正极。
原电池中的电荷流动:
在外电路(电解质溶液以外),电子(负电荷)由负极经导线(包括电流表和其他用电器)流向正极,使负极呈正电性趋势、正极呈负电性趋势。在内电路(电解质溶液中),阳离子(带正电荷)向正极移动,阴离子 (带负电荷)向负极移动。这样形成了电荷持续定向流动,电性趋向平衡的闭合电路。
发现相似题
与“分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为...”考查相似的试题有:
- 中和热测定实验中,下列操作一定会降低实验准确性的是A 用滴定管(精量仪器,读数保留到0.01)取所用酸碱溶液的体积B NaOH溶...
- 已知反应:①②稀溶液中,,下列结论正确的是:A.碳的燃烧热大于110.5kJ/molB.①的反应热为221kJ/molC.稀硫酸与稀NaOH溶液反应...
- 目前合成氨的技术原理为:该反应的能量变化如图所示。在反应体系中加入催化剂,反应速率增大,△H的变化是A.增大B.减小C.不...
- 已知有:(l) =H2O(g) △H1=a kJ·(2) =2H2O(g) △H2=b kJ·(3)=H2O(l) △H3=c kJ·(4) =2H2O(l) △H4=d kJ·...
- 光伏组件采用高效率单晶硅或多晶硅光伏电池、高透光率钢化玻璃、抗腐蚀铝合多边框等材料,使用先进的真空层压工艺及脉冲焊接...
- 氢氧燃料电池以氢气作还原剂,氧气作氧化剂,电极为多孔镍,电解质溶液为30%的氢氧化钾溶液。以下几种说法,正确的组合是( ...
- 以下装置能形成原电池的是( )A.B.C.D.
- 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如下图所示装置。试回答下列问题:(1)若电解质溶液为稀硫酸,则Zn棒为...
- 根据右图可判断下列离子方程式中错误的是( )A.2Ag(s)+Cd2+(aq)=2Ag+(aq)+Cd(s)B.Co2+(aq)+Cd(s)=Co(s)+Cd2...
- 把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池.若A、B相连时,A为负极;C、D相连,D上有气泡逸出;...